Из этого следует, что основные компоненты в огарке представлены следующими фазами; цинк в виде ZnO, ZnFe2O4, ZnO·2 ZnSО4, Zn2SiO4ZnS; железо в виде Fe3O4, Fe2O3, ZnFe2O4; свинец в виде PbSO4, PbO·PbSO4, 2PbO·PbSO4, PbO, Pb2SiO4, PbS; медь в виде CuFe2O4, CuSO4, CuO·CuSO4, Cu2S, борнита Cu2O и Cu0. Для достижения низких содержаний сульфидной серы в огарке неблагоприятно сочетание заметных количеств сульфидов меди и свинца в концентрате из-за образования легкоплавкой эвтектики PbS - Cu2S (борнит), у которой tпл = 5400С [17].
1. Теория обжига цинковых концентратов
Обжиг — сложный гетерогенный процесс, связанный с явлениями адсорбции, десорбции, диффузии и рядом различных химических взаимодействий.
Химизм реакций окисления сульфидов металлов в работах различных исследователей трактуется по-разному. Существуют две теории обжига - оксидная и сульфатная [7].
По оксидной теории окисление сульфида любого двухвалентного металла можно представить следующими уравнениями:
2MeS + 3O2 = 2MeO + 2SO2; (1.11)
2SO2 + O2 ↔ 2SO3; (1.12)
MeO + SO3 ↔ MeSO4 (1.13)
Согласно этой теории, при обжиге вначале образуются окислы, которые при благоприятных условиях (большая концентрация сернистых газов и низкая температура) могут дать с серным ангидридом сульфаты металлов.
Таким образом, сульфаты получают только из окислов.
По сульфатной теории окисление протекает иначе:
MeS + 2O2 = MeSO4, (1.14)
MeSO4 ↔ MeO + SO3 (1.15)
2SO3 ↔ 2SO2 + O2, (1.16)
MeO + SO3 ↔ MeSO4. (1.17)
Согласно этой теории, при обжиге сульфидов сначала образуются только сульфаты, которые потом разлагаются с выделением окислов металлов. Полученные окислы при благоприятных условиях могут вновь прореагировать с серным ангидридом и образовать сульфаты вторичной формации.
Существует и третья, видимо, наиболее верная, точка зрения, по которой при низких температурах обжига первичным продуктом является сульфат, а при высоких окисление идет непосредственно до окислов, минуя сульфатную стадию.
Окисел или сульфат при обжиге сульфида образуется по следующим конечным реакциям:
MeS+1,5O2=MeO+SO2 (1.18)
2SO2+O2↔2SO3, (1.19)
MeO+SO3↔MeSO4. (1.20)
Реакции окисления протекают на поверхности твердых частиц сульфидов и сопровождаются образованием сернистого ангидрида. По мере протекания обжига поверхность сульфидных зерен постепенно покрывается пленкой, состоящей из окислов и сульфатов. Кроме того, зерна обжигаемого материала обволакиваются сернистым ангидридом, образующим газовую оболочку, также препятствующую диффузии кислорода внутрь сульфидных зерен. По мере утолщения пленки из окислов и газов на зернах обжигаемого материала процесс диффузии кислорода к поверхности сульфида замедляется, так как кислород и движущиеся навстречу ему обжиговые газы встречают возрастающее сопротивление.
Сульфиды, декриптирующие при нагревании (FеS2, СuFеS2), обжигаются быстрее и легче [14]. Цинковая обманка не декриптирует, является плотным сульфидом и обжигается с большими трудностями.
Некоторые сульфиды при температуре обжига диссоциируют с выделением атома серы. Сера, выделяясь, оставляет в сульфидном зерне поры, облегчающие диффузию кислорода и ускоряющие обжиг. Цинковая обманка практически не диссоциируется при обжиге, что также замедляет процесс ее окисления.
При обжиге сульфидных материалов интенсивность и полнота окисления возрастают с уменьшением крупности помола, так как при этом достигается более полный контакт поверхности частиц с кислородом.
При повышении температуры возрастает скорость окисления, и обжиг проводят при максимально допустимой температуре. Большой избыток воздуха ускоряет окисление сульфидов, но вызывает разбавление сернистых газов.
С точки зрения термодинамики, отражающей окончательный результат взаимодействия отдельных компонентов, процесс обжига концентрата характеризуется величиной изменения изобарно-изотермического потенциала реакций окисления. Сравнение этих величин для однотипных реакций позволяет оценить предпочтительность протекания одной реакции перед другой. Из нескольких однотипных реакций предпочтительно протекает та, для которой изменение стандартного изобарно-изотермического потенциала выражается наиболее отрицательной величиной.
Присутствующий в концентрате сульфид цинка окисляется по схеме:
ZnS + 2О2 = ZnSO4 (1.21)
3ZnSO4 + ZnS ↔ 4ZnO + 4SО2 (1.22)
3ZnSО4 ↔ 3ZnO·2SO3 + SО2 + 1/2О2 (1.23)
3ZnО · 2SО3 ↔ 3ZnО + 2SО2 + О2 (1.24)
В продуктах обжига получаются ZnО и ZnSО4 в соотношениях, зависящих от условий обжига, которые были рассмотрены выше.
Независимо от способа проведения окислительного обжига, он
является процессом автогенным из-за экзотермического характера окисления
сульфидов:
2ZnS + ЗО2 = 2ZnО + 2SO2 + 212,8 ккал/г-моль; (1.25)
ZnS + 2О2 = ZnSО4 + 185,4 ккал/г-моль; (1.26)
2FeS2 + 3,5O2 = Fe2О3 + 4SО2 + 396,2 ккал/г-моль. (1.27)
Кинетические закономерности процесса взаимодействия газа с твердым веществом определяются кристаллохимическими превращениями и диффузией газа между реакционной поверхностью и внешней газовой средой, а также условиями теплообмена [12].
Кинетику обжига минералов сфалерита, марматита и цинкового концентрата в кипящем слое изучал . Он показал, что при 800 оС окисление воздухом зерен размером 0,27 мм практически заканчивается за 20 мин.
На скорость окисления сернистого цинка сильно влияет температура обжига. Экспериментально установлено, что окисление зерен сульфида размером 0,92 мм при температуре 900 °С протекает примерно в 6 раз быстрее, чем при 800°С и практически заканчивается за 10 мин. Цинка в форме сульфида остается 3,63% от общего содержания. При температуре 700 °С и продолжительности 180 мин в форме сульфида остается 24,6% Zn. В этом случае скорость обжига примерно в 18 раз меньше, чем при температуре 800 °С. Процесс окисления сульфида цинка может протекать в кинетической, диффузионной и промежуточной областях. При низких температурах пока скорость реакции мала по сравнению со скоростью диффузии (кинетическая область), суммарная скорость реакции определяется истинной кинетикой на поверхности и экспоненциально возрастает с повышением температуры согласно закону Аррениуса. Но это возрастание продолжается только до тех пор, пока скорость реакции не сделается соизмеримой со скоростью диффузии. В дальнейшем процесс перейдет в диффузионную область, где скорость его всецело определяется скоростью диффузии и весьма слабо возрастает с повышением температуры. При такой зависимости скорости выделения тепла от температуры и при определенных условиях теплоотдачи возможны три стационарных тепловых режима, из которых средний оказывается неустойчивым, верхний отвечает протеканию в диффузионной и нижний - в кинетической области. Воспламенение поверхности представляет собой скачкообразный переход от нижнего к верхнему стационарному тепловому режиму.
Зависимость скорости окисления сульфида цинка воздухом в интервале температур от 470 до 1100 °С приведена на рис. 1.1. Кривая имеет две резко отличающиеся ветви: нижнюю, отвечающую кинетической области, и верхнюю - для диффузионной области.
Применение воздуха, обогащенного кислородом, при обжиге цинковых концентратов дает возможность увеличить скорость обжига, и тем самым увеличить производительность печи, повысить содержание сернистого ангидрида в газах, удешевить очистку газов от пыли, уменьшить потери тепла с отходящими газами.
При повышении содержания кислорода в газовой смеси с 21 до 78% скорость процесса возрастает примерно вдвое. При всех температурах огарок содержит вдвое меньше силикатного и ферритного цинка, что указывает на возможность повышения извлечения цинка при выщелачивании.
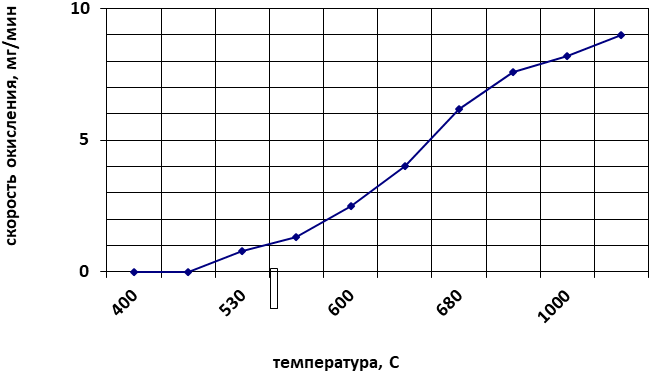
Рис. 1.1. Зависимость скорости окисления сульфида цинка воздухом от
температуры
ИССЛЕДОВАНИЕ ПРОЦЕССОВ ОБРАЗОВАНИЯ ФЕРРИТОВ И СИЛИКАТОВ ПРИ ОБЖИГЕ СУЛЬФИДНЫХ ЦИНКОВЫХ КОНЦЕНТРАТОВ
Ферритообразование. При наличии в цинковых концентратах минерала марматита (mZnS·nFeS) или сульфидов железа в процессе обжига образуется метаферрит цинка ZnO·Fe2O3, который не растворяется в слабой серной кислоте и остается неизменным в остатке от выщелачивания огарка, снижая тем самым прямое извлечение цинка в раствор. Количество образующегося метаферрита цинка тем больше, чем выше содержание железа в цинковом концентрате [7,15]. Поэтому перед обогатительными фабриками всегда стоит задача снижения содержания железа в продуктах цинковой флотации, а действующий отраслевой стандарт ограничивает его содержание в цинковых концентратах следующими пределами:
Марка концентрата | КЦ1 | КЦ2 | КЦ3 | КЦ4 |
Допустимое содержание железа, % | 5 | 7 | 9 | 12 |
В процессе обжига цинкового концентрата внутри зерно оксид цинка взаимодействует с окисью железа Fе2О3, образуя метаферрит цинка по следующий реакции.
ZnO + Fe2O3 = ZnO⋅Fe2O3 (2.1)
При температуре 650°С это реакция протекает весьма интенсивно, поэтому проведение обжига при температуре 700-750 °С не исключает образования феррита цинка, так как цинковые концентраты содержат железо, то предотвратить образование феррита цинка при обжиге невозможно.. Он не растворяется в слабой серной кислоте и остается в остатке от выщелачивания обожженного концентрата, что приводит к прямым потерям цинка.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |




