Глава 3. ИЗУЧЕНИЕ КИНЕТИКИ РЕАКЦИЙ ВЗАИМОДЕЙСТВИЯ ВОДЯНОГО ПАРА С ТВЁРДЫМИ МАТЕРИАЛАМИ
При обогащении дутья кислородом в пирометаллургическом агрегате ( печи «КС» и вельцпечи в металлургии цинка ) развиваются достаточно высокие температуры [15, 16, 17], что приводит к образованию нежелательных соединении, как ферриты-силикаты цинка, клинкера и потерия редких металлов отходящими газами, а также преждевременному износу футеровки. Этот факт послужил толчком для исследований по использованию эндотермических реакций сульфидов металлов с водой в качестве терморегулятора [18 - 20]. В области взаимодействия расплавов сульфидов железа и меди с водяным паром накоплен значительный экспериментальный материал, который, по нашему мнению, весьма при трактовке химизма процессов низкотемпературного окисления сульфидов металлов водяным паром.
В связи с этим рассмотрим результаты по кинетике и механизму взаимодействия расплавленных сульфидов металлов с водяным паром, а также имеющиеся в литературе сведения по окислению твердых сульфидов железа и цветных металлов водяным паром.
3.1. Общая характеристика кинетических реакций взаимодействия водяного пара с сульфидными минералами металлов.
Среди многообразия процессов, использующих пар в качестве основного и вспомогательного реагента, значительное место занимает физическая адсорбция - одна из основных стадий при взаимодействии пара с твердым материалом. Такие процессы называют топохимическими. Рассмотрим краткую характеристику общих закономерностей топохимических реакций. Как при обсуждении закономерностей любой химической реакции, используем понятие реакционной способности.
Количественной мерой такой способности является удельная скорость реакции. Зависимость скорости химической реакции (или количества прореагировавшего вещества) от условий эксперимента выражается кинетическим уравнением. Для простейшей (одностадийной) химической реакции оно монет быть составлено на основе системы постулатов. Основное допущение состоит в том, что химические реакции происходят при соударении статистически независимых частиц. Тогда скорость реакции пропорциональна числу соударений, а следовательно, и концентрации частиц в степени, показатель которой определяется числом частиц, участвующих в столкновении. Так как в топохимических процессах реализация этого допущения представляется маловероятной, то при описании взаимодействия твердых неорганических веществ лежат следующие общие кинетические принципы [23].
- скорость реакции твердого тела пропорциональна суммарной эффективной площади границы раздела реагент - продукт;
- в изотропном реагенте скорость продвижения границы раздела в изотермических условиях постоянна;
- в подавляющем большинстве твердофазных реакций температурная зависимость константы скорости описывается уравнением Аррениуса;
- когда одна иди несколько фаз продукта образует слой препятствующий прямому контакту между реагентами, суммарная скорость реакции контролируется диффузией их через этот слой;
- скорость реакции твердого тела с газом может зависеть от концентрации газа.
Кроме перечисленных принципов, относящихся главным образом к скорости продвижения границы раздела, на кинетические характеристики могут существенно влиять и такие факторы, как степень превращения б, распределение по размерам частиц реагента, его предварительная обработка, обратимость реакции, плавление, медленный рост докритических зародышей, неравномерность распределения температуры внутри реагента и ряд других.
Химические реакции, как правило, являются многостадийными процессами. Это ведет к усложнению кинетических закономерностей. Для одностадийной реакции А → В справедливо кинетическое уравнение
![]() (3.1)
(3.1)
где V - объем; nA - .количество вещества А; К – константа скорости реакции; С0 - начальная концентрация.
В случае системы двух последовательных реакций А → В, В → С для каждой из них можно написать:
![]() (3.2)
(3.2)
![]() (3.3)
(3.3)
Тогда
![]() (3.4)
(3.4)
Решение этой системы приводит к следующему уравнению:
![]() (3.5)
(3.5)
Процесс, в котором концентрация реагента А, промежуточного вещества В и продукта реакции С изменяются во времени, называют нестационарным. В нём скорости расхода реагентов и образования продуктов реакции не равны друг другу. Решение (3.5) можно получить лишь для системы последовательных реакций первого порядка. В случае реакций более высокого порядка для получаемых систем нелинейных дифференциальных уравнений пока не найдены точные решения.
Систему последовательных реакций называют стационарной, если скорости всех стадий не изменяются во времени. Условие стационарности для процесса ![]() можно записать в виде
можно записать в виде
![]() (3.6)
(3.6)
Тогда
![]() (3.7)
(3.7)
Таким образом скорость суммарного процесса определяется скоростью первой стадии. Как видно на примере простейших двухстадийных процессов, кинетическое уравнение суммарной реакции зависит от её механизма. В ряде случаев это позволяет решить обратную задачу: выяснить механизм реакции по кинетическим данным. Так, в рамках рассматриваемой модели кинетическая кривая в виде прямой линии означает, что данный процесс стационарен и имеет лимитирующую стадию, конкретный вид которой уточняется в ходе дополнительных исследований. В тех случаях, когда скорость реакции увеличивается (что характерно для большинства топохимических реакций), процесс нестационарен.
Химические реакции, имеющие хотя бы один твердый реагент и твердый продукт реакции, характеризуются специфическими кинетическими закономерностями. В начальный период скорость реакции мала, затем возрастает, проходит через максимум и снижается практически до нуля. Принято различать интегральную кинетическую кривую, отражающую зависимость степени превращения б от продолжительности (рис. 3.1,а), и дифференциальную кривую показывающую изменение скорости процесса (рис. 3.1, б).
а - интегральная; б - дифференциальная
Рис. 3.1. Типичные кинетические кривые топохимических реакций
Как показано выше, условию ![]() отвечают нестационарные процессы. Современная теория топохимических превращений связывает нестационарность процесса прежде всего о изменением площади реакционной поверхности.
отвечают нестационарные процессы. Современная теория топохимических превращений связывает нестационарность процесса прежде всего о изменением площади реакционной поверхности.
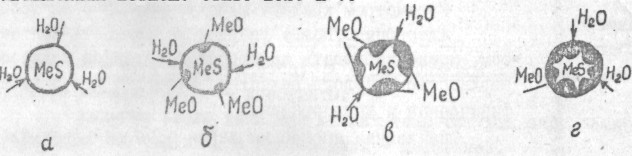
При контакте газа с поверхностью твердого реагента твердый продукт реакции отсутствует, и скорость реакции мала (индукционный период) (рис. 3.2, а ).
Рис. 3.2. Схема роста зародышей оксидов на сульфиде металла при воздействии водяного пара
Затем образуются ядра (зародыш) фазы твердого продукта, т. е. совокупность частиц твердого продукта, содержащая элементы собственной кристаллической структуры, отличной от структуры исходного твердого тела. С появлением ядер (рис. 3.2,б) возникает и поверхность раздела фаз. Наблюдаемая скорость реакции увеличивается, что обусловлено как возникновением новых ядер, так и (главным образом) их ростом, при котором резко возрастает и поверхность раздела твердых фаз (рис. 3.2. в). Эта поверхность раздела фаз возрастает до тех пор, пока растущие ядра не начинают касаться друг друга; перекрываться и т. д.
Именно в этот момент скорость реакции (а не степень превращения) проходит через максимум, что графически иллюстрируется экстремумом на зависимости W - б. Завершаются процессы образованием cплошного слоя твердого продукта (рис. 3.2,г). Поверхность раздела фаз уменьшается, и наблюдаемая скорость реакции падает; именно на этом участке появляется дополнительная медленная стадия диффузии реагирующего газа (например, пара) через слой твердого продукта.
Ход топохимических реакций, в которых продукты реакции не появляются равномерно по всей поверхности образца, т. е. ядра (зародыш) образуются на отдельных участках (см. рис. 3.2, б, в), описывается сигмовидными кривыми (см. рис. 3.1, а). Однако протекание ряда реакций может определяться только химической стадией или диффузией, т. е. не лимитироваться стадией зародышеобразования. Такие реакции описываются простой (а не сигмовидной) кинетической кривой (рис. 3.3, а, б) с постоянно уменьшающейся скоростью.
а - интегральная; б - дифференциальная; Т1 > Т12
Рис. 3.3. Кинетические кривые топохимических реакций, не лимитируемых зародышеобразованием
Когда ход реакции определяется продвижением поверхности раздела фаз, т. е. стадия зародышеобразования не является лимитирующей, а зависит только он кинетики процесса, начальная стадия (зародышеобразование или образование, поверхности раздела фаз) протекает очень быстро по сравнению с полный временем превращения.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |




