Исходя из теплоты образования воды и теплового эффекта реакции 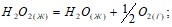
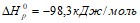
вычислите теплоту образования 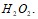
Вычислите 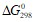 реакции, протекающей по уравнению, используя значения стандартных теплот образования и абсолютных стандартных энтропий веществ:
реакции, протекающей по уравнению, используя значения стандартных теплот образования и абсолютных стандартных энтропий веществ: 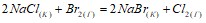 . Реакция между оксидом азота (РР) и хлором протекает по уравнению 2NO + Cl2 ↔ 2NOCl. Как изменится скорость реакции при увеличении: а) концентрации оксида азота в 2 раза; б) концентрации хлора в 2 раза; в) концентрации обоих веществ в 2 раза? Константа равновесия для реакции
. Реакция между оксидом азота (РР) и хлором протекает по уравнению 2NO + Cl2 ↔ 2NOCl. Как изменится скорость реакции при увеличении: а) концентрации оксида азота в 2 раза; б) концентрации хлора в 2 раза; в) концентрации обоих веществ в 2 раза? Константа равновесия для реакции 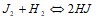 равна 36, а начальные концентрации водорода и иода равны по 0,02 моль/л. Вычислить равновесные концентрации водорода, иода и иодоводорода. В растворе объемом 1,5 л содержится карбонат натрия массой 12,5 г. Чему равна молярная концентрация эквивалента этого раствора? Составьте молекулярные уравнения реакций, представленных следующими ионными уравнениями:
равна 36, а начальные концентрации водорода и иода равны по 0,02 моль/л. Вычислить равновесные концентрации водорода, иода и иодоводорода. В растворе объемом 1,5 л содержится карбонат натрия массой 12,5 г. Чему равна молярная концентрация эквивалента этого раствора? Составьте молекулярные уравнения реакций, представленных следующими ионными уравнениями: 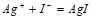 ;
; 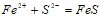 Вычислите температуру кипения раствора, содержащего 120 г сахара
Вычислите температуру кипения раствора, содержащего 120 г сахара 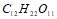 в 650 г воды. Эбуллископическая константа воды равна 0,520. Вычислите константу диссоциации уксусной кислоты
в 650 г воды. Эбуллископическая константа воды равна 0,520. Вычислите константу диссоциации уксусной кислоты 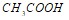 , если степень диссоциации ее в 0,25 М растворе равна 2,51 %. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
, если степень диссоциации ее в 0,25 М растворе равна 2,51 %. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 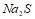 и
и 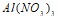 . Укажите рН среды.
. Укажите рН среды.
Вариант 6.
Определите тепловые эффекты процессов, протекающих по уравнениям: 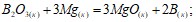
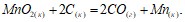 Исходя из значений стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ, вычислите
Исходя из значений стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ, вычислите 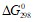 реакции, протекающей по уравнению
реакции, протекающей по уравнению 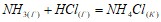 . Возможен ли этот процесс при стандартных условиях? Во сколько раз увеличится константа скорости химической реакции при повышении температуры на 40°, если г=3,2? Исходные концентрации
. Возможен ли этот процесс при стандартных условиях? Во сколько раз увеличится константа скорости химической реакции при повышении температуры на 40°, если г=3,2? Исходные концентрации 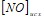 и
и 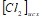 в гомогенной системе
в гомогенной системе 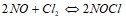 составляют соответственно 0,5 и 0,2 моль/л. Вычислите константу равновесия, если к моменту наступления равновесия прореагировало 15 % NO. Вычислите молярную концентрацию иодида калия, 1 л которого содержит 0,0025 г KI. Составьте молекулярные и ионные уравнения реакций, протекающих при смешивании растворов: а)
составляют соответственно 0,5 и 0,2 моль/л. Вычислите константу равновесия, если к моменту наступления равновесия прореагировало 15 % NO. Вычислите молярную концентрацию иодида калия, 1 л которого содержит 0,0025 г KI. Составьте молекулярные и ионные уравнения реакций, протекающих при смешивании растворов: а)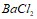 и
и 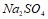 ; б)
; б) 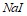 и
и 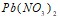 ; в)
; в) 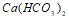 и
и 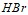 . Давление пара воды при 25єС составляет 3167 Па. Вычислите для той же температуры давление пара раствора, в 375 г которого содержится 85 г глюкозы. Составьте уравнения электролитической диссоциации следующих электролитов:
. Давление пара воды при 25єС составляет 3167 Па. Вычислите для той же температуры давление пара раствора, в 375 г которого содержится 85 г глюкозы. Составьте уравнения электролитической диссоциации следующих электролитов: 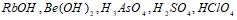 . Запишите выражения констант равновесия для слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
. Запишите выражения констант равновесия для слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 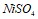 и
и 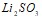 . Укажите рН среды.
. Укажите рН среды.
Вариант 7.
Теплоты растворения 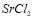 и
и 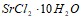 составляют соответственно – 47,7 и 31,0 кДж/моль. Вычислите изменение энтальпии реакции:
составляют соответственно – 47,7 и 31,0 кДж/моль. Вычислите изменение энтальпии реакции: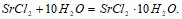 Не прибегая к расчетам, установите знак энтропии следующих реакций:
Не прибегая к расчетам, установите знак энтропии следующих реакций: 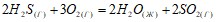 ;
; 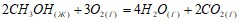 ;
;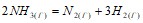 ;
;
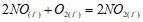
На сколько градусов следует повысить температуру системы, чтобы скорость протекающей в ней реакции возросла в 30 раз (г=2,5)? Почему при изменении давления смещается равновесие системы 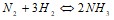 и не смещается равновесие системы
и не смещается равновесие системы 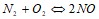 ? Мотивируйте ответ, используя расчет скоростей прямой и обратной реакций до и после изменения давления. Составьте уравнения для констант равновесия обеих систем. 0.6 л раствора гидроксида калия содержит 16.8 г KOH. Чему равна молярная концентрация этого раствора? Напишите ионно-молекулярные уравнения реакций:
? Мотивируйте ответ, используя расчет скоростей прямой и обратной реакций до и после изменения давления. Составьте уравнения для констант равновесия обеих систем. 0.6 л раствора гидроксида калия содержит 16.8 г KOH. Чему равна молярная концентрация этого раствора? Напишите ионно-молекулярные уравнения реакций: 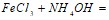 ;
; 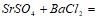 ;
; 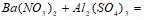 .
.
Сколько граммов глюкозы 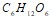 следует растворить в 300 г воды для получения раствора, температура кипения которого превышает температуру кипения чистого растворителя на 0,06єС? Эбуллиоскопическая константа воды равна 0,52 0. Составьте уравнения электролитической диссоциации электролитов
следует растворить в 300 г воды для получения раствора, температура кипения которого превышает температуру кипения чистого растворителя на 0,06єС? Эбуллиоскопическая константа воды равна 0,52 0. Составьте уравнения электролитической диссоциации электролитов 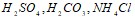 . Объясните, какой из них легче распадается на ионы и почему. Запишите выражение для константы равновесия слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
. Объясните, какой из них легче распадается на ионы и почему. Запишите выражение для константы равновесия слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 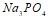 и
и 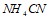 . Укажите рН среды.
. Укажите рН среды.
Вариант 8.
Вычислите изменение энтальпии следующих процессов: 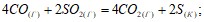
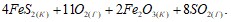 Как изменяется энтропия при фазовых переходах: а) алмаза в графит; б) воды в пар; в) воды в лед? Почему? Вычислите энтропию каждого превращения. При повышении температуры на 50° скорость реакции возросла в 1200 раз. Вычислите г. Равновесие в гомогенной системе
Как изменяется энтропия при фазовых переходах: а) алмаза в графит; б) воды в пар; в) воды в лед? Почему? Вычислите энтропию каждого превращения. При повышении температуры на 50° скорость реакции возросла в 1200 раз. Вычислите г. Равновесие в гомогенной системе 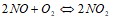 установилось при следующих концентрациях реагирующих веществ
установилось при следующих концентрациях реагирующих веществ 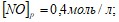
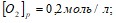
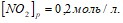 . Вычислите константу равновесия и исходную концентрацию оксида азота и кислорода. Вычислите молярную концентрацию K2SO4, в 0.02 л которого содержится 2,74 г растворенного вещества. Составьте молекулярные уравнения по ионно-молекулярным:
. Вычислите константу равновесия и исходную концентрацию оксида азота и кислорода. Вычислите молярную концентрацию K2SO4, в 0.02 л которого содержится 2,74 г растворенного вещества. Составьте молекулярные уравнения по ионно-молекулярным: 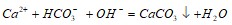 ;
; 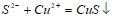 Вычислите осмотическое давление при 29єС раствора сахара
Вычислите осмотическое давление при 29єС раствора сахара 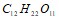 , 1 л которого содержит 85 мг растворенного вещества. Составьте уравнения электролитической диссоциации следующих электролитов:
, 1 л которого содержит 85 мг растворенного вещества. Составьте уравнения электролитической диссоциации следующих электролитов: 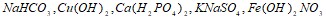 . Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 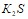 и
и 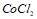 . Укажите рН среды.
. Укажите рН среды.
Вариант 9.
Теплота сгорания метана равна – 890 кДж/моль. Вычислите теплоту его образования. Вычислите 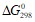 реакции, протекающей по уравнению, используя значения стандартных теплот образования и абсолютных стандартных энтропий веществ:
реакции, протекающей по уравнению, используя значения стандартных теплот образования и абсолютных стандартных энтропий веществ: 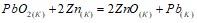 . Вычислите г реакции, если константа скорости ее при 120°С равна 6,7•10-2. Константа равновесия гомогенной системы
. Вычислите г реакции, если константа скорости ее при 120°С равна 6,7•10-2. Константа равновесия гомогенной системы 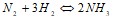 при некоторой температуре равна 0,2. Равновесные концентрации водорода и аммиака соответственно равны 0,4 и 0,15
при некоторой температуре равна 0,2. Равновесные концентрации водорода и аммиака соответственно равны 0,4 и 0,15 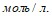 Вычислите исходную и равновесную концентрации азота. Сколько граммов растворенного вещества и сколько граммов воды содержится в 350г 9%-ного раствора
Вычислите исходную и равновесную концентрации азота. Сколько граммов растворенного вещества и сколько граммов воды содержится в 350г 9%-ного раствора 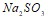 ? Составьте молекулярные уравнения реакций, представленных следующими ионными уравнениями:
? Составьте молекулярные уравнения реакций, представленных следующими ионными уравнениями: 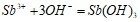 ;
; 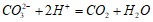 . Вычислите массовую долю сахара
. Вычислите массовую долю сахара 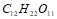 в растворе, температура кипения которого 100,24єС. Эбуллиоскопическая константа воды равна 0,52 0. Составьте уравнения электролитической диссоциации для электролитов: серной кислоты, ортомышьяковой кислоты, азотистой кислоты, кремнистой кислоты. Запишите выражения для констант диссоциации слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
в растворе, температура кипения которого 100,24єС. Эбуллиоскопическая константа воды равна 0,52 0. Составьте уравнения электролитической диссоциации для электролитов: серной кислоты, ортомышьяковой кислоты, азотистой кислоты, кремнистой кислоты. Запишите выражения для констант диссоциации слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 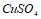 и
и 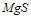 . Укажите рН среды.
. Укажите рН среды.
Вариант 10.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6
|
![]()
![]() ;
;![]() ;
;![]()
![]() ;
; ![]() ;
; ![]() .
.



