Федеральное агентство по образованию
ГОУ ВПО Тюменский архитектурно-строительный университет
Кафедра общей и специальной химии

МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к контрольной работе № 1
по курсу
«ХИМИЯ»
для студентов инженерных специальностей 1 курса
Тюмень 2007
Методические указания к контрольной работе №1 по курсу «Химия» для студентов всех специальностей 1 курса: , дневное отделение – 1 курс, 1 семестр, Тюмень: ТюмГАСУ, 2007 год, 35 с.
Рецензент: к. х.н., доцент
(степень, звание, Фамилия, Имя, Отчество)
Учебно-методический материал утвержден на заседании кафедры :
Протокол №_______ от «_____» ________________2007 г.
Учебно-методический материал утвержден на УМС университета:
Протокол №________от «_____»________________2007 г.
Тираж 200 экземпляров
ВВЕДЕНИЕ
Предлагаемое методическое указание разработано для студентов дневного отделения инженерных специальностей университета и соответствует учебной программе по курсу «Общая химия». Руководство содержит 27 вариантов заданий, предназначенных для самостоятельного выполнения с целью закрепления полученного теоретического материала по следующим темам:
«Термодинамика химических процессов»,
«Кинетика и химическое равновесие»,
«Свойства растворов и расчет концентраций»,
«Электролитическая диссоциация»,
«Гидролиз солей».
Для удобства решения задач по теме «Термодинамика химических процессов» в методических указаниях приведено приложение «Термодинамические свойства некоторых соединений».
ВАРИАНТЫ КОНТРОЛЬНЫХ ЗАДАНИЙ
Вариант 1
Рассчитайте тепловой эффект реакции окисления оксида мышьяка озоном, протекающей по уравнению: 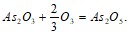 Дайте мотивированный ответ на вопрос, в каком состоянии при одной и той же температуре энтропия вещества больше: в газообразном или кристаллическом? Напишите выражение для скорости химической реакции, протекающей в гомогенной системе по уравнению
Дайте мотивированный ответ на вопрос, в каком состоянии при одной и той же температуре энтропия вещества больше: в газообразном или кристаллическом? Напишите выражение для скорости химической реакции, протекающей в гомогенной системе по уравнению 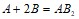 и определите, во сколько раз увеличится скорость этой реакции, если: а) концентрация вещества А увеличится в 2 раза; б) концентрация вещества В увеличится в 2 раза; в) концентрация обоих веществ увеличится в 2 раза. Напишите выражение для константы равновесия следующих обратимых процессов: а)
и определите, во сколько раз увеличится скорость этой реакции, если: а) концентрация вещества А увеличится в 2 раза; б) концентрация вещества В увеличится в 2 раза; в) концентрация обоих веществ увеличится в 2 раза. Напишите выражение для константы равновесия следующих обратимых процессов: а) 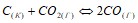
б) 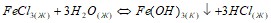 .
.
Какой объем 8%-ного раствора соли плотностью 1,15 г/см3 надо прибавить к ее 3%-ному раствору плотностью 1,08 г/см3 объемом 1 л, чтобы получить 5%-ный раствор карбоната натрия? Составьте молекулярные и ионные уравнения реакций, протекающих при смешивании растворов: а)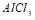 и
и 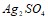 ; б)
; б) 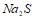 и
и 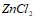 ; в)
; в) 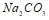 и
и 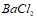 . Вычислите осмотическое давление раствора при 25єС, в 1,5 л которого содержится 22,5 мг сахара
. Вычислите осмотическое давление раствора при 25єС, в 1,5 л которого содержится 22,5 мг сахара 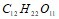 (М=342). Составьте уравнения электролитической диссоциации следующих электролитов:
(М=342). Составьте уравнения электролитической диссоциации следующих электролитов: 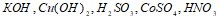 . Запишите выражения констант равновесия для слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
. Запишите выражения констант равновесия для слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 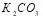 и
и 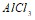 . Укажите рН среды.
. Укажите рН среды.
Вариант 2
Вычислите тепловой эффект реакции взаимодействия металлического натрия с водой. Вычислите 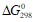 реакции, протекающей по уравнению, используя значения стандартных теплот образования и абсолютных стандартных энтропий веществ:
реакции, протекающей по уравнению, используя значения стандартных теплот образования и абсолютных стандартных энтропий веществ: 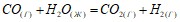 . Во сколько раз следует увеличить концентрацию оксида углерода (РР) в системе 2СО = СО2 + С, чтобы скорость реакции увеличилась в 4 раза? При синтезе аммиака равновесие установилось при следующих равновесных концентрациях веществ: [N2]=2.5, [H2]=1.8, [NH3]=3.6 моль/л. Рассчитайте значение константы равновесия и исходные концентрации. Какой объем 0,6 н. раствора нужно прибавить к 750 мл 0,2н. раствора, чтобы получить 0,3н. раствор? Напишите ионно-молекулярные уравнения реакций:
. Во сколько раз следует увеличить концентрацию оксида углерода (РР) в системе 2СО = СО2 + С, чтобы скорость реакции увеличилась в 4 раза? При синтезе аммиака равновесие установилось при следующих равновесных концентрациях веществ: [N2]=2.5, [H2]=1.8, [NH3]=3.6 моль/л. Рассчитайте значение константы равновесия и исходные концентрации. Какой объем 0,6 н. раствора нужно прибавить к 750 мл 0,2н. раствора, чтобы получить 0,3н. раствор? Напишите ионно-молекулярные уравнения реакций: 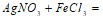 ;
; 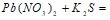 ;
; 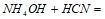 .
.
Вычислите давление пара воды над 10%-ным раствором сахара 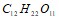 при 100єС. Вычислите концентрацию анионов
при 100єС. Вычислите концентрацию анионов 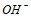 , если концентрация катионов водорода (моль/л) составляет: а) 2·10-9; б) 1·10-5; в) 0,5·10-6; г) 3,5·10-3. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
, если концентрация катионов водорода (моль/л) составляет: а) 2·10-9; б) 1·10-5; в) 0,5·10-6; г) 3,5·10-3. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 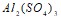 и
и 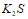 . Укажите рН среды.
. Укажите рН среды.
Вариант 3.
Определите стандартное изменение энтальпии реакции горения этана 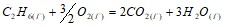 ,
,
используя табличные значения энтальпий образования исходных веществ и продуктов реакции.
Вычислите 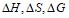 реакции восстановления
реакции восстановления 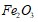 углеродом:
углеродом: 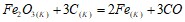 при стандартных условиях. Возможна ли эта реакция при 800 К? Во сколько раз следует увеличить давление, чтобы скорость образования NO2 по реакции 2NO +O2 ↔ 2NO2, возросла в 1000 раз? Как повлияет повышение давления и температуры на равновесие следующих обратимых реакций:
при стандартных условиях. Возможна ли эта реакция при 800 К? Во сколько раз следует увеличить давление, чтобы скорость образования NO2 по реакции 2NO +O2 ↔ 2NO2, возросла в 1000 раз? Как повлияет повышение давления и температуры на равновесие следующих обратимых реакций: а) 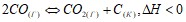 ; б)
; б) 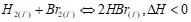
в) 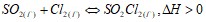
В какой массе воды следует растворить 50 мг хлорида калия для получения раствора, в котором массовая доля KCl равна 7,5 %? Составьте молекулярные уравнения по ионно-молекулярным: 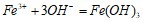 ;
; 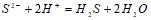 Вычислите температуру кипения 5%-ного раствора сахара
Вычислите температуру кипения 5%-ного раствора сахара 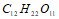 в воде. Эбуллиоскопическая константа воды равна 0,52 0. Составьте уравнения электролитической диссоциации электролитов
в воде. Эбуллиоскопическая константа воды равна 0,52 0. Составьте уравнения электролитической диссоциации электролитов 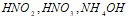 . Объясните, какой из них легче распадается на ионы и почему. Запишите выражение для константы равновесия слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
. Объясните, какой из них легче распадается на ионы и почему. Запишите выражение для константы равновесия слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 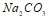 и
и 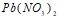 . Укажите рН среды.
. Укажите рН среды.
Вариант 4.
Вычислите изменение энтальпии следующих процессов: 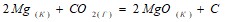 ;
; 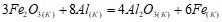 .
.
Реакция горения ацетилена идет по уравнению: 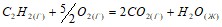 . Вычислите
. Вычислите 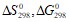 , объясните уменьшение энтропии в результате этой реакции. Напишите выражение для скорости реакции С(К) + О2(Г) =СО2(Г) и определите, во сколько раз увеличится ее скорость при увеличении концентрации кислорода в 3 раза. Используя справочные данные (Приложение «Термодинамические свойства некоторых соединений»), определите, в какую сторону произойдет смещение равновесия гомогенной реакции:
, объясните уменьшение энтропии в результате этой реакции. Напишите выражение для скорости реакции С(К) + О2(Г) =СО2(Г) и определите, во сколько раз увеличится ее скорость при увеличении концентрации кислорода в 3 раза. Используя справочные данные (Приложение «Термодинамические свойства некоторых соединений»), определите, в какую сторону произойдет смещение равновесия гомогенной реакции: 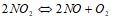 при следующих воздействиях: а) охлаждение системы; б) увеличение давления. Какая масса HCl содержится в 0,25 л раствора соляной кислоты с массовой долей 10,52% (плотность раствора равна 1,050 г/см3)? Выразите ионными и молекулярными уравнениями следующие процессы: а) растворение гидроксида цинка в серной кислоте; б) действие щелочи на раствор сульфата меди. В 250 мл раствора содержится 17 мг растворенного вещества. Осмотическое давление раствора при 27єС равно 1,84 кПа. Вычислите молекулярную массу вещества. Составьте уравнения электролитической диссоциации для слабых электролитов: угольной кислоты, ортофосфорной кислоты, сернистой кислоты, уксусной кислоты. Запишите выражения для констант равновесия первых ступеней диссоциации. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
при следующих воздействиях: а) охлаждение системы; б) увеличение давления. Какая масса HCl содержится в 0,25 л раствора соляной кислоты с массовой долей 10,52% (плотность раствора равна 1,050 г/см3)? Выразите ионными и молекулярными уравнениями следующие процессы: а) растворение гидроксида цинка в серной кислоте; б) действие щелочи на раствор сульфата меди. В 250 мл раствора содержится 17 мг растворенного вещества. Осмотическое давление раствора при 27єС равно 1,84 кПа. Вычислите молекулярную массу вещества. Составьте уравнения электролитической диссоциации для слабых электролитов: угольной кислоты, ортофосфорной кислоты, сернистой кислоты, уксусной кислоты. Запишите выражения для констант равновесия первых ступеней диссоциации. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 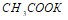 и
и 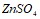 . Укажите рН среды.
. Укажите рН среды.
Вариант 5.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6
|

![]() .
.![]() ;
; ![]() ;
; ![]() .
.![]() ,
,![]() ; б)
; б) ![]()
![]()
![]() ;
; ![]() .
.



