Сколько теплоты выделится при сжигании 45 г сероуглерода? Процесс горения сероуглерода идет по уравнению: 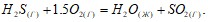 Вычислите
Вычислите 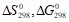 , объясните уменьшение энтропии в ходе этой реакции. Реакция между веществами А и В выражается уравнением А + 2В =С. Начальные концентрации соответственно равны 0,3 и 0,5 моль/л. Константа скорости равна 0,4 л2/(моль2 ·с). Вычислите скорость реакции в начальный момент и в тот момент, когда концентрация вещества А уменьшилась на 0,1 моль/л. Константа равновесия системы при постоянной температуре
, объясните уменьшение энтропии в ходе этой реакции. Реакция между веществами А и В выражается уравнением А + 2В =С. Начальные концентрации соответственно равны 0,3 и 0,5 моль/л. Константа скорости равна 0,4 л2/(моль2 ·с). Вычислите скорость реакции в начальный момент и в тот момент, когда концентрация вещества А уменьшилась на 0,1 моль/л. Константа равновесия системы при постоянной температуре 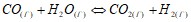 равна 1. Вычислите равновесные концентрации всех реагентов, если исходные концентрации составляют:
равна 1. Вычислите равновесные концентрации всех реагентов, если исходные концентрации составляют: 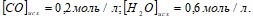 Вычислите массовую долю растворенных веществ в растворах, содержащих: а) 75 г
Вычислите массовую долю растворенных веществ в растворах, содержащих: а) 75 г 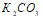 в 350 г воды; б) 40 г
в 350 г воды; б) 40 г 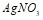 в 600 г воды. Напишите ионно-молекулярные уравнения реакций:
в 600 г воды. Напишите ионно-молекулярные уравнения реакций: 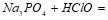 ;
; 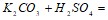 ;
; 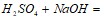 .
.
В каком количестве воды следует растворить 19 г глицерина 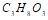 , чтобы получить раствор с температурой кипения 100,099єС? Эбуллиоскопическая константа воды равна 0,52 0. Константа диссоциации одноосновной кислоты равна 1,5·10-5. Определите степень ее диссоциации в 0,003 М растворе. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
, чтобы получить раствор с температурой кипения 100,099єС? Эбуллиоскопическая константа воды равна 0,52 0. Константа диссоциации одноосновной кислоты равна 1,5·10-5. Определите степень ее диссоциации в 0,003 М растворе. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 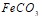 и
и 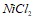 . Укажите рН среды.
. Укажите рН среды.
Вариант 11.
Вычислите тепловой эффект реакции гашения 15 кг извести. Процесс протекает по уравнению 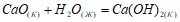 . Исходя из значений стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ, вычислите
. Исходя из значений стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ, вычислите 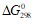 реакции, протекающей по уравнению
реакции, протекающей по уравнению 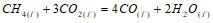 . Возможен ли этот процесс в стандартных условиях? Если температурный коэффициент реакции равен 3, то во сколько раз увеличится скорость реакции при увеличении температуры с 22 до 62°С? Равновесие системы
. Возможен ли этот процесс в стандартных условиях? Если температурный коэффициент реакции равен 3, то во сколько раз увеличится скорость реакции при увеличении температуры с 22 до 62°С? Равновесие системы 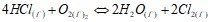 при постоянной температуре установилось при следующих концентрациях:
при постоянной температуре установилось при следующих концентрациях: 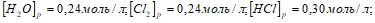
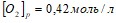 . Вычислите исходные концентрации хлороводорода и кислорода. Какой объем 25%-ного раствора плотностью 1,15 г/см3 надо прибавить к ее 12%-ному раствору плотностью 1,05 г/см3 объемом 1 л, чтобы получить 14%-ный раствор карбоната натрия? Закончите молекулярные и составьте ионно-молекулярные уравнения процессов, проходящих по схемам:
. Вычислите исходные концентрации хлороводорода и кислорода. Какой объем 25%-ного раствора плотностью 1,15 г/см3 надо прибавить к ее 12%-ному раствору плотностью 1,05 г/см3 объемом 1 л, чтобы получить 14%-ный раствор карбоната натрия? Закончите молекулярные и составьте ионно-молекулярные уравнения процессов, проходящих по схемам: 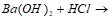 …;
…; 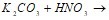 …. Чему равно при температуре 8єС осмотическое давление раствора, в 1,6 л которого содержится 256 мг глицерина
…. Чему равно при температуре 8єС осмотическое давление раствора, в 1,6 л которого содержится 256 мг глицерина 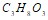 ? Приведите по три примера сильных и слабых электролитов, составьте уравнения их диссоциации. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
? Приведите по три примера сильных и слабых электролитов, составьте уравнения их диссоциации. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 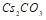 и
и 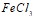 . Укажите рН среды.
. Укажите рН среды.
Вариант 12.
Вычислите величину изменения энтальпии реакций: 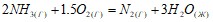 ;
; 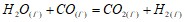 . Прямая или обратная реакция будет протекать при стандартных условиях в системе
. Прямая или обратная реакция будет протекать при стандартных условиях в системе 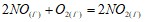 . Ответ мотивируйте, вычислив
. Ответ мотивируйте, вычислив 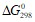 прямой реакции. Напишите математические выражения для определения скоростей следующих химических реакций, протекающих в гомогенных системах: a) CO + Cl2 → COCl2; б) 2NO + O2 → 2NO2;
прямой реакции. Напишите математические выражения для определения скоростей следующих химических реакций, протекающих в гомогенных системах: a) CO + Cl2 → COCl2; б) 2NO + O2 → 2NO2; в) 4HCl + O2 → 2H2O + 2Cl2.
Напишите выражение для константы равновесия гетерогенной системы 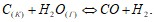 Как следует изменить давление и концентрацию веществ, чтобы сместить равновесие в сторону прямой реакции? Какой объем раствора серной кислоты с массовой долей
Как следует изменить давление и концентрацию веществ, чтобы сместить равновесие в сторону прямой реакции? Какой объем раствора серной кислоты с массовой долей 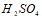 15% (с=1.219 г/см3) можно приготовить из 4 кг раствора серной кислоты с массовой долей
15% (с=1.219 г/см3) можно приготовить из 4 кг раствора серной кислоты с массовой долей 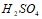 65%? Составьте молекулярные уравнения по ионно-молекулярным:
65%? Составьте молекулярные уравнения по ионно-молекулярным: 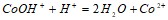 ;
; 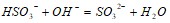 Вычислите осмотическое давление 0,035 М раствора сахара
Вычислите осмотическое давление 0,035 М раствора сахара 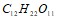 при 35єС. Составьте уравнения электролитической диссоциации следующих электролитов:
при 35єС. Составьте уравнения электролитической диссоциации следующих электролитов: 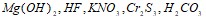 . Запишите выражения констант равновесия для слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
. Запишите выражения констант равновесия для слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 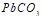 и
и 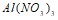 . Укажите рН среды.
. Укажите рН среды.
Вариант 13.
Теплота растворения безводного сульфата меди составляет 66,1 кДж/моль, а теплота перевода его в пятиводный гидрат 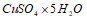 равна –78,8 КдЖ/моль. Вычислите теплоту растворения
равна –78,8 КдЖ/моль. Вычислите теплоту растворения 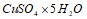 . Вычислите
. Вычислите 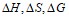 реакции восстановления
реакции восстановления 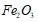 углеродом:
углеродом: 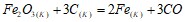 при стандартных условиях. Возможна ли эта реакция при 300 К? Напишите математические выражения для определения скоростей следующих химических реакций, протекающих в гетерогенных системах: а) С(к) + O2(Г) → СO2 (Г); б) СO2(Г) + С(К) → 2СО(Г); в) СаО(К) + СO2 (Г) → СаСО3(Г). Объясните особенность составления формул в гетерогенной системе. Составьте выражение для константы равновесия гетерогенной системы
при стандартных условиях. Возможна ли эта реакция при 300 К? Напишите математические выражения для определения скоростей следующих химических реакций, протекающих в гетерогенных системах: а) С(к) + O2(Г) → СO2 (Г); б) СO2(Г) + С(К) → 2СО(Г); в) СаО(К) + СO2 (Г) → СаСО3(Г). Объясните особенность составления формул в гетерогенной системе. Составьте выражение для константы равновесия гетерогенной системы 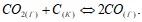 Что необходимо предпринять для повышения выхода оксида углерода? Как изменится скорость прямой реакции, если концентрацию диоксида углерода увеличить в 3 раза? 10 мл 25%-ного раствора содержит 0,458 г растворенного вещества. Какова плотность этого раствора? Составьте молекулярные и ионно-молекулярные уравнения реакций, которые возможны при попарном взаимодействии растворов следующих солей:
Что необходимо предпринять для повышения выхода оксида углерода? Как изменится скорость прямой реакции, если концентрацию диоксида углерода увеличить в 3 раза? 10 мл 25%-ного раствора содержит 0,458 г растворенного вещества. Какова плотность этого раствора? Составьте молекулярные и ионно-молекулярные уравнения реакций, которые возможны при попарном взаимодействии растворов следующих солей: 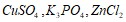 . Температура кипения ацетона 56,1єС, а его эбуллиоскопическая константа равна 1,73є. Вычислите температуру кипения 8%-ного раствора глицерина
. Температура кипения ацетона 56,1єС, а его эбуллиоскопическая константа равна 1,73є. Вычислите температуру кипения 8%-ного раствора глицерина 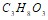 в ацетоне. Составьте уравнения электролитической диссоциации электролитов
в ацетоне. Составьте уравнения электролитической диссоциации электролитов 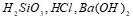 . Объясните, какой из них легче распадается на ионы и почему. Запишите выражение для константы равновесия слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей:
. Объясните, какой из них легче распадается на ионы и почему. Запишите выражение для константы равновесия слабых электролитов. Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: 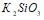 и
и 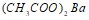 . Укажите рН среды.
. Укажите рН среды.
Вариант 14.
Определите тепловой эффект следующих химических реакций: 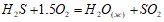 ;
; 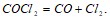 Исходя из значений стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ, вычислите
Исходя из значений стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ, вычислите 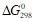 реакции, протекающей по уравнению
реакции, протекающей по уравнению 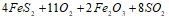
 . Определите, как изменится скорость прямой реакции
. Определите, как изменится скорость прямой реакции 2SO2(Г) + O2(Г) ↔ 2 SO3(Г), если давление в системе увеличить в 5 раз?

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6
|
![]() ;
; ![]() ;
; ![]() .
.



