![]()
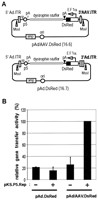
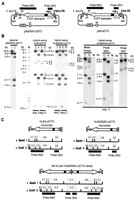
Структура репликационных форм двойного hcAd/AAV гибридного вектора. В следующем наборе экспериментов мы исследовали структурную организацию репликационной гибридной векторной ДНК. С этой целью мы построили pAd/AAV. eDYS. У этой плазмиды есть точно то же самое устройство Ad и AAV cis-активные элементы такие, как pAd/AAV. DsRed. Однако, вместо того, чтобы управлять транскрипцией DsRed, генный промотор EF1б ведет экспрессию рекомбинантного генетического кода продуктом слияния EGFP и человеческого дистрофина во всю длину (Рис. 2A). Конструкция pAd/AAV. eDYS была получена из pAd. eDYS (Рис. 2A), кодируя обычный hcAd векторный геном, заменяя 3 ′ Ad - специфичными сегментами с AAV ITR. Следовательно, EGFP-дистрофин кодирующие hcAd и hcAd/AAV геномы отличаются друг от друга только в их 3 ′ окончаниях. Накопление EGFP-дистрофин кодирующей hc векторной ДНК было начато трансфекцией MssI-переваренный pAd/AAV. eDYS или MssI-перевареной pAd. eDYS в PERtTA. Cre76 клетках. Продуцирующие клетки были впоследствии заражены Ad. floxedШ. После развития CPE, клеточные культуры были собраны и заново посеяны PER tTA. Cre76 клетки с одной десятой каждого очищенного лизата. Функции Ad помощника были снова обеспечены Ad. floxedШ. Отрицательный контроль состоял из свежее посеянных PER tTA. Cre76 клеток, зараженные одним только Ad. floxedШ. После того, как инкубационный период 48 час прошел, ДНК была извлечена из клеток, переварил с BamHI или EcoRV и подвергнута саусен блот анализу (Рис. 2A) . Плазмида pAd/AAV. eDYS переваренная с теми же самыми ферментами обеспечила шаблоны для надежного управления гибридизаций ДНК. Переваривание с BamHI произвело фрагменты 0.7, 8.6, и 10.6 КБ (Рис. 2B, переулок 1), тогда как с EcoRV выдавало продукты 1.9, 2.4, 6.9, и 8.6 КБ (Рис. 2B, переулок 2) после инкубации со смесью обоих проб. И BamHI-и EcoRV-леченная экстрахромосомальная ДНК от PER. tTA. Cre76 клеток, зараженных одним только Ad floxedШ, не производили сигнала гибридизации, подтверждающего специфичность обоих проб (не показанно). Используя ту же самую комбинацию проб, экстрахромосомальной ДНК из двух независимых экспериментов и распространения начался с MssI-леченных pAd. eDYS продуктов 0.7, 2.7, 4.5, и 8.6 КБ когда переварено с BamHI (Рис. 2B, 3 и 5) и 1.9, 2.4, 4.8, и 6.9 КБ после переваривания с EcoRV (Рис. 2B, 4 и 6). Эти результаты показывают превосходство репликационных форм векторной ДНК после одного раунда распространения hcAd. eDYS частиц в разрешающих клетках. При тех же самых условиях саусен блот анализ экстрахромосомальной ДНК из трех независимых экспериментов освобождение/сборки и распространения с MssI-переваренным pAd/AAV. eDYS, использующим пробу 2832 один или вместе с иробой 6563, показали наличие дополнительного фрагмента EcoRV 9.0 КБ (Рис. 2B, переулки 8, 10, 12, и 16). Эти особые разновидности ДНК соответствуют репликационным формам ДНК с тандемной организацией от хвоста к хвосту (Рис. 2C). Лечение экстрахромосомальной ДНК с BamHI произвело внутренние сегменты кодирующие дистрофин на 8.6 КБ, которые не достаточно от ожидаемых определили димер - фрагменты ДНК на 8.4 КБ (Рис. 2B, переулки 7, 9, и 11). Мы подтвердили наличие определенных димер фрагментов на 8.4 КБ при использовании пробу 2832 один (Рис. 2B, переулок 15), тогда как как ожидалось внутренние определенные ДНК – специфические сегменты дистрофина на 8.6 КБ были обнаружены пробой 6563 (Рис. 2B, переулок 13). Интересно, хотя менее видный чем те, которые соответствуют hcAd. eDYS мономерные репликационные формы, фрагменты ДНК, совместимые с гибридными мономерами Ad/AAV. eDYS (Рис. 2C), были также обнаружены (Рис. 2B,). Эта интерпретация далее подтверждена обнаружением 4.2 и 4.5 КБ сегментов после того, как гибридизации с 3 ′-концом специфической пробы 2832, но не с пробой 6563 (Рис. 2B, сравнивают).
Чтобы определить, способствует ли межмолекулярная рекомбинация через AAV ITRs поколение структур ДНК от хвоста к хвосту PER. tTA. Cre76 клетки, были инфицированы вирусом с равным количеством pAd/AAV. DsRed и pAd/AAV. EGFP (Рис. 3A). Эксперименты контроля были выполнены с эквимолярными смесями DsRed и EGFP (Рис. 3A,). Все конструкции были переварены с MssI до трансфекции. Прямая флюоресцентная микроскопия через 20 часов после трансфекции показала, что значительное количество клеток PER. tTA. Cre было позитивно из-за наличия маркера, демонстрирующих одновременное наличие DsRed-и EGFP-кодирующей плазмиды в пределах этих клеток (Рис. 3B). После инфекции с Ad floxedШ и развитием CPE, были собраны клеточные культуры, и к Рисунок 2 одной десятой очищенных лизатов была добавлена Ad. floxedШ к свежее посеянным PER. tTA. Cre76 клеткам. Один день спустя слои клеток были проверены на DsRed-и EGFP-маркеры прямой флюоресцентной микроскопией (Рис. 3C). Как показано выше, при тех же самых экспериментальных условиях, мы наблюдали димеры от хвоста к хвосту при использовании hcAd/AAV гибридных векторных плазмид кодирования ДНК (Рис. 2B, 8, 10, 12, 15, и 16), тогда как в экспериментах контрольной группы с обычными hcAd векторными конструкциями мономеры были единственной обнаруженной структурой (Рис. 2B, 4 и 6). Следовательно, трансфекция PER. tTA. Cre76 клеток со смесью MssI-переваренной. pAd DsRed и pAd EGFP в присутствии Ad floxedШ, как ожидают, не породит hcAd частицы, которые могут передать оба репортерных гена (Рис. 3A, правильная группа). AAV ITR-опосредованная межмолекулярная рекомбинация между химерными геномами Ad/AAV, в дополнение к гомодимерам, экспрессия одного из этих двух репортерных генов, выдал бы гетеродимеры, кодирующие и DsRed и EGFP (Рис. 3A, оставленный группу). Следствия трех независимых экспериментов показали, что DsRed-и EGFP-позитивные-клетки были редки (Рис. 3C, оставленный группу). Подобные результаты были получены в группе контроля (Рис. 3C, правильная группа), указывая, что клетки с DsRed и EGFP являются, наиболее вероятно, результатом двух независимых событий трансдукции единственной клетки вместо того, чтобы быть вызванными передачей упакованных гетеродимеров. Взятые вместе, эти данные предполагают, что гетеродимеризация через межмолекулярную рекомбинацию в AAV ITRs не играет значительную роль в блоке от хвоста к хвосту hcAd/AAV химерных геномов.
![]()
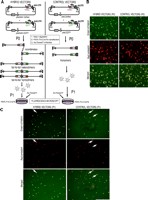
В заключение комбинация 5′Ad с 3′AAV ITRs в pAd/AAV строит пары Ad зависимой ДНК репликации к ITR-зависимой димеризации, приводя к блоку, в клетках производителя, двойных hcAd/AAV
![]()
фантастических геномов с от хвоста к хвосту геномная организация. Таким образом AAV ITR может использоваться гетерологичной Ad ДНК репликацией, чтобы произвести димерного Ad репликоны с определенной структурой.
Распространение и определение количества двойных hcAd/AAV гибридных векторных частиц. Впоследствии, мы определили, могли ли после блока двойные hcAd/AAV. eDYS векторные частицы быть эффективно усилены последовательным распространением. С этой целью, PER. tTA. Cre76 клетки были инфицированы вирусом с MssI-переваренным pAd/AAV. eDYS, зараженным AdfloxedШ, пока CPE не наблюдался. Клеточные культуры, соответствующие этому начальному шагу (P0) , были собраны, и одна десятая очищенных лизатов была добавлена к недавно отобранному PER. tTA. Cre76 клетки, вместе с AdfloxedШ в MOI 2 IU/клетками (отрывок P1). Эта схема инфекции была повторена в последующих пробах (то есть, P2 через P4), за исключением использования увеличивания числа клеток. Из-за маркировки N-терминального конца дистрофина EGFP, усиление векторных частиц могло быть с готовностью проверено при помощи прямой флюоресцентной микроскопии (не показано) и проточной цитометрии (Рис. 4). Следствия трех независимых проб, начатых с MssI-леченным pAd/AAV. eDYS, показали эффективное усиление двойных hcAd/AAV. eDYS гибридных векторных частиц с процентом EGFP-дистрофин позитивных клеток, увеличивающихся от 3.3 ± 0.46 в P1 до 92.0 ± 1.26 в P4 (Рис. 4). Пробы контроля с непереваренным pAd/AAV. eDYS выдавали очень немного PER. tTA. Cre76 клеток EGFP-дистрофин позитивных, указывая на небольшое количество высвобожденных химерных геномов Ad/AAV от ковалентной присоединенной прокариотической ДНК, для достижения эффективного образования поколения двойных hcAd/AAV гибридных векторных частиц.
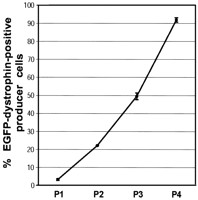
Осветленные лизаты клеток, полученные после трех раундов векторного распространения, были очищены ультрацентрифугированием CsCl. Затем, функциональные титры очищенных гибридных векторных образцов были определены двумя различными методами. Первый метод определил количество активности переноса генов EGFP-дистрофина, существующей в двойных hcAd/AAV гибридных векторах титрованиями результата на клетках индикаторах HeLa при использовании проточной цитометрии (Таблица 1). Вторая процедура состояла из титрований результата на PER. tTA. Cre76 клетках, разрешавших реплекацию ДНК двойного hcAd/AAV гибридного вектора при инфекции АdfloxedШ помощника. Эта схема компенсирует тусклую флюоресценцию белка EGFP-дистрофина усилением сигнала флюоресценции EGFP-дистрофина в преобразованных клетках индикатора. Основанные на репликации пробы были разработаны для более высокой чувствительности и таким образом лучшиего определении приблизительного числа EGFP-дистрофин преобразованных частиц в гибридных векторных образцах. В этих экспериментах титрования действия переноса генов было определено количественно проточной цитометрией и прямой флюоресценцентной микроскопией.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



