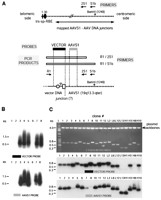
Чтобы далее подтвердить природу этих вставок, как являющихся AAVS1-гибридными векторными соединениями ДНК, образцы ДНК были переданы в двойном экземпляре и инкубированны отдельно с пробами, изображенными в Рис. 9A. После ауторадиографии оба гибридных вектора - и AAVS1-специфические пробы признали всех проанализированных клонов (Рис. 9C, середина и более низкие группы, соответственно), подтверждая это они представляют соединения между местом перед интеграцией AAV на хромосоме 19 и гибридной векторной ДНК. Вставки клонов Л13, Х1, и H8 (Рис. 9C, средняя группа) и 8 (Рис. 9C, более низкая группа) были обнаружены после увеличения времени выдержки в отсутствие любых других сигналов гибридизации (не показано). Интересно, для обоих проб сила сигнала изменились у различных клонов (Рис. 9C, середина и более низкие группы). Кроме того, большинство клонов реагировало до различной степени с двумя пробами (Рис. 9C, сравните середину и более низкие группы). Эти результаты указывают на существование определенных для клона усечений не только в области AAVS1, но также и в пределах гибридного векторного воздействия ДНК, до различных степеней, отжига исследования. Поэтому, чтобы изучить в мелких деталях структуру AAVS1-гибридных векторных соединений ДНК, исследования последовательности нуклеотидов были выполнены у клонов 3, 5, 7, L2, и H10. Результаты, полученные в итоге Рис. 10A, подтвердили организменные хромосомные контрольные точки ДНК, рассеянные всюду по области AAVS1 вниз по течению trs и связанного Rep элемента ( Рис. 10B). Кроме того гибридная векторная ДНК всегда ломалась вверх по течению в p5IEE последовательности (Рис. 10C). Эти данные подтверждают, что у каждой вставки есть определенная последовательность. Кроме того проанализированные соединения не содержали последовательности кроме таковых из гибридного векторного генома и AAVS1. Наконец, интенсивности гибридизации при саусен блот анализе совместимы с данными о последовательности ДНК. В целом эти эксперименты демонстрируют способность двойных hcAd/AAV гибридных векторов предназначаться для чужеродной ДНК в AAVS1 на человеческой хромосоме 19 при условии, что Rep78 и Rep68 доступны в пределах преобразованных клеток.

Дискуссия
hcAd векторы достигают эффективного транспорта полной последовательности ДНК in vitro и in vivo (19, 27, 31) и благодаря недостатку Ad протеин кодирующей последовательности значительно менее иммуногены, чем Ad векторы с одним или более удаленным ранним регионом (28). Тем не менее, если используются большие количества Ad капсидов in vivo, это может вызвать активацию иммунной системы. (5, 49). Поэтому, увеличение числа терапевтических генных копий, поставленных в пределах каждой капсулы вируса, позволит использовать более низкие векторные дозы при достижении определенного трансгенного уровня экспрессии. Кроме того, обычные hcAd векторы не удовлетворяют необходимость постоянного генетического исправления распространяющихся групп клеток, потому что поставленная ДНК обычно остается в клетках. В данном исследовании представлена новая система переноса генов, которая основывается на привлекательных особенностях hcAd векторов. Эти двойные hcAd/AAV гибридные векторы несут димерные геномы и могут устойчиво преобразовать клетки интеграцией ДНК в предопределенное место в пределах человеческой ДНК.
![]()
Здесь, мы показали, что механизм репликации ДНК может быть соединена с AAV ITR-опосредованным процессом димеризации, чтобы собрать определенные ДНК репликоны в зараженных вектором помошником клетках. Применяя этот принцип мы произвели гибридные векторные частицы, кодирующие две человеческих последовательности дистрофина во всю длину. Мы предполагаем два пути для повторного исследования двойных hcAd/AAV гибридных векторов (Рис. 11). После трансфекции MssI-переваренных гибридных векторных плазмид Ad/AAV в PRE tTA. Cre76 клетки заражаются вектором помошником Ad. floxedШ с делецией E1. В пути I, AAV ITRs представляют собой в ковалентные закрытые шпильки AAV Rep78 и белки Rep68 или, альтернативно, клеточными действиями, которые действуют на их вторичную структуру подобную Holliday (53, 55). Эта структура может быть сформирована в AAV ITR из-за его мультирецидивирующего характера. Интересно, выше упаковочные уровни химерных геномов Ad/AAV в капсулы вируса наблюдались в присутствии белков AAV Rep наиболее вероятно в результате расширения AAV ITRs от ковалентной присоединенной прокариотической ДНК каталитических действий AAV Rep. Эти данные в соответствии с предыдущими экспериментами с ДНК AAV, ITR-содержащими плазмидами в наличии или отсутствии экспрессии AAV rep(55).
![]()
Комплекс инициирования репликации Ad ДНК признает Ad ITR, расположенный близко к другому концу молекул. Впоследствии, смещение и полимеризация ДНК, которая продвигает через ковалентный закрытый AAV ITR структуры последовала. Эти процессы производят структуры ДНК, содержащие в обоих концах Ad и упаковочных элементов, который делает их эффективными субстратами для репликации Ad ДНК. Для простоты не вынуты двойные дочерние молекулы, произведенные во время этого процесса. Заканчивающиеся одноцепочечные молекулы ДНК содержат AAV ITRs с непарными хвостами в их 3 концах ′. Удаление этих хвостов 3 ′ экзонуклеазами производит шпильки со свободными 3 ′ гидроксильными группами. Эти структуры составляют идеальные инициаторы для полимеризации ДНК. После удлинения двойные 5 ′ Ad ITRs с функциональной Ad ДНК восстановлены. Дальше Ad ДНК подчиненная реинициации, следующей за ДНК полимеризацией через AAV ITR, содержащий в ДНК молекулах оба конца Ad и упаковочные элементы. Эти элементы могут дальше быть амплифицированы и упакованы в Ad капсид. Оба пути не взаимно исключающи, и согласно эксперементальным данным приближаются к одному типу продукции

После сбора двойные hcAd/AAV. eDYS гибридные векторные частицы могли быть усилены высоким титрам посредством последовательного распространения Ad floxedШна PER. tTA. Cre76 клетках. Структурные исследования ДНК, извлеченной из двойных hcAd/AAV. eDYS гибридных векторных частиц, подтвердили накопление тандемных геномов от хвоста к хвосту. Хотя мономеры не были обнаружены в пределах векторных частиц, они присутствовали в экстрахромосомной фракции ДНК клеток производителя после одного раунда распространения. Кроме того они были также найдены в клетках производителя при втором способе (не показано). Эти данные предполагают, что фракция двойных hcAd/AAV химерных геномов заключена в мономеры возможно из-за клеточных действий, действующих на крестообразные структуры подобные Holliday, которые могут быть сформированы в центрально ограниченном AAV ITRs (55). Кроме того отсутствие мономеров из упакованного материала ДНК может быть связано с легкой энкапсидацией димерных геномов, длина которых ниже предела размера генома, что необходимо для эффективного накопления ДНК (37).
Данные флюоресцентной микроскопии из экспериментов с рекомбинантным человеческим дистрофином, помеченным в окончании N EGFP, вместе с результатами иммуногистохимии, полученными с MAb для С конца дистрофина, показали эффективную передачу рекомбинантного гена в мышечные клетки in vitro и в естественных условиях и синтез белка дистрофина во всю длину в этих клетках. Хотя этот белок ограничивал положение ядер к сарколемме страдающих дистрофией mdx волокон мышцы, перераспределение ядер мышечного волокна к периферии синцития не наблюдалось. Этот результат является, вероятно, относящимся к факту, что процедура переноса генов имела место во взрослую клетку (13) и к промежутку времени, требуемому для этого феномена. Предыдущие результаты указали на причастность последовательности ДНК, которая накладывается p5 промотором в предназначенной интеграции ДНК AAV из-за высокой частоты контрольных точек, наблюдаемых в пределах или около этой области в дополнение к контрольным точкам, которые были найдены в AAV ITRs (14, 43, 50). Позже, непосредственного участия этой последовательности ДНК в интенсивной определенной для места интеграции иностранной ДНК было продемонстрировано в экспериментах трансфекции, выполненных с круглыми плазмидами(38, 39). p5IEE отсутствует в стандартных рекомбинантных векторах AAV, которые содержат от вирусного генома исключительно AAV ITRs. Введение p5IEE последовательности в рекомбинантные векторы AAV, чтобы восстановить интенсивную сайт специфическую интеграцию ДНК, далее уменьшит их уже ограниченную способность кодирования. В данном исследовании мы представили свидетельства, что эффективный Ad, установленный капсулой вируса процесс переноса генов может быть использован, чтобы ввести в ядра целевых клеток большие сегменты ДНК, напоминающие о провирусных геномах AAV, и мы показали, что эти структуры - субстраты для AAVS1-предназначенной интеграции ДНК в присутствии белков члена палаты представителей AAV. Исследования последовательности нуклеотида AAVS1-гибридных векторных соединений ДНК показали, что контрольные точки встречались вверх по течению в p5IEE, оставляющем позади полное Ad ITR и некоторые или все Ad упаковочные элементы. Эта особенность важна по двум причинам. Во-первых, это предполагает, что разрушение терапевтических и/или трансгенных последовательностей ДНК часто не происходит и, во-вторых, это указывает, что интегрированная генетическая информация не будет склонной к мобилизации после инфекции устойчиво преобразованных клеток с диким типом Ad (40).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



