При прямой флюоресценции распространение EGFP-дистрофина через собранные de novo векторные частицы было предотвращено присоединением агара. При этих условиях флюоресценция EGFP-специфического дистрофина была ограничена отдельными клетками индикатора в (Рис. 5A). С прогрессией репликационного цикла единственные EGFP-дистрофин позитивные клетки, как ожидалось, развивались во флуоресцентные фокусы, обнаруженные прямой флюоресценцентной микроскопией через 5 дней. (Рис. 5B). Определение количества этих фокусов показало, что их число было немного выше чем таковые из единственных EGFP-дистрофин позитивных клеток, предполагая, что это основанно на репликации проб, определеное действий переноса генов двойных hcAd/AAV. eDYS гибридных векторов после 20 часов. Титры, полученные прямой флюоресцентной микроскопией были в среднем втрое ниже чем измеренные после 20 часов при помощи проточной флюоресцентной цитометрией клеток индикатора, которые не были покрыты агаром. Это различие не может быть приписано вторичным хитам, так как свидетельства роста сигнала EGFP-дистрофина не наблюдался при прямой флюоресценцентной микроскопии после инкубационного периода 20 часов. Независимо от используемой пробы титрования можно прийти к заключению, что двойные hcAd/AAV. eDYS гибридные векторные частицы относительно легко произвести и могут быть сконцентрированы в высоких титрах.
![]()
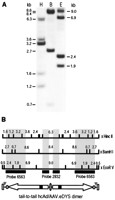
Структура двойных hcAd/AAV гибридных векторных геномов. Чтобы исследовать структурную организацию упакованных химерных геномов Ad/AAV, ДНК была извлечена из очищенных гибридных векторных частиц. Затем, восстановленная ДНК была переварена с HincII, BamHI или EcoRV и подвергнута Саузерн-блот-анализу со смесью двух специфичных для вектора проб. Результаты, показаны на Рис. 6A, совместимы исключительно с тандемной от хвоста к хвосту геномной организации для упакованной гибридной векторной ДНК Ad/AAV (Рис. 6B), демонстрируя, что ранее идентифицированные от хвоста к хвосту репликационные формы (Рис. 2B, переулки 8, 10, 12, 15, и 16, и Рис. 2C) являются
упаковочно-компетентными субстратами. Значительно, никакие добавочные формы ДНК или любые другие геномные конструкции такие как лицом к лицу или димеры головы к хвосту не были идентифицированы. Интересно, что фрагменты ДНК, соответствующие мономерным геномам, ранее обнаруженным в клетках производителя во время первого раунда распространения гибридных векторных частиц, не были упакованы (сравните Рис. 2B, 7, 9, и 15, с Рис. 6A, B, и сравните Рис. 2B, 8, 10, и 16, с Рис. 6A, E).
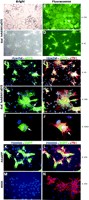
Передача человеческой последовательности кодирующей дистрофин во всю длину крысиным кардиомиоцитам in vitro двойными hcAd/AAV. eDYS гибридными векторами. В общей сложности 95 % людей с МДД имеют повреждение миокарда, и 10 - 15 % из них умирают из-за порока сердца (8). Сердца этих пациентов повреждены механическими силами из-за отсутствия функционального дистрофина в кардиомиоцитах (9). Клетки сердечной мышцы известны тем, что были невосприимчивыми к большинству способов трансгенеза. Однако, Ad векторы с делецией E1-, как показывали, преобразовывали кардиомиоциты in vitro, так же как в естественных условиях(20). Таким образом мы решили проверить, могли ли мы предоставить человеческий ORF во всю длину в кардиальные клетки двойной hcAd/AAV. eDYS гибридной векторной трансдукцией. С этой целью in vitro модели использовалась культуры кардиомиоцитов новорожденной крысы. Эти культуры были мнимо преобразованны или преобразованны с помощью 103 FFU двойного hcAd/AAV. eDYS гибридного вектора и, прямая флюоресцентная микроскопия и иммунофлюоресцентная микроскопия использовались, чтобы обнаружить EGFP-дистрофин и cTNI белки, соответственно. Основные культуры крысиных кардиомиоцитов, преобразованные Ad вектором с удаленным E1 и кодирующий EGFP, служила контролем. Другой контроль состоял из клеток HeLa, преобразованных двойными hcAd/AAV. eDYS гибридными векторными частицами. Векторы Ad преобразуют эти клетки человека очень хорошо. Прямая флюоресценция EGFP-дистрофина показала наличие белка слияния в> у 90 % клеток HeLa (Рис. 7A и B) и у 70 - 80 % сердечных клеток (Рис. 7C и D). Иммунореактивность клеток определена для кардиотонического маркера TNI (Рис. 7F, H, J, L, и N) и их ритмичное сокращение, которое продолжалось после трансдукции (не показанный), подтвердило, что значительная фракция клеток в этих культурах действительно кардиомиоциты. Кроме того характерная полосатая структура объединения cTNI в кардиальных мышечных клетках различалась (Рис. 7J). Обнаружение белка EGFP-дистрофина (Рис. 7E и G) в значительном большинстве TNI-позитивных-клеток (Рис. 7F и H) указывает на эффективную трансдукцию кардиомиоцитов двойными hcAd/AAV. eDYS гибридными векторными частицами. Наконец, сравнение внутриклеточного распределения EGFP и EGFP-дистрофина показало, что, в то время как первый проникал во всю клетку, включая ядро (Рис. 7 K), последний был исключен из ядер и был найден связанным с плазмолеммой кардиомиоцитов (Рис. 7 г и I). Эти результаты - в согласии с известной внутриклеточной локализацией дикого типа дистрофина и с данными, восстановленными из экспериментов с этим геномом EGFP-дистрофина в контексте невирусных трансфекций ДНК (6). Наконец, мнимо преобразованные клетки не показывали зеленую флюоресценцию, показывая, что этот сигнал был определенным для наличия EGFP в преобразованных вектором клетках (Рис. 7M и N).
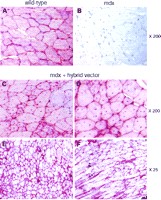
Передача последовательности содержащий человеческий дистрофин во всю длину страдающей дистрофией скелетной мышце мишей в естественных условиях двойными hcAd/AAV. eDYS гибридными векторами. Основная генетическая причина дистрофии у mdx мышей находится в преждевременной остановке кодона в экзоне 23 гена дистрофина (47). За исключением редких так называемых ревертантных волокон мышц, дистрофин не наблюдается в ткани мышцы mdx мышей. Скелетные мышци взрослых mdx мышей показывают определенную гистопатологическую особенность МДД такогую как гетерогенность в диаметре волокон мышц и высокую распространенность расположенных в центре ядер. Эти признаки делают mdx мышей привлекательной образцовой системой для того, чтобы оценить процедуры, направленные на восстановление синтеза дистрофина, особенно на гистологическом уровне. Для оценки эффективности двойной hcAd/AAVгибридной вектор-опосредованной генной доставки, мы провели инъекции икроножных мышц у 6-ти недельных mdx мышей с
![]()
2 Ч 108 FFU двойных hcAd/AAV. eDYS гибридных векторов. Отрицательная контрольная группа составляла из икроножных мышц, в которые введен буферный раствор, тогда как позитивная контрольная группа состояла из дикого типа мышей. Через 6 дней после инъекции секции мышцы от каждой из экспериментальных групп были подвергнуты иммуногистохимии при использовании MAb, направленного против C-терминальной части дистрофина. Иммуногистохимические исследования позитивной контрольной группы полученных из мышей дикого типа, показали сарколемное окрашивание в однородных по размеру волокнах мышцы с периферическими ядрами (Рис. 8A), тогда как таковые из введенных симуляцией мышц не показывали дистрофин-положительные волокна (Рис. 8B). Результаты, полученные с положительными и отрицательными образцами контроля, свидетельствуют о специфичности иммуногистохимической пробы для дистрофина. Исследования поперечных разрезов, полученных из образца мышц мышей получивших инъекцию двойного hcAd/AAV. eDYS гибридного вектора, показали ясную и широко распространенную рекомбинантную экспрессию дистрофина во всю длину (Рис. 8C к F)., ограниченную в сарколемме страдающих дистрофией волокон мышцы, как упомянуто выше, широким диапазоном размеров поперечного сечения и центральных ядер (Рис. 8C и D). В дополнение к сильной маркировке сарколеммы некоторые волокна также показали поддающееся обнаружению эндоплазматическое окрашивание, обусловленное трансгенной чрезмерной экспрессией (Рис. 8E). Взятые вместе, эти эксперименты демонстрируют способность двойных hcAd/AAV. eDYS гибридных векторов эффективно поставлять и экспрессировать последовательность кодирующую человеческий дистрофин во всю длину в кардиомиоцитах in vitro так же как во взрослой страдающей дистрофией скелетной мышце в естественных условиях.
![]()
Нацеленная интеграция ДНК после трансгенеза двойного hcAd/AAV гибридного вектора. Наконец, мы занимались исследованиями, могло ли введение двойных hcAd/AAV химерных геномов в клетки человека. С этой целью клетки HeLa были инфицированы вирусом или с плазмидой экспрессии pGAPDH. Rep78/68 кодирующий AAV Rep78 и Rep68 или с плазмидой экспрессии pKS. P5. Элемент кодирующий Rep78, Rep68, Rep52, и Rep40. Контрольные группы состояли из ложно-инфицированных вирусом клеток HeLa и из клеток HeLa, инфицированных вирусом с плазмидой pEFO. DsRed. T4, содержащий DsRed ORF вместо AAV. Затем, клетки были пребразованы двойными hcAd/AAV. eDYS гибридными векторными частицами в трех различных MOIs. Через 3 дня p. i., геномная ДНК была извлечена из этих клеток, и ПЦР проба интеграции ДНК была выполнена, чтобы обнаружить AAVS1-гибридные векторные соединения ДНК, используя два набора инициатора (Рис. 9A).Эти инициаторы отжигают гибридный векторный геном и хромосому 19, где вставки ДНК AAV были картированы (30, 32, 43). ПЦР-усиленные образцы были подвергнуты электрофорезу в геле агарозы и соусен блот анализу или с гибридным вектором - или с AAVS1-специфической пробой (Рис. 9B, верхние и более низкие группы, соответственно). В обоих случаях накоплении по-другому размерных фрагментов ДНК, мигрирующих, поскольку, мазок наблюдался в образцах инфицированных вирусом и двойных hcAd/AAV. eDYS-инфицированных клеток (Рис. 9B, 3 - 5, 7, и 8). Образцы произошли из клеток HeLa, которые были преобразованы двойными hcAd/AAV гибридными векторными частицами будучи или мнимо или pEFO. DsRed. T4-инфицированны (Рис. 9B, 1 и 2, соответственно) не выдавал сигналы гибридизации. Эти результаты демонстрируют Rep зависимую нацеленную интеграцию AAV гибридной векторной ДНК в AAVS1. События интеграции ДНК AAV не сайт специфичны, определенные в классическом смысле, так как они не имеют место в единственном положении нуклеотида, но в относительно протяженном участке ДНК. Следовательно, AAVS1-гибридные векторные соединения ДНК, произведенные посредством интеграционного процесса ДНК AAV, обычно присутствуют как единственные копии в пределах AAVS1- клеток. Поэтому, наблюдаемый мазок наиболее вероятно отражает усиление смеси AAVS1-гибридных векторных соединений ДНК с различными длинами. Чтобы исследовать это, продукты ПЦР были клонированы в вектор pCR4-TOPO. Рекомбинантные плазмиды из рандомизированно отобранных колоний были переварены с EcoRI, чтобы выпустить вставки. Исследования электрофорезом в геле агарозы показали вставки с различными размерами, отражающими разнообразие размеров фрагмента ДНК, наблюдаемых в Рис. 9B (Рис. 9C, верхняя группа).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



