На основании обнаруженных воды и оксида углерода (IV) сделайте вывод о качественном составе Crоревшего вещества.
2. Зажгите парафиновую свечу и аналогичным путем установите качественный состав парафина. Проведите опыт по обнаружению свободного углерода в пламени свечи.
Составьте уравнение реакции горения парафина свечи, приняв, что в его молекуле содержится 16 атомов углерода.
Примечание: опыты 1 или 2 проводятся по выбору учащихся.
3. Соберите прибор, как указано на рисунке 22.5, и испытайте его на герметичность.
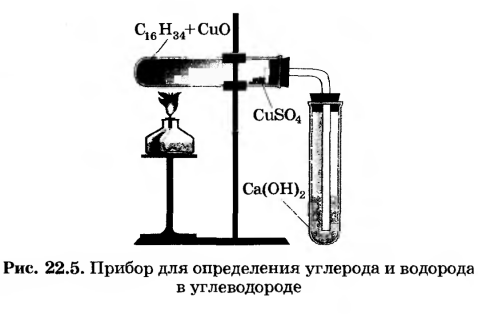
В сухую пробирку поместите 2— 2,5 г оксида меди и немного вазелина, чтобы его хватило только для пропитки подогретого оксида меди (II). Закрепите пробирку в штативе горизонтально и внесите в нее не более 0,5 г сульфата меди (II), разместив около отверстия пробирки. Закройте пробирку пробкой с газоотводной трубкой, конец которой
опустите в пробирку с известковой водой. Нагревайте пламенем горелки (спиртовки) смесь оксида меди (II) с вазелином.
Наблюдайте, какие изменения происходят с известковой водой. По окончании опыта, прежде чем погасить пламя горелки, поднимите вверх лапку штатива с прибором и выньте газоотводную трубку из пробирки. (Почему это надо проделать?)
На основании результатов опыта сделайте вывод о качественном составе вазелина. Составьте уравнение реакции полного окисления оксидом меди предельного углеводорода, в состав которого входит 16 атомов углерода.
Из опыта следует, что в сгоревшем веществе есть углерод и водород.
б) Эксперимент проводится аналогично опыту а). Уравнение реакции горения парафина:
![]()
Для обнаружения свободного углерода в пламени свечи нужно подержать чистое стекло над пламенем. Стекло постепенно закоптится. Это и есть свободный углерод.
Тема: Взаимодействие этилена с бромной водой, раствором перманганата калия
Цель работы: экспериментальным путем получить этилен, провести качественные реакции, доказывающие непредельный характер этилена; совершенствовать умение получить газообразные вещества.
Оборудование и реактивы: металлический штатив, лабораторный штатив с пробирками, спиртовка, спички, пробка с газоотводной трубкой, фарфоровая чашка, тигельные щипцы, смесь этанола и концентрированной серной кислоты, растворы перманганата калия, бромная вода, чистый песок или кусочки пористой керамики.
Получаем этилен нагреванием смеси этилового спирта с концентрированной серной кислотой. Опустим газоотводную трубку с выделяющимся этиленом в подкисленный раствор перманганата калия. Раствор быстро обесцвечивается. При этом этилен окисляется в двухатомный спирт этиленгликоль.
СН2=СН2 + [О] + Н-ОН = CH2ОН - CH2ОН
Эта реакция является качественной реакцией на двойную связь.
Тема: Изучение растворимости спиртов в воде.
Цель работы: познакомиться со свойствами кислородсодержащих органических соединений, которые включают полярную функциональную группу, определяющую их физические и химические свойства; изучить особые свойства многоатомных спиртов; определить роль функциональной группы в формировании физических свойств и химической активности спиртов.
Оборудование и реактивы: штатив с пробирками, дистиллированная вода, этанол, пропанол, глицерин, сульфат меди (II), раствор гидроксида натрия, серной кислоты.
Экспериментальная задача I. Уровень I
Изучение растворимости спиртов в воде.
В три пробирки наливаем по 1 мл этанола, пропанола и глицерина.
Рассчитываем относительные молекулярные массы спиртов.
Располагаем пробирки в штативе в порядке увеличения относительной молекулярной массы спиртов.
Добавляем в каждую пробирку по 2 мл дистиллированной воды.
Встряхиваем пробирки.
Наблюдаем за растворимостью спиртов, используя для характеристики слова «хорошо», «ограниченно», «плохо».
Результаты сверяем с табличными.
|
|
|
|
|
|
|
|
|
| ||
|
|
|
|
Тема: Изучение восстановительных свойств альдегидов: реакция «серебряного зеркала», восстановление гидроксида меди (II).
Цель работы: закрепить знания о свойствах альдегидов и с помощью качественных реакций распознавать альдегиды среди органических соединений.
Оборудование:
чистые пробирки.
Реактивы:
раствор глюкозы (1 таблетку на 50 мл воды),
раствор сульфата меди (II),
раствор гидроксида натрия, аммиачный раствор оксида серебра (готовится из ляписного карандаша и раствора нашатырного спирта).
Ход работы.
Восстановление гидроксида меди (II)
1. Налейте в пробирку 1 мл раствора глюкозы и добавьте 1 мл раствора гидроксида натрия.
2. Прилейте по каплям раствор сульфата меди (II). Образуется ярко-синий раствор глюконата меди.
3. Подогрейте раствор на кипящей водяной бане (в стакане с кипятком). Выпадает красный осадок оксида меди (I).
Восстановление оксида серебра - реакция "серебряного зеркала"
1. Налейте в пробирку 1 мл раствора глюкозы и добавьте 1 мл аммиачного раствора оксида серебра.
2. Подогрейте раствор в стакане с горячей водой. Наблюдайте образование на стенках пробирки "серебряного зеркала".
Тема: Растворимость различных карбоновых кислот в воде. Взаимодействие уксусной кислоты с металлами. Получение изоамилового эфира уксусной кислоты.
Цель работы:
Получить уксусную кислоту и изучить её свойства; закрепить знания о карбоновых кислотах, сложных эфира. Получить этиловый эфир уксусной кислоты, исследовать его физические свойства.Реактивы и оборудование:
ацетат натрия, серная кислота (конц.), уксусная кислота, магний (порошок), цинк, гидроксид натрия, карбонат натрия, фенолфталеин, универсальная индикаторная бумага, прибор для получения и собирания кислоты, спиртовка, пробирку, вата, спички. конические колбы с пробками, мерные цилиндры, навески мыла и синтетического моющего средства, пробирки, разбавленные растворы соляной или серной кислот, раствор гидроксида натрия или калия, раствор ацетата свинца, сульфат меди (II), фенолфталеин, жесткая вода.Ход работы
Напишите возможные изомеры для соединений с формулой С5Н10О2 С какими из перечисленных веществ будет реагировать уксусная кислота: оксид магния, гидроксид алюминия, сульфат бария, карбонат калия, формиат натрия, цинк? Запишите уравнения возможных реакций. Как осуществить превращения: этан – этилен – ацетилен – ацетальдегид – уксусная кислота – метиловый эфир уксусной кислоты.Опыт 1. Получение уксусной кислоты.
В пробирку с ацетатом натрия прибавить 1- 2 мл концентрированной серной кислоты. Закрыть пробирку пробкой с газоотводной трубкой, конец которой опустите в другую пробирку вход в пробирку прикрыть ваткой, смотрите рисунок:
Смесь в пробирке осторожно нагревайте до тех пор, пока в приёмнике –
пробирке не собёрётся 1 -2 мл жидкости. Прекратите нагревание, закройте спиртовку.
Опустите в пробирку с образовавшейся жидкости универсальную индикаторную бумагу. Как изменился цвет индикатора? Почему? Запишите уравнение диссоциации уксусной кислоты.
Опишите запах, образовавшейся жидкости? Соблюдайте осторожность при определении запаха! Составьте уравнение данной химической реакции.
Опыт 2. Взаимодействие уксусной кислоты с металлами.
Посмотрите видео-опыт «Взаимодействие уксусной кислоты с металлами»
В одну пробирку положите гранулу цинка, в другую порошок магния. В обе пробирки прилейте 1 мл уксусной кислоты. Что наблюдаете? Сравните скорость этих реакций? Запишите соответствующие уравнения химических реакций, назовите продукты, укажите тип реакции.
Тема: Действие аммиачного раствора оксида серебра на сахарозу.
Ход работы:
а) В пробирку, содержащую 1-2 мл раствора сахарозы в воде, прилейте 1-2 мл аммиачного раствора оксида серебра и нагрейте пробирку на кипящей водяной бане. Что наблюдается?
б) В пробирку, содержащую 1-2 мл раствора сахарозы в воде, добавьте несколько капель разбавленной серной кислоты и нагрейте на кипящей водяной бане в течение 5-10 мин. Затем охлажденный раствор доведите до слабощелочной реакции (проба на лакмус), добавив в пробирку раствор щелочи. К полученному раствору добавьте 1-2 мл аммиачного раствора оксида серебра и нагрейте пробирку на кипящей водяной бане.
Почему сахароза не дает реакцию «серебряного зеркала»? Какие процессы происходят с сахарозой при нагревании ее раствора с кислотой? Почему после нагревания проба с аммиачным раствором оксида серебра дает положительный результат? Напишите уравнение реакции гидролиза сахарозы.Тема: Денатурация белка. Цветные реакции белков.
Приготовьте раствор белка. Для этого белок куриного яйца растворите в 150 мл воды. В пробирку налейте 4—5 мл раствора белка и нагрейте на спиртовке до кипения. Отметьте помутнение раствора. Охладите содержимое пробирки и разбавьте водой в 2 раза.
Вопросы
1. Почему раствор белка при нагревании мутнеет?
2. Почему образующийся при нагревании осадок не растворяется при охлаждении и разбавлении водой?
Цветные реакции белков
Ксантопротеиновая реакция. В пробирку налейте 2—3 мл раствора белка и прибавьте несколько капель концентрированной азотной кислоты. Нагрейте содержимое пробирки, при этом образуется жёлтый осадок. Охладите смесь и добавьте раствор аммиака до щелочной реакции (проба на лакмус). Окраска переходит в оранжевую.
Биуретовая реакция. В пробирку налейте 2—3 мл раствора белка и 2—3 мл раствора гидроксида натрия, затем 1—2 мл раствора сульфата меди (II). Появляется фиолетовое окрашивание.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



