CH2(OH)-CH(OH)-CH(OH)-CH(OH)-CH(OH)-CHO + + 2Cu(OH)2=CH2(OH)-CH(OH)-CH(OH)-CH(OH)-CH(OH)-COOH + Cu2O + 2H2O
3. Выпадает осадок серебра на стенка пробирки. Это означает что глюкоза относится к классу альдегидов
CH2(OH)-CH(OH)-CH(OH)-CH(OH)-CH(OH)-CHO + Ag2O=CH2(OH)-CH(OH)-CH(OH)-CH(OH)-CH(OH)-COOH + 2Ag
Лабораторная работа №7
Тема: Свойства крахмала.
Цель: изучить свойства углеводов на примере крахмала.
1. В пробирку насыпьте немного порошка крахмала. Прилейте воды и взболтайте смесь. Что можно сказать о растворимости крахмала в воде? 2. Вылейте взвесь крахмала в воде в химический стакан с горячей водой и прокипятите ее. Что наблюдаете? 3. В пробирку с 2-3 мл полученного во втором опыте крахмального клейстера добавьте каплю спиртового раствора йода. Что наблюдаете?
Ход выполнения лабораторной работы, ответы на вопросы:
1. В первом опыте лабораторной работы крахмал не растворился в воде, а образовалась взвесь крахмала в воде. отсюда можно сделать вывод что крахмал не растворим в холодной воде.
2. Во втором опыте наблюдаем следующее: образовался коллоидный раствор (клейстер)
3. Окрас клейстера в синий цвет
Лабораторная работа №8
Тема: Свойства белков.
Цель: изучить свойства белков
В пробирку налейте 2 мл раствора белка и добавьте 2 мл раствора щелочи, а затем несколько капель раствора медного купороса (сульфата меди (II)). Что наблюдаете?
2. В пробирку с 2 мл раствора белка добавьте несколько капель азотной кислоты. Что наблюдаете? Нагрейте содержимое пробирки. Что наблюдаете? Охладите смесь и добавьте к ней по каплям 2-3 мл нашатырного спирта. Что наблюдаете?
3. Подожгите несколько шерстяных нитей. Охарактеризуйте запах горящей шерсти.
4. К 3-4 мл раствора белка в воде добавьте несколько капель раствора медного купороса (сульфата меди (II)). Что наблюдаете?
Ход выполнения лабораторной работы:
1. Раствор приобретает фиолетовый окрас в первом опыте
2. При добавлении азотной кислоты выпадает белый осадок. При нагревании осадок становится желтым. При добавлении нашатырного спирта осадок становится оранжевым
3. В этом опыте появляется характерный запах "жженного рога", который обусловлен наличием в белках такого вещества как серы
4. В четвертом опыте наблюдаем раствор белка приобретает голубой цвет, т. е. происходит разбавление раствора белка раствором медного купороса, химической реакции не происходит
Лабораторная работа №9
Тема: Получение водорода взаимодействием металлов с кислотами.
Цель работы: получить водород взаимодействием соляной кислоты с цинком; изучить некоторые свойства газа водорода.
Оборудование и реактивы: лабораторный штатив, спиртовка, пробирки, пробка с газоотводной трубкой, цинк, раствор соляной кислоты.
Ход работы:

2. Проверьте водород «на чистоту». Для опыта используется водород, собранный вытеснением воздуха. Не изменяя положения пробирки приемника, поднесите ее вплотную к пламени горелки или спички и резко поверните так, чтобы ее отверстие оказалось в пламени. Если при этом раздается резкий “лающий” звук, с газом (водородом) работать нельзя, так как он содержит примесь воздуха. Необходимо некоторое время подождать, пока из пробирки будет вытеснен весь воздух. Если вы услышите легкий звук, напоминающий “п - пах”, с водородом можно работать. Запишите название опыта, ваши наблюдения и соответствующий вывод.
3. Изучение физических свойств водорода.
Рассмотрите пробирку с собранным водородом и отметьте его физические свойства: агрегатное состояние, цвет, вкус, запах, растворимость в воде, плотность по отношению к воздуху.
Запишите название опыта, ваши наблюдения и соответствующий вывод.
4. Изучение химических свойств водорода.
А) Горение чистого водорода.
Рассмотрите пробирку, в которой проверяли водород на чистоту. Что наблюдаете? Откуда взялось данное вещество в пробирке, ведь вы взяли чистую и сухую пробирку.
Запишите название опыта, ваши наблюдения, составьте уравнение реакции, укажите его тип.
Образец выполнения работы
Что делали? | Что наблюдали? | Выводы |
Получение водорода. | Выделяется газ. Так как газ легче воздуха, поэтому пробирку-приемник устанавливаем вверх дном. | Атомы металла вытеснили атомы водорода из молекулы кислоты. Zn+2HCl=ZnCl2+H2↑ это реакция замещения |
Проверка водорода на чистоту. Через минуту снимаем пробирку с трубки и, не переворачивая, поднесем её отверстием к пламени | Если водород сгорит с легким глухим хлопком, то это доказывает, что он чистый. Если раздастся свистящий звук, то водород смешан с кислородом воздуха. Поджигать такой водород нельзя. Он может взорваться | Водород горючий газ, поэтому горит. |
Рассматриваем пробирку с водородом | Молекула водорода двухатомна-H2. При обычных условиях – это газ без цвета, запаха и вкуса. Самый легкий газ, его плотность в 14,5 раза меньше плотности воздуха. Малорастворим в воде. По распространенности во Вселенной занимает первое место. | |
Рассмотрите пробирку, в которой проверяли водород на чистоту | Внутренняя стенка стакана запотела. | При взаимодействии молекул водорода с молекулами кислорода образуется молекулы воды в виде пара. 2H2+O2= 2H2O При нагревании он отнимает кислород от некоторых оксидов. |
Вывод: Научились получать газ водород. Изучили физические и химические свойства водорода.
Лабораторная работа №10
Тема: Получение и распознавание кислорода.
Цель: получить в лабораторных условиях кислород и изучить его химические свойства.
Ход работы
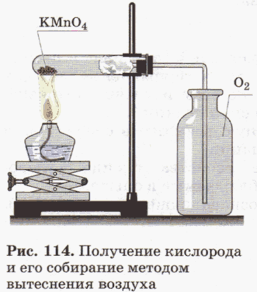
Соберите прибор, как показано на рисунке 114, и проверьте его на герметичность. В пробирку насыпьте примерно на ј ее объема перманганата калия KMnO4 и у отверстия пробирки положите рыхлый комочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки доходил почти до дна сосуда, в котором будет собираться кислород. Наличие кислорода в сосуде проверьте тлеющей лучинкой.
Вопросы и задания
1. Что происходит при нагревании перманганата калия? Составьте уравнение реакции и дайте ее характеристику по всем изученным признакам классификации химических реакций.
2. Рассмотрите записанную реакцию с точки зрения процессов окисления-восстановления.
3. Опишите физические свойства кислорода, непосредственно наблюдаемые в опыте.
4. Опишите, как вы распознавали кислород.
Ответы:
Собрали прибор для получения кислорода и проверили его на герметичность. В пробирку насыпали примерно на 1/4 ее объема перманганата калия у отверстия пробирки положили рыхлый комочек ваты.
Закрыли пробирку пробкой с газоотводной трубкой. Укрепили пробирку в лапке штатива так, чтобы конец газоотводной трубки доходил почти до дна сосуда, в котором будет собираться кислород.
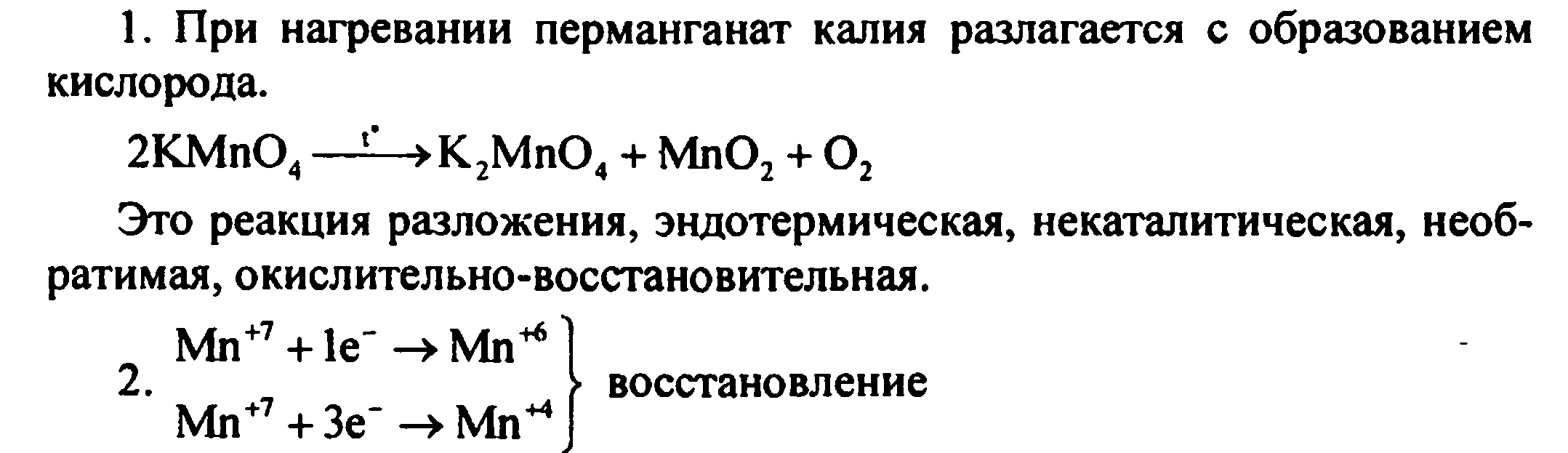

Лабораторная работа №11
Тема: Качественные реакции на катионы металлов.
Ход работы
Исследование сульфата меди
1. Задание: написать формулу, найти относительную молекулярную массу, описать физические свойства, влияние на организм.
Сульфат меди(II) (медный купорос) CuSO4 *5Н2О Мr(CuSO4 *5Н2О) = 249,68г\моль. Синие кристаллы или синий кристаллический порошок без запаха, металлического вкуса. На воздухе и в сухом месте кристаллы выветриваются, и цвет становится светлее. CuSO4 *5Н2О хорошо растворяется в воде (1: 3 в холодной и 1 : 8 в горячей)
1%-й раствор CuSO4 - прозрачная жидкость голубого цвета, используется для внутреннего употребления как рвотное средство.
Плотность + 2,284; температура плавления + 110ОС; температура кипения + +150 ОС.
2. Задание: проделать качественные реакции на ион Сu+2. Написать уравнения реакции в ионном виде.
а) Реакция с NH4OH
Аммиак при взаимодействии с ионом Cu(II) осаждает основные соли переменного состава сине-зеленого цвета.
CuSO4+ NH4OH —> [Cu(NH3)4 ]SO4 +4Н2О
4-5 кап. 1 кап. конц. синий осадок.
б) Железная проволочка или железные опилки, помещенные в раствор соли меди (II), через несколько минут покрывается красным налетом металлической меди.
Сu +2. + Fе(тв.) —> Fе+2 + Сu(тв.)
3. Задание: проделать качественные реакции на обнаружение иона SO4-2 . Написать уравнения реакции.
SO4-2 с ионом Ва+2 образует белый мелкокристаллический осадок сульфат бария, практически нерастворимый в разбавленных минеральных кислотах.
К2SО4 + ВаСl2 = ВаSО4![]() + 2КСl
+ 2КСl
SO4-2 + Ва+2 = ВаSО4![]()
Лабораторная работа №12
Тема: Качественные реакции на анионы кислотных остатков.
Ход работы
Анион | Реактив, уравнение реакции, признаки присутствия данного аниона, открываемый минимум |
F - | 1) AgNO3 не образует осадка, т. к. фторид серебра растворим в воде (в отличие от других галогенидов серебра). 2) Хлорид кальция дает белый осадок фторида кальция. |
Cl - | 1) В азотнокислой среде AgNO3 дает белый осадок, растворимый в NH4OH. Открываемый минимум - 1 µг Cl-, предельное разбавление 1:105. |
Br - | 1) В азотнокислой среде AgNO3 образует светло-желтый осадок. Чувствительность реакции - 20 µг Br -, предельное разбавление 1:2.105. 2) Хлорная вода окисляет бромид-анион до свободного брома, который окрашивает органический растворитель в соломенно-желтый цвет. Фуксин, обесцвеченный гидросульфитом, окрашивается свободным бромом в синий цвет. Чувствительность реакции 50 µг Br-. 2Br - + Cl2 ® 2Cl - + Br2 |
I- | 1) Нитрат серебра образует темно-желтый осадок AgI, нерастворимый в растворах HNO3, и NH4OH (в отличие от хлоридов и бромидов серебра, растворимых в аммиаке). 2) Хлорная вода окисляет йодид-анион до йода: 2I - + Cl2 ® I2 + 2Cl- 3) Открываемый минимум - 40 µг I-; предельное разбавление 1:2,5.104 Выделившийся йод можно открыть с помощью крахмала, который окрашивается йодом в синий цвет, или взбалтывая раствор с органическим растворителем, который приобретает красновато-фиолетовую окраску. При прибавлении избытка хлорной воды окраска исчезает, т. к. свободный йод окисляется до бесцветной йодноватой кислоты: I2 + 5Cl2 + 6H2O ® 2HIO3 + 10H+ + 10Cl - Другие окислители (перманганат калия, дихромат калия и др.) в кислом растворе также окисляют йодид-анион до йода: Cr2O7 2- + 2I - + 14H+ ® 2Cr3+ + 3I2 + 7H2O 2MnO4- + 10I - + 16H+ ® 2Mn2+ + 5I2 + 8H2O |
S2- | 1) Хлористоводородная и др. кислоты при взаимодействии с сульфидами выделяют сероводород, который имеет запах тухлых яиц: S2- + 2H+ ® H2S 2) Сульфид-анион с катионами многих тяжелых металлов образует разноцветные осадки: ZnS (белый), CdS (желтый), CuS, PbS, NiS (черный), HgS (красный) и др. 3) Нитропруссид натрия в щелочном растворе дает красно-фиолетовое окрашивание. |
SO32- | 1) Йодная вода или раствор перманганата калия обесцвечивается. 2) Разбавленные минеральные кислоты выделяют сернистый газ SO2, который обесцвечивает раствор KMnO4 или йода. |
SO42- | 1) Хлорид бария дает белый осадок, нерастворимый в HNO3: Ba2+ + SO42- ® BaSO4 |
CO32- | 1) Минеральные кислоты разлагают карбонаты (и гидрокарбонаты) с образованием углекислого газа СO2, который с известковой водой образует белый осадок: CO32- + 2H+ ® H2O + CO2 Ca(OH)2 + CO2 ® CaCO3 |
SiO32- | 1) Минеральные кислоты выделяют гель кремниевой кислоты |
СН3СОО- | 1) При растирании в ступке уксуснокислой соли с гидросульфатом калия появляется характерный запах уксусной кислоты (сильная кислота вытесняет из соли слабую): CH3COOK + KHSO4 ® CH3COOH + K2SO4 2) Хлорид железа (III) дает на холоде интенсивно-красное окрашивание (вследствие гидролиза до основной соли), при нагревании бурый осадок (образуется конечный продукт гидролиза - гидроксид железа (III)). 3) Этиловый спирт (в присутствии конц. Н2SO4) образует сложной эфир, имеющий специфический фруктовый запах. |
Лабораторная работа №13

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



