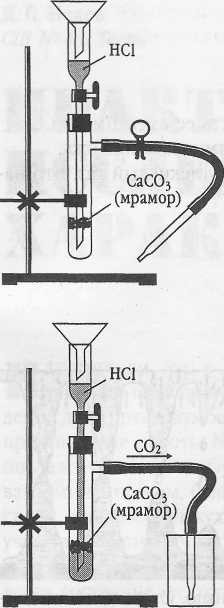
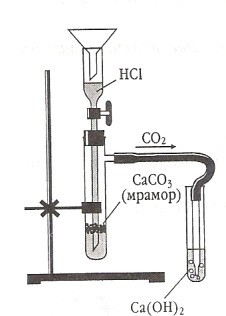
В пробирку с раствором соляной кислоты HCl добавить гранулу Zn. Пробирку немного нагреть (не кипятить!)
Признак реакции __________________________________________________________________________
Уравнение реакции Zn + HCl = ______________________________________________________________
3). Взаимодействие с оксидами металлов.
В пробирку с раствором соляной кислоты добавить горошину оксида меди CuO. Пробирку немного нагреть (не кипятить!).
Признак реакции ___________________________________________________________________________
Уравнение реакции CuO + HCl = _____________________________________________________________
4). Взаимодействие с основаниями.
В пробирку с раствором гидроксида натрия NaOH (добавить 1 каплю ф – ф) добавить 1 – 2 мл раствора соляной кислоты (до исчезновения малиновой окраски).
Признак реакции ___________________________________________________________________________
Уравнение реакции NaОН + HCl = ____________________________________________________________
Ионное уравнение реакции:__________________________________________________________________

Сокращенное ионное уравнение реакции ______________________________________________________

5). Взаимодействие с солями. В пробирку с раствором соляной кислоты HCl добавить 1 – 2 капли раствора нитрата серебра AgNO3 (качественная реакция на ион хлора Cl-).


Признак реакции ___________________________________________________________________________
Уравнение реакции HCl + AgNO3 = ____________________________________________________________
Ионное уравнение реакции: __________________________________________________________________________________________

Сокращенное ионное уравнение реакции __________________________________________________________________________________________

Тема: Получение аммиака, его свойства.
1) Получение аммиака и растворение его в воде
а) Действия: Насыпаем смесь![]()
в пробирку. Закрываем газоотводной трубкой, конец которой направлен вверх. Нагреваем смесь. Наблюдения: Ощущается запах аммиака. Уравнения реакции:![]()
Выводы: Аммиак можно получить, нагревая смесь соли аммония и щелочи. б) Действия: Через некоторое время пробирку с аммиаком, не переворачивая, закрываем пробкой, затем опускаем в кристаллизатор с водой и открываем пробку. Наблюдения: Вода заполняет пробирку.
Уравнения реакции![]()
Выводы: Аммиак очень хорошо растворим, образует![]()
в) Действия: В полученный раствор помещаем красную лакмусовую бумажку. Добавляем к раствору фенолфталеин. Наблюдения: Бумажка синеет; раствор с фенолфталеином розовый. Уравнения реакции:![]()
Выводы: Гидроксид аммония обладает основными кислотными свойствами.
2) Горение аммиака в кислороде
Действия: Нагреваем смесь![]()
затем поджигаем с помощью лучинки газ, выходящий из газоотводной трубки. Наблюдения: Газ горит ярким пламенем. Уравнения реакции: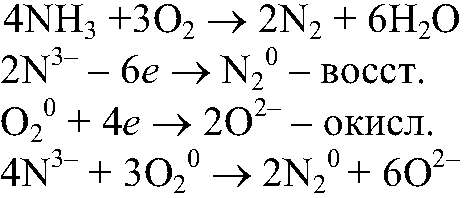
Выводы: В результате горения аммиака образуется азот и вода. Аммиак обладает восстановительными свойствами.
3) Взаимодействия аммиака с кислотами
Действия: Пробирку со смесью нагреваем. Газоотводную трубку последовательно вводим в пробирки с концентрированными кислотами![]()
не касаясь поверхности кислот. Наблюдения: Появляется «белый дым». Уравнения реакции:![]()
Выводы: Аммиак реагирует с кислотами, проявляя основ. св-ва.
4) Свойства водного раствора аммиака
а) Действия: Вводный раствор аммиака опускаем красную лакмусовую бумажку. Наблюдения: Бумажка синеет. Уравнения реакции:![]()
Выводы: Водный р-р аммиака обладает основными свойствами. б) Действия: К водному р-ру аммиака добавляем фенолфталеин Наблюдения: Раствор розовый. Уравнения реакции:![]()
Выводы: В растворе аммиака присутствуют ионы![]()
в) Действия: Добавляем разбавленную соляную кислоту. Наблюдения: Раствор обесцвечивается. Уравнения реакции:![]()
Выводы: Водный раствор аммиака имеет основные свойства.
Тема: Получение гидроксидов алюминия и цинка; исследование их свойств.
Задание. Получите гидроксид алюминия и исследуйте характер его химических свойств.
Оборудование: Штатив с пробирками. Вещества. Растворы соли алюминия, гидроксида натрия, серной кислоты.
Выполнение опыта
1. Налейте в пробирку 2 мл раствора соли алюминия, добавьте по каплям раствор разбавленной щелочи до образования студенистого осадка. Напишите ионные уравнения проведенной реакции.
2. Разделите содержимое пробирки пополам и добавьте к одной части раствор серной кислоты, к другой — раствор гидроксида натрия до «исчезновения» осадка. Напишите ионные уравнения осуществленных реакций.
Сделайте вывод о характере химических свойств гидроксида алюминия.
При добавлении к раствору соли алюминия щелочи образуется студенистый осадок![]()
2.
В обеих пробирках осадок растворяется
![]()
Вывод:
![]()
Тема: Получение и исследование свойств оксидов серы, углерода, фосфора.
Цель: Получить оксида углерода (IV) и изучение его свойства.
Оборудование и реактивы: штатив с пробирками, прибор для получения газов, мел, известковая вода (р-р гидроксида кальция), раствор соляной кислоты, индикатор, лучина
ТБ:
Ход работы
№ и цель опыта | Ход опыта | Наблюдения. Уравнения реакций. Выводы. |
1.Получить оксид углерода (IV) и изучить его физических свойств. |
| Наблюдения : Написать уравнение реакции: CaСO3 + HCl = ... + СO2↑ + ... Физические свойства углекислого газа: ..........
Оксид углерода (IV) ... воздуха, поэтому собираем методом вытеснения....; приемник находится дном... . Горящая лучина в атмосфере углекислого газа..., следовательно, оксид углерода (IV) - газ, который не поддерживает... |
2. Исследование химических свойств оксид углерода (IV). 2.1. Изучение кислотно-основных свойств водного раствора оксида углерода (IV). 2.2. Взаимодействие известковой водой | В стакан с водным раствором СО2 добавляем лакмус Конец газоотводной трубки помещаем в пробирку с известковой водой и пропускаем через нее углекислый газ
Продолжаам пропускать углекислый газ через мутную смесь до полного осветления раствора | Лакмус окрасился в... цвет. СО2 + H2O ⇄ Вывод: оксида углерода (IV) - ... оксид, при взаимодействии с водой образует... кислоту. Наблюдения: Ca(OH)2 + CO2(недост.) = ... ↓ + .... Нерастворимый карбонат превращается в растворимый гидрокарбонат при пропускании через раствор избытка углекислого газа. CaCO3 + CO2 + H2O ↔ Ca(HCO3)2 Вывод: качественной реакцией на углекислый газ является его взаимодействие с... ... . |
4. Окислительно-восстановительные свойства. | В стакан с углекислым газом вносим горящий магний | Наблюдения: CO2 + Mg = Вывод: при взаимодействии с активными металлами оксид углерода (IV) является... |
Вывод: 1.Какая реакция лежит в основе получения оксид углерода (IV)? 2.Перечислите физические свойства углекислого газа, которые наблюдались во время его получения.3. Поясните, какое свойство углекислого газа лежит в основе его определения с помощью зажженной лучины. 4. Объясните, в чем заключается качественная реакция на углекислый газ? |
Тема: Ознакомление с коллекцией удобрений и пестицидов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |