Ознакомление с образцами средств бытовой химии и лекарственных препаратов.
Реактивы и оборудование: образцы чистящих средств «Комет», «Доместос», раствор аммиака, йодкрахмальная бумага (фильтровальная бумага, пропитанная концентрированным раствором иодида калия и крахмальным клейстером), вода; тигель, стеклянная палочка.
Задание: проверьте, что произойдет, если нарушить правило: «Запрещается использовать порошок «Комет» вместе с жидкостями, содержащими аммиак».
Примечания. Аммиак содержат, например, стеклоочищающие и обезжиривающие средства. «Комет» имеет в своем составе вещество, известное под торговым названием «Хлоринол». Судя по всему, это вещество представляет собой соединение, в котором содержится хлор. Возможно, это соль, кислотный остаток которой С1О−.
Вопросы - подсказки
• Какими свойствами — окислительными или восстановительными — обладают хлор и азот в названных веществах?
• Как поведут себя эти вещества, «встретившись» на какой-либо поверхности?
• Образование какого продукта реакции можно ожидать?
• Какой способ качественного определения предполагаемого продукта реакции следует выбрать? (Используйте данные таблицы «Качественные реакции катионов и анионов».)
Ход работы
1. Смешайте в тигле небольшое количество (!) порошка «Комет» и раствора аммиака. (Соблюдайте технику безопасности!)
2. Прикройте тигель влажной йодкрахмальной бумагой.
3. Поясните наблюдаемые процессы.
4. Сделайте вывод о правильности выдвинутой вами гипотезы.
Лабораторные работы.
Лабораторная работа №1
Тема: Определение элементного состава органического вещества.
Цель: установить, содержится ли в составе выданного образца водород и углерод.
Оборудование: пробирки, вата, газоотводная трубка, резиновая пробка, горелка, тигельные щипцы, спички, штатив.
Реактивы: сахар, оксид меди, медный купорос, известковая вода.
Ход работы.
В широкий химический стакан поместите небольшой кусочек парафиновой свечи и подожгите его с помощью горящей лучинки. Обратите внимание на стенки стакана — на них появляются капельки воды. О наличии какого химического элемента в составе парафина они свидетельствуют? Погасите свечу и выньте ее из стакана. Затем налейте в стакан немного прозрачной известковой воды и осторожно взболтайте. Что наблюдаете? О наличии какого химического элемента свидетельствуют изменения, произошедшие с известковой водой? Запишите уравнения проведенных реакций.
Лабораторная работа №2.
Тема: Получение и свойства этилена и опыты с ним.
Цель: Получить этилен путём нагревания смеси этилового спирта с концентрированной серной кислотой и изучить его свойства.
Реактивы и оборудование: Прибор для получения газов, водный раствор перманганата калия, раствор брома в воде (бромная вода), реакционная смесь этилового спирта и серной концентрированной кислоты (1:3), спиртовка, спички.
Ход работы
1. Получение этилена
Получите готовую реакционную смесь. Соберите прибор для получения газов.
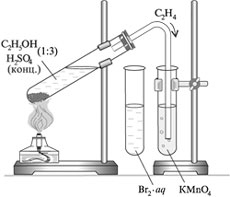
Осторожно, равномерно нагрейте смесь.
Внимание!!!
Соблюдайте осторожность. Вы работаете с концентрированной серной кислотой.
2. Окисление этилена кислородом перманганата калия
Пропустите выделяющийся газ в пробирку с водным раствором перманганата калия, подкисленного серной кислотой.
3. Взаимодействие этилена с бромной водой
Выделяющийся этилен пропустим через раствор брома в воде, который называют бромной водой.
4. Окисление этилена кислородом воздуха (горение)
Поверните газоотводную трубку отверстием вверх и подожгите выделяющийся газ.
5. Оформите работу в тетради в виде таблицы:
Название опыта, рисунок | Ваши наблюдения | Уравнение реакции, выводы |
1 | Какой газ выделяется? | Закончите уравнение реакции: CH3-CH2-OH t>140°C, H2SO4(конц.)→ Укажите тип реакции, назовите продукты реакции? |
2 | Что происходит с раствором марганцовки? | Закончите уравнение реакции: CH2=CH2 + [O] + H2O KMnO4→ Назовите продукты и тип реакции? |
3 | Что происходит с бромной водой? | Закончите уравнение реакции: CH2=CH2 + Br2 → Назовите продукты и тип реакции? |
4 | Почему этилен горит более светящимся пламенем, чем этан? | Закончите уравнение реакции: C2H4 + O2 t → Назовите тип реакции и продукты? |
5. Вывод: (из цели)
Лабораторная работа №3
Тема: Свойства этилового спирта.
Цель: изучить химические свойства одноатомных спиртов.
Ход работы
Изучение кислотных свойств
1. В пронумерованных пробирках находятся щёлочь (№ 1), кислота (№ 2), вода (№ 3) испытайте эти вещества лакмусовой бумажкой, заметьте изменение цвета. Опустите лакмусовую бумажку в спирт. Что наблюдаете? Сделайте вывод.
2. Может ли спирт взаимодействовать с металлическим натрием? Проведите опыт. Составьте уравнение реакции (при затруднении обратитесь к тексту учебника стр.143)
3. Проанализируйте данные опытов 1 и 2, сделайте вывод о «кислотности» спиртов.
Реакции окисления
1. Каков характер горения этанола? Запишите уравнение этой реакции. К какому типу химических реакций относится горение?
2. Можно ли провести реакцию окисления этанола в «мягких» условиях?
2.1. Сильно расколите медную проволоку, свёрнутую на конце в спираль в пламени спиртовки, не давая остыть, бросьте её в стаканчик с этиловым спиртом. Проделайте это ещё раз. Обратите внимание на признаки реакции: а) что произошло со спиралью;
б) изменился ли запах? Составьте уравнение реакции, если одним из продуктов является этаналь.
Что служило окислителем в этой реакции? Какие сильные окислители вам известны ещё?
2.2. В пробирку с 10 каплями этилового спирта добавьте раствор KMnO4 и 4 капли Н2SO4 (к). Слегка подогрейте смесь, обратите внимание на запах. Знаком ли он вам? Что произошло с раствором перманганата калия? Составьте уравнение данной реакции, обозначив KMnO4 - [О].
2.3. Сделайте вывод: подвержены ли спирты действию окислителей.
1. Вспомните, каким способом получают этилен в лаборатории. Запишите уравнение реакции. Определите её тип. Озаглавьте III группу реакций.
2. К 1 мл спирта добавьте несколько капель Н2SO4 (конц.). Слегка подогрейте содержимое пробирки. Осторожно вылейте продукты реакции в стакан с водой, обратите внимание на запах. Где вы встречались с этим веществом? ( Это диэтиловый эфир, запах его вы могли почувствовать в больнице).
3. Сравните исходные вещества и продукты этих реакций. Сделайте вывод.
Лабораторная работа №4
Тема: Свойства уксусной кислоты.
Цель: изучить химические свойства уксусной кислоты.
1. Налейте в четыре пробирки по 2 мл раствора уксусной кислоты. Осторожно понюхайте этот раствор. Что ощущаете? Вспомните, где вы применяете уксусную кислоту дома.
2. В одну пробирку с раствором уксусной кислоты добавьте несколько капель раствора лакмуса. Что наблюдаете? Затем нейтрализуйте кислоту избытком щелочи. Что наблюдаете? Запишите уравнение проведенной реакции.
3. В три оставшиеся пробирки с раствором уксусной кислоты добавьте: в одну-гранулу цинка, в другую несколько крупинок оксида меди (II) и подогрейте ее, в третью-кусочек мела или соды (на кончике шпателя). Что наблюдаете? Запишите уравнения проведенных реакций
Ход выполнения лабораторной работы:
1. Раствор имеет характерный резкий запах. Уксусная кислота в быту применяется в кулинарии для гашения соды, в пищевых целях, при мариновании овощей.
2.Сначала раствор окрасился в красный цвет. При добавлении в ту же пробирку избытка щелочи, получаем раствор синего цвета, т. к. реакция среды изменилась на щелочную.
CH3COOH + NaOH=CH3COONa + H2O
3. При добавлении цинка выделяются пузырьки водорода:
2CH3COOH + Zn=(CH3COO)2Zn + H2
При добавлении оксида меди он растворяется и образуется ярко-голубой раствор:
2CH3COOH + CuO=(CH3COO)2Cu+ H2O
При добавлении мела он растворяется и появляются пузырьки углекислого газа:
2CH3COOH + CaCO3=(CH3COO)2Ca + H2O + CO2
Лабораторная работа №5
Тема: Свойства жиров.
Цель: ознакомиться со свойствами жиров.
Ход работы
Опыт 1: свойства жиров.
В пробирку налить: воды, бензина, эфира, ацетона и др. жидкости, добавить кусочек жира или несколько капель растительного жира, все тщательно взболтать, наблюдать в какой пробирке растворился жир.
Опыт 2: доказательства непредельного характера жиров.
В одну пробирку налить2 мл. подсолнечного масла, во вторую поместить кусочек твердого жира (нагреть). К содержимому всех пробирок добавьте немного бромной воды. Что наблюдается?
Опыт 3: омыление жиров.
В фарфоровую чашечку поместить 3г. жиров, маргарина, или сливочного масла и прилейте 7 – 8 мл. раствора, содержащего в массовых долях 0,2 NаОН. Для ускорения реакции добавить 1 – 2 мл. этанола. Смесь кипятить 15 мин., помешивая стеклянной палочкой и добавляя воду до исходного уровня. Проверить омыление так: если при охлаждении на поверхности воды не всплывают капельки жира (омыление прошло).
Контрольные вопросы
Что такое омыление и для каких целей используется процесс омыления жиров? О чем свидетельствует осветление бромной воды?Лабораторная работа №6
Тема: Свойства глюкозы.
Цель: изучить свойства углеводов на примере глюкозы. Научится проводить качественные реакции.
1. В пробирку с 2-3 каплями раствора медного купороса (сульфата меди (II)) прилейте 2-3 мл раствора щелочи. Что наблюдаете? Затем добавьте в пробирку 2 мл раствора глюкозы и смесь перемешайте. Что наблюдаете? О чем свидетельствует этот опыт?
2. Нагрейте содержимое пробирки. Что наблюдаете? О чем свидетельствует этот опыт? Запишите уравнение проведенной реакции.
3. К 2 мл аммиачного раствора оксида серебра добавьте 1-2 мл раствора глюкозы и нагрейте смесь на пламени спиртовки. Старайтесь нагревать содержимое пробирки равномерно и медленно. Что наблюдаете? О чем свидетельствует этот опыт? Запишите уравнение проведенной реакции.
Ход выполнения лабораторной работы:
1. При добавлении щелочи образуется голубой осадок. Добавив глюкозу, осадок растворяется и цвет меняется на ярко синий. Это значит что глюкоза является представителем класса многоатомных спиртов.
2. При нагревании пробирки из предыдущего опыта, происходит исчезновение синего окраса и выпадение красного осадка. Это означает что глюкоза также относится и к альдегидам.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



