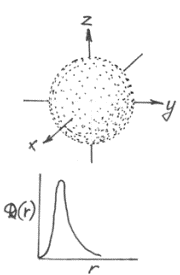
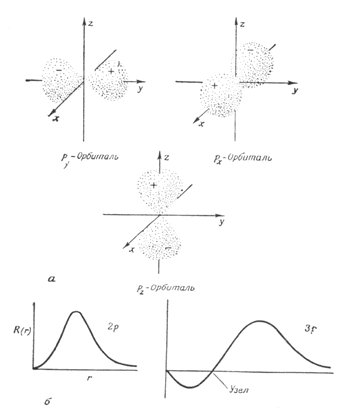
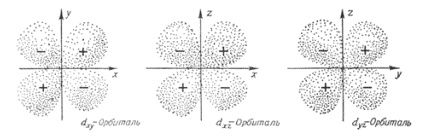
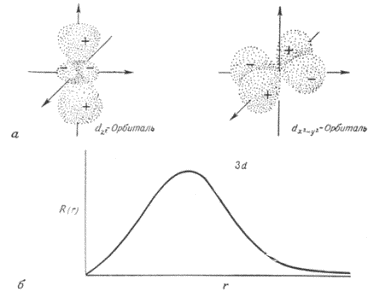
s, p,d-орбитали выглядят следующим образом
|
|
| |
| |
Экспериментально было показано, что электрон имеет еще и собственный момент количества движения, который был назван спином, квантовое число его определяющее может иметь только два значения +1/2 и -1/2. (^v)
Принципы заполнения атомных орбиталей.
Принцип минимума энергии. Электроны стремятся прежде всего занять ближние к ядру орбитали с наименьшей энергией (1s). Принцип Паули: в системе (атоме) не может быть двух электронов, характеризующихся одним и тем же набором четырех квантовых чисел. Или: на одной орбитали могут находиться только два электрона (они отличаются по спину). Правило Хунда: каждая система стремится иметь максимальный спин (максимальное число неспаренных электронов).В таком случае максимальное число электронов в слое с главным квантовым числом n равно 2n2. n=1 > 2e; n=2 > 8e; n=3> 18e; n=4 > 32e и т. д.
Сначала заполняются уровни (орбитали) с наименьшим n. Но существует еще правило Клековского - заполнение орбиталей происходит не по возрастанию n, а по возрастанию n+l, при одинаковых n+l сначала заполняется орбиталь с меньшим n. Ниже приводится картинка расположения уровней энергии для различных орбиталей.
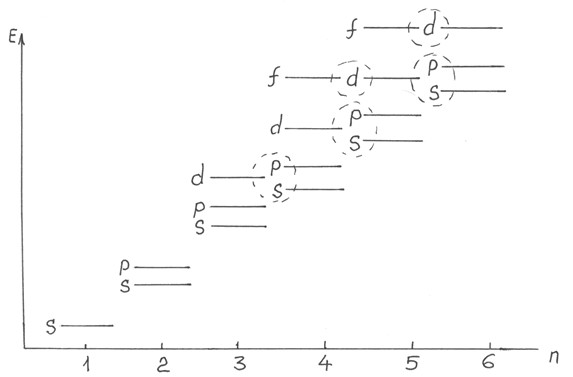
2 электрона -1s2; 3 эл. - 1s22s1; 4 эл. - 1s22s2; 5 эл. - 1s22s32p1, 6 эл. - 1s22s22p2, причем оба p-электрона неспаренные. Дальше до 18 электронов заполняются только s и p-орбитали. …3s23p6. Следующий 19-й электрон садится не на 3d-орбиталь, а на 4s, согласно вышеприведенному рисунку и правилу Клячковского: 4s n+l=4; 3d n+l=5; 4p n+l=5.
Таким образом, заполнение электронов происходит в следующем порядке:
1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f<5d<6p<7s<5f<6d<7p
Задание:
1. Определение состава атома по положению атома х. э. в ПС: определить заряд ядра; количество электронов, протонов и нейтронов у элементов 2, 11, 14, 27, 31, 40, 73, 94.
2. Электронные формулы атомов элементов:
внимательно изучить карту заполнения электронных формул; записать алгоритм; составить электронные форм, 25, 76, Fe +3, Cl-1, Ca+2.Алгоритм составления электронных формул:
1. Записать символ химического элемента.
2. Записать заряд ядра и количество электронных слоев, под которыми проставить число электронов.
3. Расписать каждый слой по облакам (условная запись).
4. Изобразить графически и определить валентные возможности атома х. э.
Критерии оценки, формы отчета: письменный отчет с правильным написанием электронных формул атомов и ионов.
Рекомендуемые источники информации: страница 19-26. Сборник задач и упражнений по химии (с дидактическим материалом): учебное пособие для студентов СПУЗ/ , . – 7-еизд. – М.: Издательский центр «Академия», 2010. – 304с.
Практическая работа № 3
Тема: Решение экспериментальных задач. (Испытание растворов кислот индикаторами. Взаимодействие металлов с кислотами, с оксидами металлов, с солями. Взаимодействие кислот с основаниями. Взаимодействие кислот с солями. Взаимодействие щелочей с солями. Разложение нерастворимых оснований. Взаимодействие солей друг с другом).
Цель: закрепление знаний по теме «Классификация неорганических соединений и их свойства», продолжить формирование умения определять химические вещества по характерным для них свойствам, составлять уравнения реакций, уравнивать их и давать названия реагентам и продуктам реакции.
Оборудование: ПСХЭ, таблицы: «Растворимость солей, кислот и оснований в воде» и «Анализ катионов анионов», набор реактивов и лабораторной посуды для проведения реакций.
Краткое содержание темы:
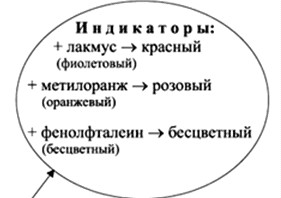
кислота
№ | Содержание работы и последовательность выполнения | Применяемое оборудование и материалы | Инструкционные указания и требования | ||||
11. | А) Получить гидроксид железа (III) | Кнопка (скрепка), NaOH, H2SO4 (1:5) | Составить план определения вещества. Записать уравнения реакций и наблюдения. | ||||
Б) Получить гидроксид цинка | Гранула цинка, раствор НСl, NaOH | ||||||
В) Получить хлорид | Гранула Al, растворы НСl, CuСl2 | ||||||
22. | А) Получить хлорид меди (II) | Cu (проволока), спиртовка, тигельные щипцы, CuО, раствор НСl | Составить план определения вещества. Записать уравнения реакций. Объяснить наблюдаемые явления. | ||||
Б) Получить сульфат цинка | ZnO, раствор Н2SO4 | ||||||
В) Получите нитрат кальция | СаО, раствор HNO3 | ||||||
33. | Определить какие вещества в пронумерованных пробирках. | Растворы солей и растворы веществ для проведения качественных реакций | Составить план определения вещества. Записать наблюдения. Уравнения реакций записать в молекулярном, полном и сокращённом ионном виде. | ||||
1 гр. | 2 гр. | 3 гр. | 4 гр. | 5 гр. | 6 гр. | 7 гр. | 8 гр. |
Хлорид натрия | Хлорид бария | Иодид калия | Карбонат калия | Карбонат натрия | Сульфат железа (III) | Сульфат меди (II) | Хлорид бария |
Карбонат калия | Хлорид железа (III) | Сульфат меди (II) | Хлорид магния | Хлорид железа (III) | Иодид калия | Хлорид натрия | Сульфат цинка |
Задание: 1.Переписать в тетрадь все пункты раздела "Содержание работы и последовательность выполнения".
2. Составить план определения веществ, провести качественные реакции, записать уравнения.
3. В выводе указать, какие вещества находятся в пронумерованных пробирках.
Критерии оценки, формы отчета: письменный отчет с планом определения вещества, с описанием наблюдений и записью уравнений реакции
Рекомендуемые источники информации:__________
Практическая работа № 4
Тема: Изготовление моделей молекул органических веществ.
Цель: закрепление знаний по теме «Основные понятия органической химии и теория строения органических соединений. Классификация органических соединений», продолжить формирование умения строить модели молекул органических веществ разных классов углеводородов (алканы, циклоалканы, алкены, алкины, спирты, карбоновые кислоты).
Оборудование: компьютер, CD-диск «Виртуальная химическая лаборатория»
Краткое содержание темы:
Для классификации огромного разнообразия органических соединений принято выделять в структуре их молекул углеродный скелет, который считается главной частью молекулы, и функциональные группы, которыми в значительной степени обуславливаются свойства различных классов соединений.
Углеродный скелет — это последовательность связанных между собой атомов углерода (и, в отдельных случаях, других атомов) в молекуле.
Функциональные группы — это все атомы или группы атомов, связанные с углеродным скелетом, за исключением атомов водорода.
Основная классификация органических соединений — это классификация по типу углеродного скелета. В соответствии с ним выделяют ациклические, циклические и гетероциклические соединения.
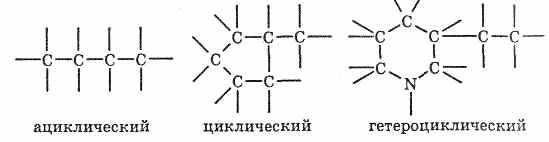
Атомы углерода могут образовывать между собой не только одну связь, а до трех. Двойные и тройные связи носят название кратных, а соединения, их содержащие, — ненасыщенных. Соответственно, соединения, содержащие только одинарные связи, называются насыщенными. Все соединения, содержащие в своем составе только атомы углерода и водорода (то есть не содержащие функциональных групп), называются углеводородами. В классификации по функциональным группам считается, что любое органическое соединение можно рассматривать как углеводород, в котором один или более атомов водорода замещены на функциональные группы – гидроксильная –ОН, карбонильная – С=О, карбоксильная - СООН
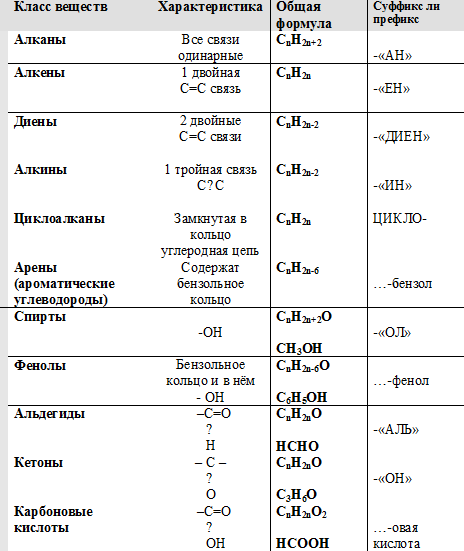
Задания по 4 вариантам:
В программе «Excel» создайте таблицу и внесите в неё общую информацию: название практической работы, фамилию и имя студента группы, цель работы. Для оформления отчета подготовьте следующую таблицу:№ опыта | Углеводород, ответы на вопросы | Фото модели | Оценка |
Ознакомьтесь с инструкцией и интерфейсом виртуальной лабораторной работы «Конструирование моделей молекул углеводородов и кислородсодержащих органических соединений». Сконструируйте модель молекулы этана (пропана, бутана, пентана). Рассмотрите модель молекулы в разном представлении: стрежневая, шаростержневая, Стюарта-Бриглеба. Результаты моделирования (фото) и свои ответы занесите в таблицу. Для фотографирования моделей воспользуйтесь кнопкой PrtSc на клавиатуре, для переноса изображения в таблицу используйте программу Paint. Сконструируйте модель молекулы пропана (бутана, пентана, гексана). Почему атомы углерода расположены не по прямой линии, как мы пишем в структурных формулах? Попробуйте повернуть атомы углерода в молекуле вокруг химической связи С-С. Что наблюдаете? Результаты моделирования (фото) и свои ответы занесите в таблицу. Сконструируйте модель молекулы этена (пропена, бутена-2, бутена-1). Попробуйте повернуть атомы углерода в молекуле вокруг химической связи С=С. Что наблюдаете? Результаты моделирования (фото) и свои ответы занесите в таблицу. Творческое задание: сконструируйте возможные пространственные структуры изомеров состава С4Н8 (С5Н10,С6Н12,С7Н14)Вещества назовите. К каким классам органических соединений они относятся? Результаты моделирования (фото) занесите в таблицу. Сконструируйте модель молекулы этанола С2Н5ОН (пропанола С3Н7ОН, муравьиной кислоты НСООН, уксусной кислоты СН3СООН). Результаты моделирования (фото) занесите в таблицу. Сохраните работу в папке «ПР №4. Группа № ____» на рабочем столе или передайте по сети на компьютер преподавателя.
Критерии оценки, формы отчета: таблица с ответами на вопросы и с фото составленных моделей.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |