Рекомендуемые источники информации:__________
Практическая работа № 5
Тема: Решение экспериментальных задач на идентификацию органических соединений. Цель: закрепление знаний о качественных реакциях на вещества; продолжить формирование умения проделывать качественные химические реакции на углеводы, спирты, альдегиды и карбоновые кислоты и распознавать вещества.
Оборудование: набор реактивов и лабораторной посуды и оборудования для проведения реакций.
Краткое содержание темы:
Для определения присутствия веществ, анионов, катионов используются качественные реакции. Проведя их можно подтвердить однозначно их наличие. Эти реакции широко используются при проведении качественного анализа, целью которого является определение наличия веществ или ионов в растворах или смесях. Здесь представлены основные качественные реакции на органические соединения и ионы.
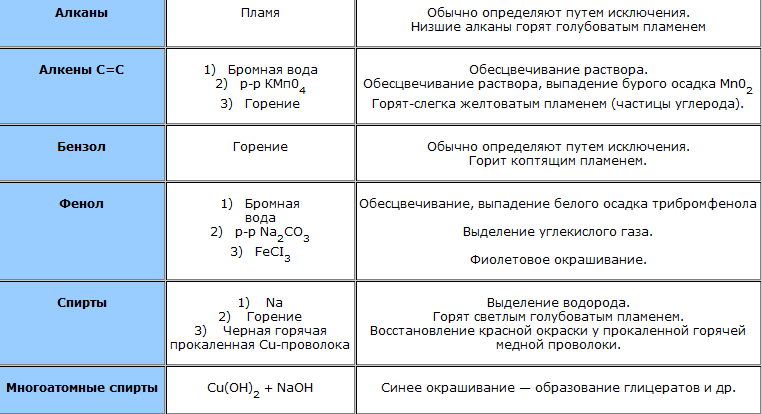
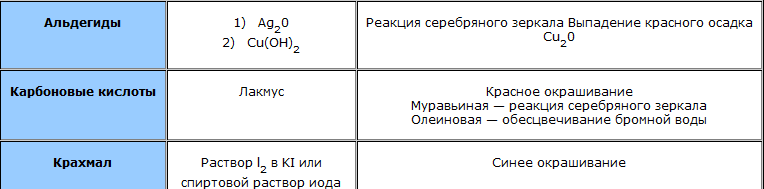
Задание: 1.Переписать в тетрадь все пункты раздела "Содержание работы и последовательность выполнения".
2. Составить план определения веществ, провести качественные реакции, записать уравнения.
3. В выводе указать, какие вещества находятся в пронумерованных пробирках.
№ | Содержание работы и последовательность выполнения | Применяемое оборудование и материалы | Инструкционные указания и требования |
11. | В трех пробирках даны растворы фенола, глюкозы и сахарозы. Определить с помощью характерных реакций каждое из веществ. | Растворы АgNО3, NН4ОН, сахарозы и глюкозы, С6Н5ОН, FeCl3, спиртовка, пробирки, спички | Записать наблюдения и уравнения реакций в тетрадь. |
22. | Даны три пробирки с глицерином, уксусной кислотой и ацетальдегидом. Определить с помощью характерных реакций каждое из веществ. | Мел, растворы АgNО3, СuSО4 , NаОН, NH4OH, глицерина, уксусной кислоты и ацетальдегида, спиртовка, пробирки, спички | Записать наблюдения и уравнения реакций в тетрадь. |
33. | Доказать, что в сыром картофеле и белом хлебе содержится крахмал. | Раствор йода, картофель, белый хлеб | Записать наблюдения и уравнения реакций в тетрадь. |
44. | Доказать, что в состав сахарозы и крахмала входит углерод. | сахароза, крахмал, спиртовка, спички, тигель | Записать наблюдения и уравнения реакций в тетрадь. |
Критерии оценки, формы отчета: письменный отчет с планом определения вещества, с описанием наблюдений и записью уравнений реакции
Рекомендуемые источники информации:
Практическая работа № 6
Тема: Распознавание пластмасс и волокон.
Цель: обобщить знания о свойствах ВМС (пластмассы, волокна); продолжить формирование умения сравнивать, анализировать и выявлять причинно-следственные связи при распознавании веществ.
Оборудование: коллекции и образцы «Пластмассы», «Волокна»; таблицы для определения веществ ВМС, набор реактивов и лабораторной посуды для проведения реакций.
Краткое содержание темы:
Пластмассы - материалы на основе высокомолекулярных веществ (полимеров). Помимо полимеров пластмассы, как правило, содержат и другие компоненты: пластификатора, наполнители и т. п. Наличие полимеров в составе пластмасс обусловливает ряд специфических свойств этих материалов. Пластмассы подразделяются на термопластичные, изготовляемые на основе линейных полимеров, и термореактивные - на основе полимеров с пространственной структурой. Первые при нагревании приобретают пластичность, а при охлаждении вновь возвращаются в исходное состояние; вторые, будучи отверждены, при нагревании не переходят в пластическое состояние. К пластмассам, применяемым в строительных конструкциях, относятся стеклопластики, оргстекло, винипласты, пенопласты, сотопласты, древесные пластики, синтетические клеи и др.
Волокна – протяженные, гибкие, прочные тела с малыми поперечными размерами, пригодные для изготовления пряжи и текстильных изделий.
Волокна делят на натуральные (природные) и химические. Натуральные волокна могут быть растительного или животного происхождения. Химические волокна в свою очередь подразделяют на искусственные и синтетические.
Природные волокна: Волокно растительного происхождения – хлопок, лен.
Хлопковое волокно получают из субтропического растения – хлопчатника. Состав хлопкового волокна:
- целлюлоза – 96%
- пентозан – 1 – 2 %
- жиры и воска – 1%
- азотосодержащие и белковые вещества – 0,3%
- зола – 0,2 – 0,4%
Хлопковое волокно легкое, достаточно прочное, мягкое, гигроскопичное. Волокна растительного происхождения формируются на поверхности семян (хлопок), в стеблях растений (тонкие стеблевые волокна – лён, рами; грубые – джут, пенька из конопли, кенаф и др.) и в листьях (жесткие листовые волокна, например, манильская пенька (абака), сизаль).
Волокна животного происхождения – шерсть и шелк.
Шелк вырабатывают многочисленные гусеницы и пауки.
Шерсть – волокна волосяного покрова овец, коз, верблюдов и других животных.
Искусственные волокна:
Наибольшее значение среди искусственных волокон занимают ацетатное и вискозное волокна, получаемые из древесной целлюлозы. Целлюлозу переводят в диацетат целлюлозы, действуя на нее уксусной кислотой.
Синтетические волокна: изготовляют из синтетических высокомолекулярных соединений: полиамидные (капрон, нейлон), полиакрилонитрильные, полиэфирные (лавсан), перхлорвиниловые, полиолефиновые.
К волокнам минерального происхождения относятся асбесты (наиболее широко используют хризолит-асбест)
Задание: 1.Переписать в тетрадь все пункты раздела "Содержание работы и последовательность выполнения".
2. Составить план определения веществ, провести качественные реакции, записать уравнения.
3. В выводе указать, какие вещества находятся в пронумерованных пробирках.
п/п | Содержание работы и последовательность выполнения | Применяемое оборудование и материалы | Инструкционные указания и требования. |
11. | Даны коллекции пластмасс и волокон; рассмотреть и сравнить внешние признаки веществ. | Коллекции пластмасс, волокон. | Записать в тетрадь наблюдения. |
22. | В 4 пакетах даны образцы волокон и пластмасс; опытным путем определить каждое вещество с помощью данных таблицы (внешний вид, отношение к нагреванию и действию кислот, органических растворителей). | Пакеты с образцами, щипцы, спички, химические реактивы | Записать наблюдения и выводы в тетрадь. |
Критерии оценки, формы отчета: письменный отчет с планом определения вещества, с описанием наблюдений
Рекомендуемые источники информации:
Лабораторная работа № 1
Тема: ________________
Цель:_________________
Оборудование:________
Краткое содержание темы (основные понятия, формулы и проч., необходимые для выполнения работы)________________
Образец (алгоритм) выполнения задания:_______________
Задание (я) (варианты по уровню сложности)_______________
Критерии оценки, формы отчета______________
Требования к оформлению реферата, выступлению, презентации ____________________
Рекомендуемые источники информации:__________
Лабораторная работа № 2
Тема: Типы химических реакций.
Цель: продолжить формирование умений определять типы химических реакций по уравнению реакции, составлять уравнения реакций, уравнивать их и давать названия реагентам и продуктам реакции.
Оборудование: ПСХЭ, таблица «Растворимость кислот, оснований и солей в воде», набор реактивов и лабораторной посуды для проведения реакций.
Краткое содержание темы:
Схемы химических реакций.
Реакции соединения – это реакция, при которой из двух или нескольких простых веществ образуется одно сложное вещество: А + В = АВ Реакция разложения – это реакция, при которой одно сложное вещество распадается на два или несколько простых или сложных веществ: АВ = А + В Реакция замещения – это реакция, при которой атомы простого вещества замещают атомы в сложном веществе: А + ВС = АС + В Реакция обмена – это реакция, при которой два сложных вещества обмениваются своими составными частями: АВ + СД = АД + СВЗадание:
№ | Содержание работы и последовательность выполнения | Применяемое оборудование и материалы | Инструкционные указания и требования |
11. | Получить гидроксид меди (II) и образовавшийся осадок осторожно нагреть. | Растворы СuSО4, NaOH, спиртовка | Записать наблюдения и уравнения реакций в тетрадь. Подписать тип химической реакции. |
22. | В раствор медного купороса опустить железный гвоздь. | Раствор СuSО4, железный гвоздь. | Записать наблюдения и уравнения реакций в тетрадь. Подписать тип химической реакции. |
33. | В пробирку прилить 1-2 мл раствора NaС1, добавить по каплям раствор АgNОз до выпадения осадка. | Растворы NаС1 и АgNОз | Записать наблюдения и уравнения реакций в тетрадь. Подписать тип химической реакции. |
44. | Взять порошок цинка, растереть по фильтровальной бумаге и придерживая тигельными щипцами поджечь ее с краю. | порошок цинка, фильтровальная бумага, тигельные щипцы | Записать наблюдения и уравнения реакций в тетрадь. Подписать тип химической реакции. |
Критерии оценки, формы отчета: письменный отчет с описанием наблюдений и записью уравнений реакции, с указанием типа химической реакции.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



