Рекомендуемые источники информации:
Лабораторная работа № 5
Тема: Получение и свойства альдегидов (Окисление спирта в альдегид. Растворение глицерина в воде и взаимодействие с гидроксидом меди(II). Реакция серебряного зеркала альдегидов и глюкозы).
Цель: закрепление знаний по теме «Химические свойства альдегидов», развитие умений работать с химическими веществами и оборудованием, записывать уравнения реакций, умение наблюдать и делать выводы.
Оборудование: набор лабораторного оборудования и реактивов для выполнения задания
Краткое содержание темы:
Альдегидами называются сложные вещества, состоящие из углеводородного радикала и функциональной группы
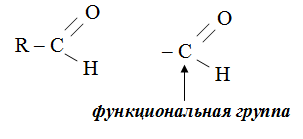
Важнейшими представителями альдегидов являются формальдегид и ацетальдегид.
Формальдегид – газ с резким запахом, единственный газообразный представитель альдегидов. Хорошо растворяется в воде. Водный раствор его называют формалином. Но! Формалин опасен для здоровья. Он способен вызывать раздражение слизистых тканей и действует на нервную систему.
Ацетальдегид – жидкость с характерным запахом зеленой листвы. Хорошо растворяется в воде. Но! Очень токсичен. Он способен соединяться с белками и подавлять дыхательные процессы в клетках.
Реакция окисления осуществляется по функциональной группе. В результате альдегиды способны превращаться в соответствующие органические кислоты. Окислителями служат KMnO4, K2Cr2O7, оксиды и гидроксиды меди и серебра.
а) окисление формальдегида аммиачным раствором оксида серебра.
II. Реакции окисления
1. Реакция серебряного зеркала – качественная реакция на альдегидную группу:
R-CH=O + 2[Ag(NH3)2]OH > R-C=O +2Agv +3NH3 + H2O
¦
ONH4 (соль аммония)
или упрощённо R-CH=O + Ag2O NH3> R-COOH + 2 Agv
карбоновая кислота
окисление ацетальдегида гидроксидом меди (II)
2. Окисление гидроксидом меди(II):
R-CH=O + 2Сu(OH)2 t > R-COOH + Cu2O +2H2O
голубой красный
Получение альдегидов.
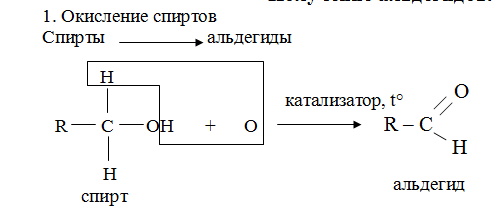
1. Окисление спиртов
Спирты альдегиды
2. Ацетальдегид получают гидратацией ацетилена (реакция )

3. Окисление этилена
Задание:
№ | Содержание работы и последовательность выполнения | Применяемое оборудование и материалы | Инструкционные указания и требования |
11. | Пробирку держать вертикально, поместить в нее 3-4мл этилового спирта. Накалить медную спираль в пламени до черного налёта и быстро опустить в пробирку несколько раз. | Пробирка, спираль медная, раствор этилового спирта. | Записать наблюдения и уравнения реакций |
22. | В пробирку внести по каплям 2мл раствора нитрата серебра и аммиачный раствор, добавить 2мл. раствора альдегида, смесь нагреть на слабом огне. | Пробирка, спиртовка, растворы альдегида и АgNО3, NH4OH. | Записать наблюдения и уравнения реакций. |
33. | В пробирку внести 2мл. конц. раствора щелочи и по каплям раствор СиSО4, прилить 2 мл раствора альдегида до образования светло-синего раствора. Смесь осторожно нагреть. | Пробирка, раствор альдегида, СиSО4, NaOН | Записать наблюдения и уравнения реакций |
Критерии оценки, формы отчета: письменный отчет с описанием наблюдений и записью уравнений химических реакций.
Рекомендуемые источники информации:
Лабораторная работа № 6
Тема: Свойства карбоновых кислот и углеводов (Свойства уксусной кислоты, общие со свойствами минеральных кислот. Взаимодействие глюкозы и сахарозы с гидроксидом меди(II). Качественная реакция на крахмал).
Цель: формирование умений проводить реакции, отражающие общие и специфические химические свойства представителей класса карбоновых кислот и углеводов.
Оборудование: набор лабораторного оборудования и реактивов для выполнения работы
Краткое содержание темы:
- органические соединения, содержащие одну или несколько карбоксильных групп
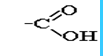 или (СООН),
или (СООН),
связанных с углеводородным радикалом
Углеводы – группа природных кислородсодержащих органических соединений – получили своё название в связи с тем, что вначале казалось, будто бы все эти соединения имеют состав, выражаемый в общем виде формулой – Сn(Н2О)m (Приложение1, слайд 5), т. е. они как бы состояли из углерода и воды. Углеводы — полигидроксиальдегиды и кетоны. Углеводы разнообразны по структуре (табл. 17). В типичных случаях их молекулы содержат прямую насыщенную цепь из пяти или шести углеродных атомов, один из которых окислен до альдегидной или кетонной группы, а остальные имеют гидроксильные заместители.
Углеводы в зависимости от их строения можно подразделить на моносахариды, дисахариды, полисахариды. (Приложение1, слайд 4)
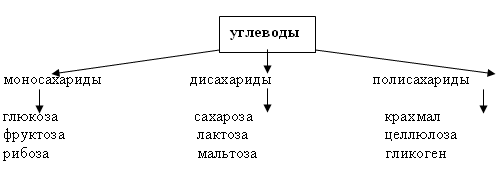
дезоксирибоза
химическое строение молекулы глюкозы можно выразить такой формулой: (Приложение 1, слайд 7)
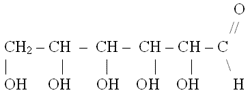
На основании результатов выполненных лабораторных опытов они делают вывод, что глюкоза – многоатомный спирт и альдегид одновременно, или точнее многоатомный альдегидоспирт. На основании выводов практической работы записать структурную формулу молекулы глюкозы (студент у доски записывает структурную формулу глюкозы).
Задание:
№№ п/п | Содержание работы и последовательность выполнения работы | Применяемое оборудование и материалы | Инструкционные указания и требования |
11. | В пробирку поместить каплю раствора уксусной кислоты. Добавить каплю раствора метилового оранжевого | Пробирка, растворы СНзСООН и метилового оранжевого | Проделать опыт, записать в тетрадь наблюдения |
22. | В пробирку поместить 2 капли раствора уксусной кислоты. Добавить стружек Мg и поднести горячую лучину к отверстию пробирки | Пробирка, р-р СНзСООН, магний, лучина | Проделать опыт, записать в тетрадь уравнение реакции наблюдения |
33. | В пробирку налить 2-3 капли р-ра уксусной кислоты и добавить несколько крупинок соды | Пробирка, р-р СНзСООН, магний, лучина, р-р порошок соды | Проделать опыт, записать в тетрадь уравнение реакции и наблюдения |
44. | В пробирку налить 2-3 капли р-ра уксусной кислоты и добавить р-р NаОН | Р-ры СНзСООН и NаОН | Проделать опыт, записать в тетрадь уравнение реакции |
65. | Взаимодействие с гидроксидом меди(II): к 1 мл раствора глюкозы добавить 1 мл щелочи NaОН и 2-3 капли раствора СиSО4. | растворы NаОН, СиSО4 и глюкозы | Записать наблюдения и уравнения реакций в тетрадь. |
66. | Качественная реакция на крахмал: к раствору крахмала добавить 2-3 капли р-ра йода. | раствор крахмала и йода (спиртовой) | Записать наблюдения и уравнения реакций в тетрадь. |
Критерии оценки, формы отчета: письменный отчет с описанием наблюдений и записью уравнений химических реакций.
Рекомендуемые источники информации:
Лабораторная работа № 7
Тема: Свойства белков (Растворение и осаждение белков в воде. Обнаружение белков в молоке. Цветные реакции белков. Горение птичьего пера и шерстяной нити. Денатурация раствора белка куриного яйца спиртом, растворами солей тяжелых металлов и при нагревании).
Цель: закрепление знаний по теме «Строение и химические реакции белков»; продолжить развитие умений работать с химическими веществами и оборудованием, наблюдать и делать выводы.
Оборудование: раствор куриного белка, набор лабораторного оборудования и реактивов для выполнения работы
Краткое содержание темы:
Белки – это природные полимеры, состоящие из альфа – аминокислот
2.связанны аминокислоты пептидными связями С-N.
3. Относительные молекулярные массы белков могут достигать нескольких миллионов т. к. число остатков аминокислот, входящих в пептидную цепь бывает очень большим.
4.Состав белков: C, Н, О,N, а также S, а иногда Р, Fe и некоторые другие элементы.
5.Белки природные полимеры т. к. образуются в природе и являются высокомолекулярными соединениями.
В дополнение к вышесказанному:
Белки образуются из остатков 20 различных аминокислот, из которых 8 незаменимые т. е. не синтезируются в организме, поэтому их поступление в организм обязательно вместе с пищей животного происхождения.
1 вариант. 2 вариант
а)CH3-CH-СOOH а) CH3-CH2-CH-СOOH
NH2 NH2
Качественные реакции на белок.
1.Гидролиз
Распад белков под действием воды на аминокислоты.
2.Денатурация – необратимое свертывание белка
Причины денатурации:
- температура, УФ – лучи, радиация, действие химических веществ.
Качественные реакции на белок.
3.Цветные реакции
а) биуретовая реакция: белок + CuSO4 +NaOH>красно–фиолетовое окрашивание
б) ксантопротеиновая: белок + конц. HNO3>желтый цвет.
Простые белки (протеины) –состоят из остатков альфа – аминокислот. Сложные белки (протеиды) – состоят из остатков альфа – аминокислот и небелковых веществ.Названия некоторых белков:
Белок яйца – альбумин
Белок молока – казеин
Белок мышц – миозин
Белок крови – гемоглобин

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |