Для улучшения структуры межфазной поверхности часто из биомассы формируют специальной формы гранулы, называемые «лепесток». Так поступают при экстракции липидов (жиров) из микробной биомассы, Для этого сначала просто гранулируют био-массу, получая сферические гранулы. Затем эти гранулы пропус-кают через вальцы, получая сплющенные лепешки толщиной 0,2—0,3 мм — «лепестки». Далее уже эти «лепестки» загружают в аппарат для экстрагирования, и при этом обеспечивается более эффективная массоотдача.
2. ЭКСТРАГИРОВАНИЕ «СУПЕРКРИТИЧЕСКИМИ» ЖИДКОСТЯМИ
При выделении липидов и всякого рода неустойчивых, лабильных соединений, проводя экстрагирование, следует учитывать дальнейшие операции выделения. Поэтому часто используют лег-кокипящие соединёния — спирт, нефрас, гексан, ацетон, которые в дальне?шем удаляют путем выпаривания.
Но для выпаривания этих соединений требуются относительно высокие температуры, которые могут повлиять на качество выделяемых биопродуктов. При этом также необходимы затраты энергии на испарение экстрагентов и их последующую конден-сацию.
Кажется очевидным, что для решения этих проблем следовало бы брать в качестве растворителей жидкости, имеющие более низкую температуру кипения. Одной из таких жидкостей является диоксид углерода. Правда, при атмосферном давлении температура его кипения довольно низка (ниже —50 °С). Но с повышением давления температура повышается: при давлении 7,3 МПа, например, температура кипения составляет +31 °С.
Обычно плотности газа и жидкости резко различаются. Например, при +10 °С плотность жидкости С02 составляет 0,86 г/см\ а газа — 0,14 г/см3. При 20 °С — соответственно 0,77 и 0,19 г/см3, а при 30 °С — 0,59 и 0,35. А вот при 31,1 °С и давлении 7,3 МПа плотность жидкости и газа становится равной. Если и температу-ра, и давление выше своих критических значений, вещество обла-дает свойствами, промежуточными между жидкостью и газом. Эта фаза — фаза «суперкритической» жидкости.
Путем повышения давления газ при любой температуре до критической точки А (31,1 °С) можно превратить в жидкость. И наоборот, газ при любом давлении ниже критического (7,3 МПа) можно превратить в жидкость путем снижения температуры.
Физические и диффузионные свойства «суперкритических» жидкостей находятся в диапазо?е между значениями соответствующих свойств газов и истинных жидкостей и обычно весьма бла-гоприятны для их применения в качестве экстрагентов. В частности, очень низка их вязкость, что снижает затраты на перекачивание. Кроме того, при работе на границе области критических значений температуры и давления можно путем небольших температурных воздействий переводить «суперкритические» жидкости в газы и обратно в жидкости.
Существуют и другие вещества, имеющие критические температуры в областях, близких к нормальной температуре (табл. 15.1).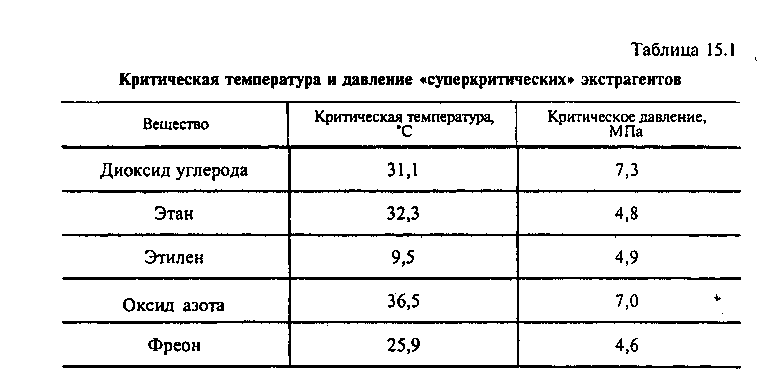
Таким образом, процесс выделения продукта проводится при обынной температуре и не требует выпарки для разделения продукта и растворителя-экстрагента.
«Суперкритические» жидкости являются неполярными растворителями и лучше растворяют неполярные вещества. Ионизированные вещества в «суперкритических» жидкостях практически нерастворимы.
Хорошо растворяются: углеводороды и растворимые в жирах органические соединения — парафины, многие эфиры, лактоны и глицериды; многие лекарства, кофеин, никотин, стероиды и алка-лоиды, вкусовые и ароматические компоненты.
Интересно, что выделение может быть даже из водных растворов
Общая оценка процесса экстрагирования «суперкритическими жидкостями» такова.
Преимущества:
высокая энергетическая эффективность;
низкие температуры;
нетоксичные и недорогие растворители (экстрагенты);
низкая вязкость, высокая диффузионная способность;
силой растворителя можно управлять.
Недостатки'.
необходимо оборудование высокого давления;
относительно низкая сила растворителя;
плохие растворители для полярных соединений;
недостаточно данных для надежного проектирования (все нуж-но проверять экспериментально).
3. ЖИДКОФАЗНАЯ ЦЕНТРОБЕЖНАЯ ЭКСТРАКЦИЯ
Жидкофазная экстракция наиболее часто используется в производствах антибиотиков, в том числе при производстве наиболее крупнотоннажного из них — пенициллина. Блок-схема технологии антибиотика, как много там стадий жидкофазной экстракции: сначала пенициллин из водной фазы переводят в органическую (бутилацетат), затем из органической фазы — опять в водную, затем опять в органическую и т. д.
Антибиотик в неионизированной форме хорошо растворяется в некоторых органических растворителях (бутилацетате или амилацетате). Растворимость его в таких растворителях почти в 100 раз больше, чем в воде. Диссоциированный же анион не имеет столь хорошей растворимости в органической фазе.
Основной характеристикой процесса экстракции «жидкость—жидкость» является коэффициент распределения Кр.
Конечные значения равновесной концентрации продукта в рафинате и степени извлечения зависят от коэффициента распределения, соотношения объемов фаз и не зависят от коэффициента массоотдачи.
Проводя экстракцию при рН 2,0, мы достигаем хорошего коэффициента распределения.
Процесс экстракции должен осуществляться в такой последовательности:
подкисление водного раствора пенициллина;
добавление к нему экстрагента — органической фазы;
диспергирование фазы для обеспечения наибольшей поверхности раздела фаз;
интенсивное перемешивание для осуществления процесса собственно экстракции, причем время протекания процесса должно быть настолько малым, чтобы не успело проявиться разрушающее действие низких значений рН на водные растворы пенициллина;
после завершения процесса экстракции — разделение (редиспергирование) водной и органической фаз.
Все эти операции быстро можно провести, только если:
процесс проводится в непрерывном режиме;
в качестве аппарата используется центробежный экстрактор.
Вот почему в биотехнологических процессах экстракция осуществляется в центробежных экстракторах, напоминающих по конструкции центробежные сепараторы. В них происходит эмульгирование фаз путем смесителя-инжектора, экстракция в центро-бежном поле и затем деэмульгирование органических фаз. Кроме того, в многоступенчатых центробежных экстракторах обеспечи-вается еще противоточное движение фаз, создающее равномерную по ходу потока движущую силу массоотдачи.
Преимущества таких экстракторов — высокая производитель-ность и возможность работы с лабильными продуктами.
Недостатки: высокие энергетические затраты, возможность проскока частично эмульгированного елоя («третьего слоя»), что увеличивает потери целевого продукта.
Вопросы для повторения
1. Назовите термины, обозначающие основные материальные компоненты, участвующие в процессе экстрагирования, — жидкую и твердую фазу до и после процесса экстрагирования.
2. В чем различие между одноступенчатым и многоступенчатым процессами экстрагирования биомассы микроорганизмов?
3. Каковы способы организации противотока и увеличения средней движушей силы при экстрагировании биомассы микроорганизмов?
4. В чем заключается метод создания эффективной межфазной повсрхности при экстрагировании компонентов из биомассы микроорганизмов?
5. Что дает экстрагирование «суперкритическими» жидкостями?
6. Назовите вещества, используемые в качестве экстрагентов биомассы — «су-перкритических» жидкостей, и параметры их критических точек по температуре и давлению.
7. Какие вещества можно экстрагировать, используя «суиеркритические» жид-кости?
8. Расскажите об особенностях жидкофазной экстракции лабильных продук-тов микробиологического синтеза.
9. Почему при экстракции пенициллина используют низкие значения рН?
10. Почему для экстракции пенициллина используют центробежные экстрак-торы?
Лекция № 12 Сорбционные методы выделения продуктов биосинтеза
Основные понятия Ионный обмен Адсорбция микропористыми сорбентами Хроматография Биосорбция Иммуносорбция
Сорбционные методы представляют собой выделение растворенного в жидкой фазе компонента с помощью твердофазного сорбента. В какой-то мере этот процесс является по смыслу про-тивоположным экстрагированию, где, наоборот, полезный компо-нент локализован в твердой фазе, а в процессе экстракции перехо-дит в жидкую (экстрагент). При сорбции же растворенное веще-ство из раствора переводится в твердую фазу (сорбент),
На этом, однако, сорбционный метод не заканчивается. Да-лее следует отделение твердой фазы от рафината — раствора, из которого извлечен растворенный компонент, и последующая десорбция этого компонента из сорбента в новую жидкость, отлича-ющуюся от исходного раствора какими-то свойствами или просто более чистую, не содержащую посторонних примесей в исходном растворе. Эта вторая операция (десорбция) уже точно практически ничем не отличается от экстрагирования, разве что при экстрагировании твердой фазой является сама биомасса, а при десорбции — промежуточный рабочий агент, специально вносимый в жидкую фазу извне. Твердая фаза — «временное пристанище» растворенного вещества.
Рассмотрим 4 различных модификации сорбционных методов:
ионный обмен;
адсорбция микропористыми сорбентами;
хроматография;
биосорбция.
Во всех случаях мы будем подразумевать, что сорбционный метод включает в себя как собственно сорбцию, так и десорбцию, и рассматривать метод вьщеления как совокупность этих двух процессов.
2. ИОННЫЙ ОБМЕН
Ионообменный метод основан на способности специальных сорбентов — ионообменных смол — сорбировать биологически активные
вещества, имеющие ионную природу (т. е. являющиеся кислотой,
основанием или солью), благодаря эквивалентному обмену между
ионами вещества, находящегося в растводе, и ионами сорбента.
Ионообменные смолы, или иониты, представляют собой синтетические высокомолекулярные органические вещества, практически нерастворимые в воде. Они содержат обменные ионы, один из ко-торых связан с твердым носителем и называется фиксированным, или анкерным ионом. С ним электростатически связан противоположно заряженный ион, называемый подвижным ионом, или противоионом.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 |




