Непрерывное нагревание среды может быть осуществлено без прямого контакта с теплоносителем в трубчатом, пластинчатом или спиральном теплообменнике, который встроен в стерилизатор или стоит перед ним. Но чаще всего среда нагревается до нужной температуры в течение нескольких секунд прямым введением (инжектированием) перегретого пара (100-1400С), полученного в паровых контактных нагревателях.
Для стерилизации небольших объемов растворов используют фильтрование через специальные фильтры-мембраны, задерживающие бактериальные клетки, а иногда и вирусы. Обычно этот способ используют для стерилизации растворов веществ, неустойчивых к нагреванию, а так же конечных продуктов (например лекарственных веществ белковой природы).
Твердые сыпучие среды, используемые для поверхностного способа культивирования, стерилизуют паром, иногда инфракрасными и ?-лучами. Стерилизация твердых питательных сред водяным паром сопровождается, как правило, комкованием частиц среды. Поскольку компоненты твердых питательных сред (жмыхи, шелуха семян, опилки) обладают низким коэффициентом теплопроводности, то комкование препятствует нормальному течению процесса стерилизации, особенно в глубине комков. Для достижения необходимого эффекта обычно используют перегретый (острый) пар (до 1400 С), однако это не обеспечивает абсолютной стерильности Однако он вполне достаточен для проведения многих процессов, таких как получение ферментов или органических кислот.
Подготовка воздуха для биотехнологических производств
Одной из важных задач биотехнологии является получение большого количества стерильного воздуха. В наибольших масштабах стерильный воздух применяется в процессах культивирования для аэрации. Его также используют для вентиляции участков цехов так называемой стерильной зоны, где в асептических условиях проводят, например, последние стадии очистки и фасовки готового продукта. В атмосферном воздухе, наряду с инертными газами, азотом, кислородом, диоксидом углерода, содержатся пары воды и мелкодисперсные частицы. В состав дисперсных частиц, наряду с частицами пыли, копоти, входят клетки и споры микроорганизмов как в свободном, так и в сорбированном на пылевых частицах виде.
Температура и влажность наружного воздуха, количество в нем пылинок и микроорганизмов непостоянны и зависят от времен года (микроорганизмов летом в 10 раз больше, чем зимой), погодных условий - наибольшее количество пыли и, соответствено микроорганизмов приходится на сухую ветреную погоду, геогра - фического расположения предприятия, высоты забора воздуха т. д. Особенно много микробов у поверхности земли, с высотой концентрация их убывает и становится постоянной на уровне около 30 м над землей.
Очистку воздуха можно осуществить принципиально разными методами, основаными либо на уничтожении микроорганизмов, либо на удалении их. Одним из самых эффективных способов стерилизации воздуха, является облучение ультрафиолетовыми лучами. Этот метод используется для обеззараживания воздуха в боксах и технологических помещениях.
Отечественным и зарубежным опытом показано, что технически и эконо-мически оправданным в промышленности является способ очистки больших количеств воздуха на фильтрах с помощью волокнистых и пористых материалов. Таким путем удается получить воздух со степе чистоты 99,9999%. Взвешенные в воздухе частицы задерживаются волокнистым материалом благодаря инерционному и диффузионному механизмам осаждения. В общих чертах механизм инерционного осаждения основан на том, что когда воздушный начинает обтекать нить волокна на своем пути, взвешенные в этом потоке частицы движутся по инерции, отклоняются от потока воздуха и осаждаются на волокне. Эффект инерционного осаждения высок на сравнительно грубых волокнах для относительно крупных частиц и высоких скоростей воздуха. Малые частицы способны к броуновскому движению. Движущиеся вблизи волокна частицы диффундируют в случайных направлениях и могут задерживаться на поверхности волокон. Этот эффект осаждения увеличивается с уменьшением диаметра частицы, диаметра волокна и скорости воздуха.
Если очищенный воздух используют в процессе поверхностного культивирования то он должен быть дополнительно кондиционирован до необходимой температуры и влажности.
Лекция №3 Подготовка и наработка продуцента для биотехнологических производств.
Получение накопительных культур. Подготовка продуцентов. Характеристика некоторых видов микроорганизмов.4.Популяционная устойчивость биологических объектов
1. Главным звеном биотехнологического процесса, определяющим его сущность, является клетка. Именно в ней синтезируется целевой продукт. По образному выражению (1985), клетка представляет собой миниатюрный химический завод, работающий с колоссальной производительностью, с предельной согласованностью и по заданной программе. В ней ежеминутно синтезируются сотни сложнейших соединений, включая гигантские биополимеры, в первую очередь белки.
Основа современного биотехнологического производства — микробиологический синтез, т. е. синтез различных веществ с помощью микроорганизмов.
Независимо от природы объекта, начальным этапом биотехнологической разработки является получение чистых культур клеток и тканей (рис. 1).
К микроорганизмам относятся все прокариоты — бактерии,, актиномицеты, риккетсии и часть эукариот — дрожжи, нитчатые грибы, простейшие и водоросли. Их общее свойство — малые размеры, вследствие чего они видимы лишь в микроскоп. В настоящее время известно более 100 тыс. различных видов микроорганизмов. При столь большом разнообразии микроорганизмов как провести правильный подбор именно тех форм, продукция которых нас интересует? 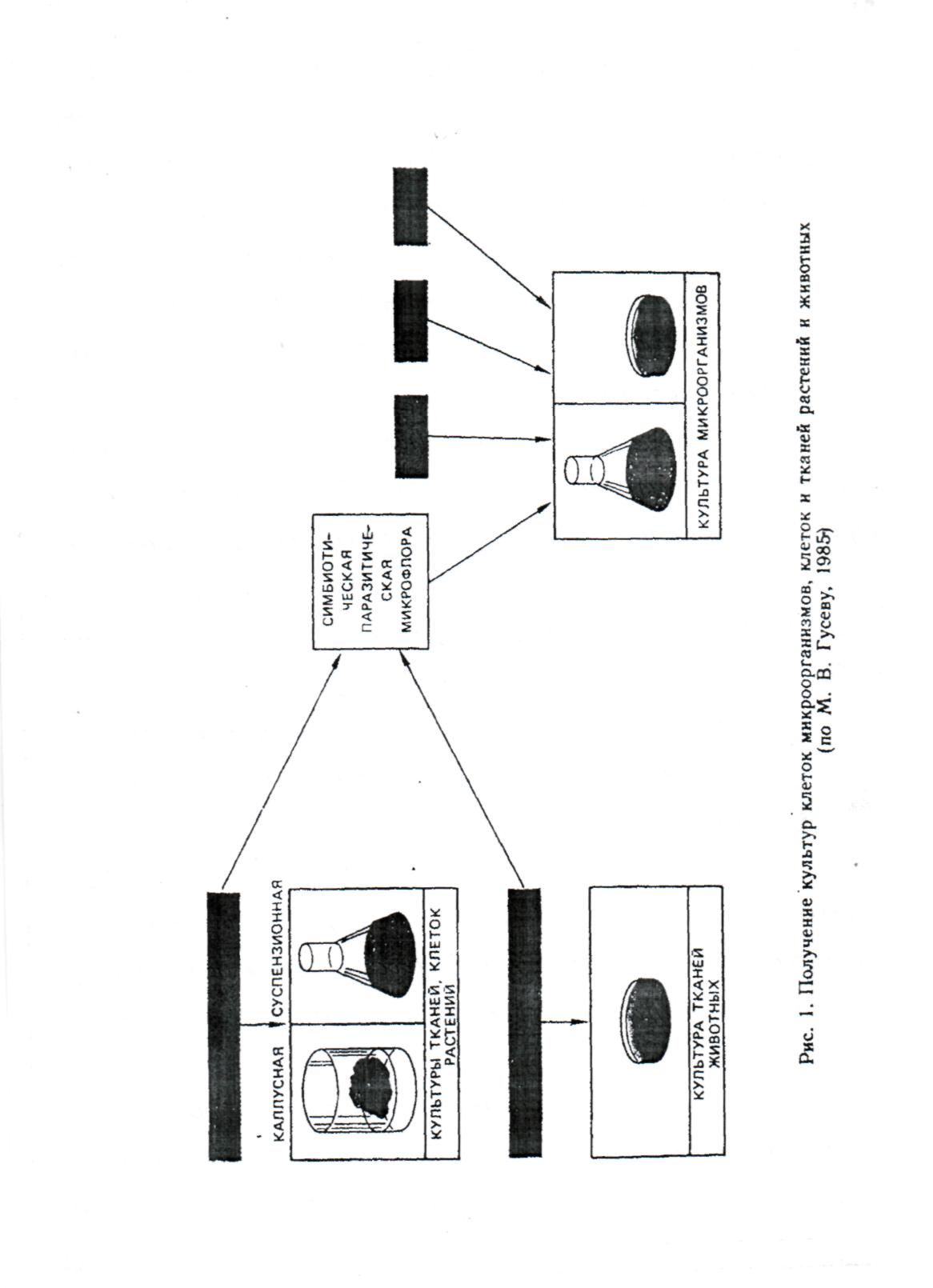
Для решения подобных задач проводится выделение микроорганизмов. Отбираются пробы из мест, где обитание того или иного продуцента наиболее вероятно. Применительно к углеводородокисляющим микроорганизмам таким местом может быть почва возле бензоколонок, винные дрожжи обильно встречаются на винограде, анаэробные целлюлозоразлагающие и метанобразующие микроорганизмы в больших количествах обитают в рубце жвачных животных. Образцы проб вносят в жидкие питательные среды специального состава. Эти среды называют элективными: в них путем варьирования различных факторов создаются избирательные условия для преимущественного развития интересующего нас продуцента. К этим факторам относятся источники энергии, углерода, азота, значения рН, температура, осмотическое давление и т. д. Для накопления продуцента холестериноксидазы используют среды с холестерином в качестве единственного источника углерода; углеводородокисляющих микроорганизмов — среды с парафинами; продуцентов протеолитических или липолитических ферментов — среды, содержащие белки или липиды. Так получают накопительные культуры микроорганизмов.
Следующий этап — выделение чистых культур. Для этого используют плотные питательные среды, на которые засевают образцы проб из накопительных культур. Отдельные клетки микроорганизмов на плотных питательных средах образуют изолированные колонии, при их последующем пересеве получаются чистые культуры продуцента, состоящие из популяций клеток одного вида.
Существует и другой путь подбора микроорганизмов — из имеющихся коллекций микроорганизмов. При этом руководствуются опытом, накопленным в результате изучения физиологии и биохимии различных групп микроорганизмов: продуцентов антибиотиков чаще всего находят среди актиномицетов, внеклеточное выделение гидролитических ферментов характерно для грамположительных бактерий, типичные продуценты этанола — дрожжи и т. д.
Способность синтезировать целевой продукт является главным критерием при отборе продуцентов. Однако микробиологическая промышленность предъявляет к продуцентам ряд других требований, важных с точки зрения технологии производства. Микроорганизмы должны: 1) обладать высокой скоростью роста; 2) использовать для жизнедеятельности дешевые непищевые субстраты; 3) быть устойчивыми к заражению посторонней микрофлорой. Все это позволяет значительно снизить затраты на производство целевого продукта.
2. Для любого микробиологического производства всегда необходима исходная культура продуцента, которая, как правило, не отличается высокой стабильностью при хранении. Поэтому, обычно, предприятие один раз в 2-3 месяца получает чистую культуру в количестве 3 пробирок из специальной лаборатории профильной фирмы или НИИ, либо в условиях собственной заводской лаборатории организует ее хранение и контроль микробиологической чистоты используемого штамма. При этом обычно одну пробирку с исходным продуцентом используют на размножение исходного штамма, вторую используют для организации микробиологического контроля за исходным штаммом-продуцентом, третью оставляют в резерве.
Объем пробирки и количество клеток микроорганизма в ней ничтожно мало по сравнению с объемом ферментера и поэтому прямой пересев культуры потребует очень длительного времени, пока не будет достигнута необходимая плотность культуры во всем аппарате. С целью сокращения времени на запуск процесса в производственных условиях наработку необходимого количества биомассы осуществляют, как правило, в несколько стадий (не более 4-х) в специальных аппаратах.
Подготовку биообъектов проводят согласно прилагаемым к регламентам инструкциям. В этих целях исходный штамм микроорганизма или споровый материал (для грибов или актиномицетов), сохраняемый в условиях, близких к анабиозу или анабиоза (высушенным в стерильной почве, песке, на пшене, путем лиофилизации, или сублимационной сушки), оживляют после добавления стерильной жидкой питательной среды с последующим высевом на уплотненную питательную среду (агар). Убедившись в подлинности и чистоте культуры (культура называется чистой, если родительские и дочерние клетки в ней практически неразличимы и между ними нельзя установить родственные связи), операции по пересеву штамма на богатую питательными веществами среду возрастающих объемов (или площади) повторяют несколько раз в асептических условиях, переходя от пробирок к колбам различного объема, помещаемым на качалочные устройства (шюттель-аппараты).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 |




