Применяемые в медицине противоопухолевые ФАВ эффективно уничтожают опухолевые клетки, однако почти столь же сильно они воздействуют и на нормальные клетки. Недостаточная терапевтическая широта как следствие высокой и не избирательной токсичности в применяемых дозах представляет собой основное препятствие при химиотерапии опухолей. Для его преодоления необходим целенаправленный транспорт противоопухолевых ФАВ преимущественно в опухолевые клетки — создание транспортных форм цитотоксичных веществ, обладающих повышенным сродством к опухолевым клеткам и возможностью проникать в них.
Противоопухолевое ФАВ может быть непосредственно соединено с лигандом, специфичным в той или иной мере для опухолевых клеток данного вида. Однако выгоднее соединять эти два компонента через полимер-носитель, что ограничивает распространение токсичного ФАВ и позволяет использовать свойства самого полимера: склонность к эндоцитозу, регулируемые заряд и М, кооперативные взаимодействия и т. д. В общей форме механизм действия прививочных ФАП, содержащих противоопухолевые ФАВ, выглядит так. ФАП связывается с клетками в соответствии со своим суммарным зарядом и гидрофильно-липофильным балансом, а также с помощью биоспецифического лиганда, если он есть, после чего подвергается эндоцитозу. В результате переваривания в лизосомах происходит внутриклеточное выделение действующего начала, приводящее к гибели данной клетки. Таким образом, роль полимера-носителя заключается в данном случае в целевом транспорте и облегчении проникновения ФАВ в быстро эндоцитирующие, в том числе опухолевые, клетки.
4. Среди систем организма, предназначенных для инактивации и выведения чужеродных химических соединений (ксенобиотиков), иммунная система «специализируется» на полимерах и более крупных частицах — вирусах, микроорганизмах и т. д. Многие чужеродные полимеры при попадании внутрь организма вызывают иммунный ответ, направленный на нейтрализацию и выведение антигенов. В особенности это относится к биополимерам и полимерам, содержащим низкомолекулярные группы (гаптены), которые иммунологически не активны сами по себе, но приобретают способность индуцировать выработку антител при связывании с полимером-носителам, в первую очередь с белком. Если в качестве гаптенов использовать молекулы низкомолекулярных ФАВ, то образующиеся модифицированные ФАВ белки называются конъюгированными антигенами (КА). Они способны индуцировать выработку антител, специфичных к ФАВ, при введении в организм животных, в то время как введение самих ФАВ иммунного ответа не вызывает.
Общий метод синтеза КА заключается в ковалентном присоединении гаптена к полимеру-носителю. В качестве носителя обычно используют белки. Возможно также применение полиаминокислот и полисахаридов, антигенных самих по себе, и других полимеров. Процесс синтеза КА представляет собой ковалентную модификацию белка низкомолекулярным реагентом. Основной принцип получения КА состоит в том, чтобы связать гаптен с белком так, чтобы та часть молекулы гаптена, которая должна служить антигенной детерминантой, осталась свободной. В зависимости от точки связывания гаптена с носителем можно получить антитела, специфичные к той или иной части его молекулы, а также набор специфических антител. Наличие «вставки» между гаптеном и белком увеличивает доступность гаптена для распознавания и повышает специфичность вырабатываемых антител.
Лекция 5 - Растворимые полимер - белковые соединения и сшитые белки
Содержание:
Синтез и свойства полимер-белковых коньюгатов и сшитых белков. Коньюгаты белков с полифункциональными полимерами-носителями. Полимер-белковые соединения других типов.1. Существует несколько стратегических подходов к синтезу водорастворимых полимерных производных белков (рис. 1). Первый подход заключается в ковалентном связывании белка с водорастворимым функциональным полимером. По замыслу эта стратегия аналогична той, которой придерживаются при иммобилизации белков на нерастворимых носителях, однако переход к растворимым конъюгатам и необходимость последующего их введения в организм вызывает дополнительные проблемы.
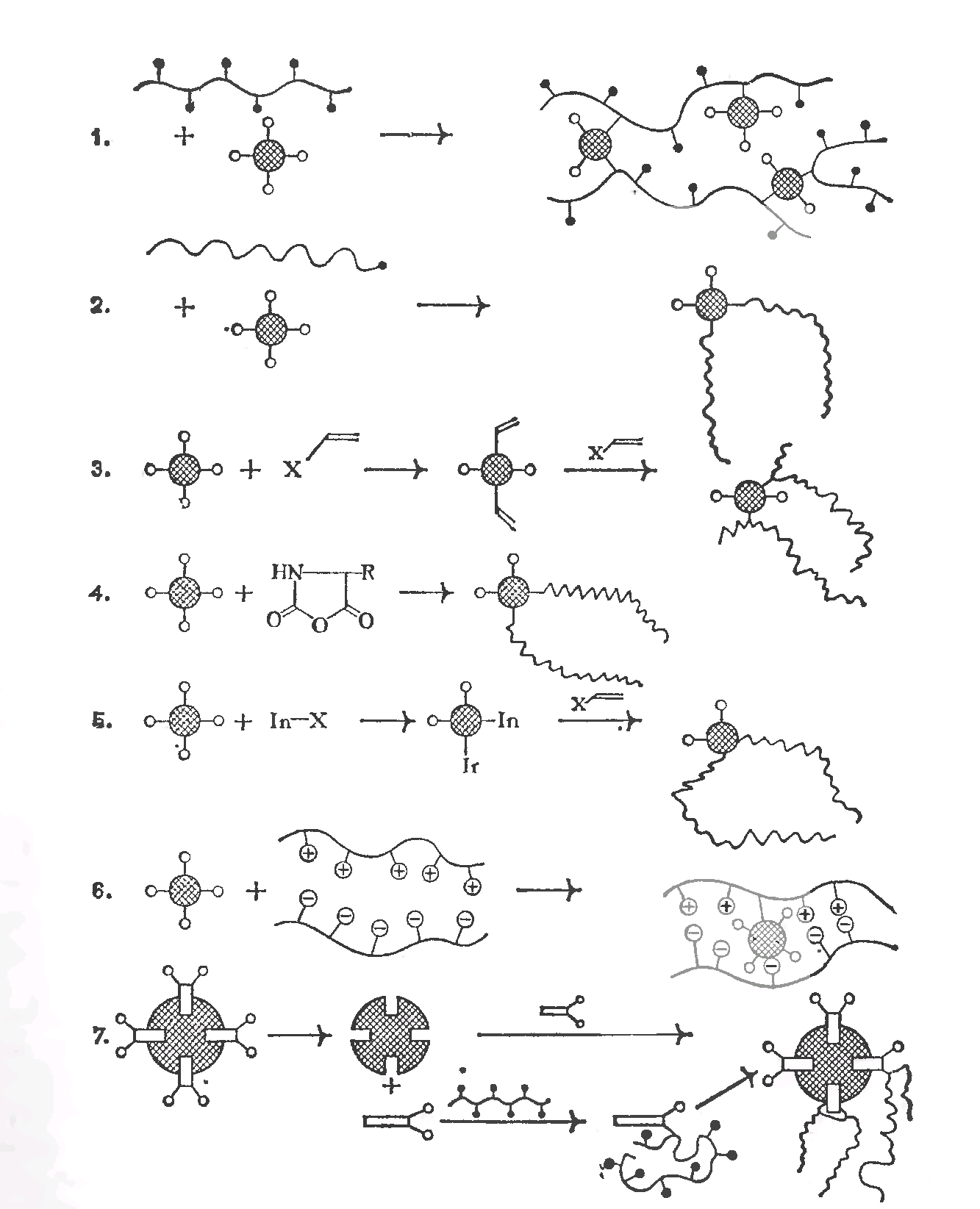
Рис.1
В то же время рассматриваемый подход относительно прост химически и при удачном использовании обеспечивает реализацию полезных свойств полимер-белковых конъюгатов, перечисленных выше.
Для связывания с белком водорастворимый полимер должен иметь группы, способные взаимодействовать с функциональными группами белка в условиях, не вызывающих денатурацию последнего. В подавляющем большинстве случаев это реакции в водных растворах при рН = 6—8, реже 3—10. Химические методы при этом в основном те же, что применяются при иммобилизации ферментов, а также для связывания с полимером низкомолекулярных ФАВ. В белке для взаимодействия с полимером-носителем используют главным образом аминогруппы. Первый вариант благоприятен для стабилизации белка в результате закрепления конформации, но, как указывалось, иногда приводит к значительному изменению физиологической активности. Второй вариант обычно позволяет в большей мере сохранить активность, но в меньшей — сопровождается стабилизацией. Полимер-носитель должен быть гидрофилен, чтобы избежать гидрофобных взаимодействий с белком, и содержать функциональные группы, которые могут непосредственно или после активации реагировать с белком. Связывание белка с полимером протекает по следующей схеме:
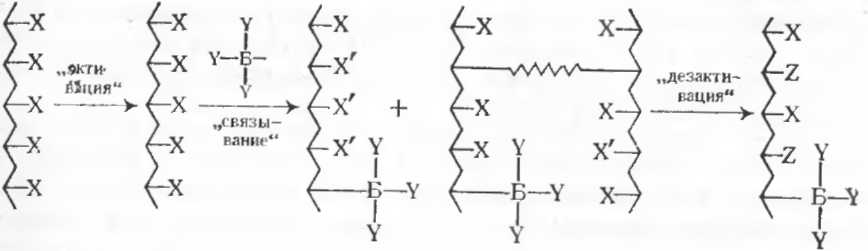
Второй подход к синтезу растворимых полимер-белковых конъюгатов также заключается в связывании белка с полимером, но не по боковым функциональным группам, а по одной из концевых. В качестве полимера используют активированные производные моноэфиров полиэтиленгликоля.
Третий подход к синтезу полимер-белковых конъюгатов заключается в превращении белка в макромономер в результате введения в него двойных связей, обычно по аминогруппам. Макромономер сополимеризуют с низкомолекулярным гидрофильным мономером, формируя таким образом оболочку полимера-носителя вокруг белковой глобулы.
Четвертый подход к синтезу полимер-белковых конъюгатов также заключается в формировании полимера-носителя вокруг белковой глобулы, однако последняя служит не макромономером, а макроинициатором полимеризации N-карбоксиангидри-дов а-аминокислот.
Полимеризация виниловых мономеров под действием радикального инициатора, ковалентно связанного с белком, представляет собой следующий (пятый) подход к синтезу полимер-белковых конъюгатов. В этом случае можно регулировать число и локализацию точек роста цепей.
Полимер-белковые конъюгаты можно получать и на основе нестехиометрических полиэлектролитных комплексов, содержащих белок. В отличие от стехиометрических поликомплексов нестехиометрические растворимы в воде. Это — шестой подход к синтезу полимер-белковых конъюгатов.
2. Трипсин и химотрипсин, связанные с поливинилпирролидоном с М=10 тыс. были получены по следующей схеме:
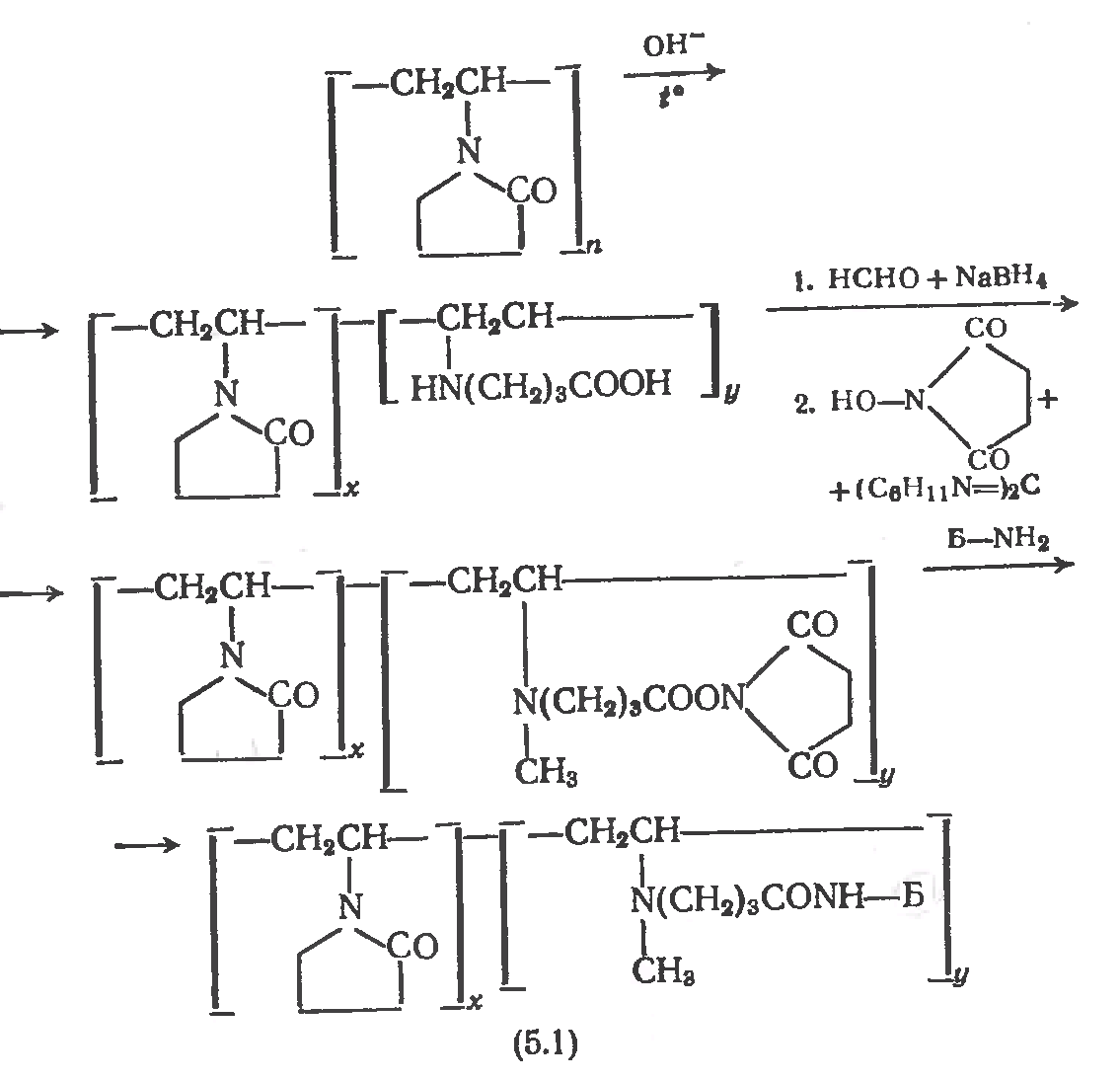
Свойства растворимых конъюгатов ферментов с полиэлектролитами зависят от свойств полимера-носителя и самого фермента. Это связано с формированием микроокружения белковой глобулы, отличающегося от окружающей среды. Поэтому удачный выбор полиэлектролита позволяет получать стабильные конъюгаты с измененным рН-оптимумом.
Аминогруппы трипсина и б-химотрипсина образуют электростатические солевые связи с карбоксильными группами носителя в результате кооперативной реакции. Число связей зависит от плотности заряда на полианионе и определяет сдвиг рН-оптимума и каталитической константы фермента в реакции гидролиза низкомолекулярного субстрата. Образование солевых связей дестабилизирует белок по отношению к тепловой денатурации. С ростом числа связей лабильность белка увеличивается, а его конформация все более отличается от нативной.
Свойства ферментов, связанных с полианионными носителями, зависят от характера носителя и условий получения конъюгата. Белковые конъюгаты на основе синтетических полимеров имеют общий недостаток; пути их метаболизма не ясны, в особенности в отношении входящего в их состав синтетического полимера.
Стабилизация белков в полисахаридных конъюгатах вызывается несколькими факторами. Один из них заключается в сшивании белка, другой был выявлен на примере фиколла-70. О-Метилирование полимера-носителя, т. е. повышение его гидрофобности, приводило к дестабилизации белка в конъюгате, полученном бромциановым методом, по отношению к тепловой денатурации. В то же время конъюгаты с самим фиколлом или О-ацетилфи-коллом были стабильнее, чем исходный фермент. При этом все три конъюгата сохраняли примерно в одинаковой мере ферментативную активность. Наконец, третий стабилизирующий фактор связан с затруднением агрегации белковых глобул перед выпадением в осадок в результате наличия гидрофильной полимерной оболочки. Гидратация белка, вероятно, не менее существенна для стабилизации.
3. Понятие «искусственные антигены» обычно связывают с двумя типами макромолекул. К первому относятся белки или природные полисахариды, модифицированные определенными химическими группировками — гаптенами, ко второму — синтетические макромолекулы, которые полностью идентичны природным. Коллектив взаимодействующих в иммунном ответе клеток состоит из трех главных классов: В-лимфоцитов, Т-лимфоцитов и макрофагов. Синтез антител осуществляется В-лимфоцитами, Т-клетки — хелперы — помогают В-клеткам синтезировать антитела к Т-зависимым антигенам. Антигены, вызывающие синтез антител при непременном участии Т-лимфоцитов, называют тимусзависимыми или Т-зависимыми. В большинстве случаев кооперация Т - и В-клеток является необходимым условием иммунного ответа. Генетический контроль силы иммунного ответа осуществляется через посредство Т-клеток. Клетки третьего типа — макрофаги или А-клетки, кооперирующиеся с Т - и В-лимфоцитами. Макрофаги захватывают антигены, попавшие в организм, в результате чего на поверхности макрофага образуется своеобразная «обойма» антигенных молекул, ориентированных своими детерминантными участками наружу. Эту «обойму» макрофаг предоставляет соответствующему В-лимфоциту, поверхностные белковые рецепторы которого связываются с антигенными детерминантами. Таким путем В-лимфоцит получает первый специфический сигнал, который необходим ему, чтобы начать размножаться и продуцировать антитела. Второй сигнал-—неспецифический — может исходить от Т-лимфоцита, активированного другим антигеном или митогеном.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



