Ни один из перечисленных неприродных полиэлектролитов сам по себе не является антигеном. Механизм действия полимерных адъювантов не связан прямым образом с тонкими особенностями строения звеньев. В основе иммуностимулирующей активности полимерных адъювантов должны лежать некоторые общие механизмы, обусловленные в первую очередь их макромолекулярной природой. Одно из таких свойств макромолекул— способность к многоточечному кооперативному взаимодействию с другими химически комплементарными макромолекулами с образованием устойчивых интерполимерных комплексов или к прочной многоточечной кооперативной адсорбции на химически комплементарных поверхностях.
Исследованы строение и свойства некоторых водорастворимых кооперативных комплексов синтетических линейных полиэлектролитов с глобулярными белками, в частности с белками сыворотки крови. В роли кооперативного партнера по отношению к линейному полимеру выступают функциональные группы на поверхности белковой глобулы. Образование комплексов белков с линейными полиэлектролитами фактически состоит в «прилипании» более или менее протяженных участков полимерных цепей к поверхности белковых глобул. В зависимости от степени полимеризации при прочих равных условиях одна макромолекула может «приклеиваться» либо к одной, либо к нескольким глобулам. Необходимо подчеркнуть, что в комплексах сохраняются достаточно длинные участки линейной цепи в виде петель или свободных концов, которые обеспечивают потенциальную возможность дополнительного многоточечного связывания с другими молекулами или частицами.
Лекция 6 - Физиологически активные полимерные микрочастицы
Содержание:
Микрочастицы, растворяющиеся в организме. Циркулирующие микрочастицы. Полимерные липосомы.1. Некоторые нерастворимые гетероцепные полимерные носители, к которым присоединены ФАВ, относительно быстро распадаются в мягких условиях с образованием водорастворимых фрагментов. Так, химотрипсин или гемоглобин, присоединенные к Сефадексу, окисленному периодатом, можно перевести в растворимые конъюгаты обработкой аминами (рН = 9) или декстраназой (рис.1).
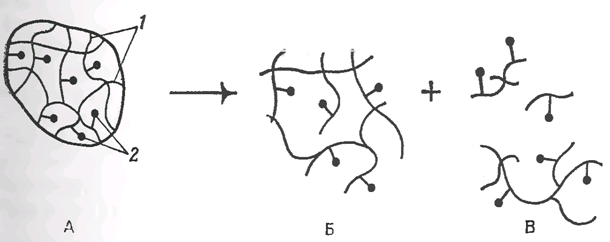
Рис.1 Деструкция микрочастиц диальдегидсефадекса, содержащего ковалентно связанный фермент, в организме: А – набухшая микрочастица до распада; Б – остаток микрочастицы в ходе распада; В – образовавшиеся в результате деструкции растворимые полимер-ферментные конъюгаты; 1 – полисахаридные цепи, 2 – молекулы фрагмента
Аналогичные результаты получены с иммобилизованной на биодеградирующих МЧ стрептокиназой. Время растворения для одного из образцов составило 48 ч, из которых в течение 32 ч в раствор выделялся конъюгированный фермент. Выделение происходило с понижающейся скоростью за счет неравномерного распределения фермента в МЧ.
Химотрипсин был также иммобилизован включением в слабо сшитый гель поливинилпирролидона. Проницаемость геля для фермента регулировалась количеством сшивающего агента так, что скорость выхода фермента в раствор можно было менять от 100 до 64 % за 50 ч. С увеличением степени сшивания возрастает также время полного растворения геля — от 2—3 сут до отсутствия полного растворения, причем фермент высвобождался значительно раньше. Ферментативные свойства химотрипсина при иммобилизации и солюбилизации претерпели изменения, аналогичные описанным выше для диальдегидсе-фадекс-фермента.
При внутрикоронарном введении суспензии МЧ, содержащих фибринолизин, происходит полное разрушение тромбов и восстановление кровотока. Количество нативного фибринолизина, необходимое для осуществления такого же эффекта, в 100 раз больше. Кроме того, в случае МЧ достаточно однократного их введения.
Аналогично ферментам в МЧ из окисленного Сефадекса был включен инсулин. После присоединения инсулина и восстановления альдиминовых связей боргидридом в раствор выделялись водорастворимые конъюгаты с М— 10, 50 и 150 тыс. (62, 40 и 30 мг белка на 1 г носителя в зависимости от степени окисления исходного Сефадекса), которые не высвобождали инсулин. В экспериментах на животных было показано, что все три конъюгата сохранили физиологическую активность исходного инсулина, а время проявления активности увеличилось с 5—6 ч до 14—16 ч.
Таким образом, биосовместимые и биодеградирующие МЧ, содержащие ФАВ, представляют собой удобную лекарственную форму для латентации и постепенного высвобождения действующего начала.
2. Другой вид МЧ — это носители ФАВ, не переходящие в растворимое состояние перед поступлением в циркуляцию. Циркулирующие корпускулы эндоцитируются клетками, либо сорбируются на их поверхности, либо попадают в межклеточное пространство. Это частицы размером 0,1—1 мкм и более, причем сферическая форма существенна для улучшения реологических свойств их суспензии в плазме. Важную роль играет также распределение частиц по размерам, которое должно быть узким. В качестве материала для МЧ используют сшитый до нерастворимого состояния альбумин, а также полученные эмульсионной полимеризацией микросферы синтетических полимеров— гидрофобных (полистирол) или гидрофильных (поли-гидроксиэтилметакрилат и другие акрилаты).
МЧ должны содержать на своей поверхности или по всей массе реакционноспособные группы, пригодные для ковалентного присоединения или сорбции ФАВ и в ряде случаев «узнающих» цель молекулы. Процесс связывания не должен приводить к изменению формы и размеров частиц, если он проводится с готовыми микросферами. Можно также физически включать ФАВ в массу МЧ в ходе их получения. Если при этом полимер образует только оболочку, внутри которой заключен раствор ФАВ, то такие частицы называются микрокапсулами, которые здесь не рассматриваются.
Важнейшие требования к МЧ, содержащим ФАВ:
- целевой транспорт в место действия (орган-мишень); высвобождение ФАВ с достаточной скоростью в месте действия и отсутствие этого процесса в ходе транспортировки кровотоком; достаточная стабильность — МЧ не должны агрегировать при хранении и введении в контакт с кровью; возможность стерилизации перед внутривенным введением; материал МЧ должен быть нетоксичен и способен к выведению из организма в результате биодеструкции.
Проблема биодеструкции МЧ имеет несколько аспектов. МЧ должны быть устойчивы, в частности не выделять ФАВ при хранении и в ходе циркуляции в кровотоке, если они специально для этого не предназначены. Попадая в клетку, МЧ должны постепенно деструкторовать. Оптимальная скорость деструкции зависит от ряда факторов. Если ФАВ механически включено в массу МЧ, то скорость деструкции определяет скорость подачи ФАВ. Для ФАВ, сорбированных на поверхности МЧ, скорость его высвобождения намного выше скорости деструкции, и такие МЧ обычно выделяют ФАВ в ходе циркуляции. ФАВ, химически связанные с МЧ, могут отщепляться в клетке или кровотоке в ходе деструкции МЧ, хотя отщепление ФАВ может опережать деструкцию.
Наилучшие перспективы магнитные МЧ имеют в терапии твердых опухолей. Сосредоточение магнитных МЧ в капиллярах имеет два важных преимущества: во-первых, максимальная диффузия ФАВ наблюдается именно в капиллярах и венулах и, во-вторых, облегчается переход МЧ в межклеточное пространство. В результате происходит насыщение выделяющимся ФАВ межклеточного пространства опухоли.
3. Липосомы — моно - или полиламелярные фосфолипидные полые корпускулы микроразмеров. Каждая из составляющих их ламелей представляет собой замкнутую мембранную бислойную структуру, в которой фосфолипидные молекулы обращены полярными концами наружу, в водную фазу, а гидрофобными, неполярными концами,—внутрь, навстречу друг другу. Минимальный размер липосом составляет около 0,025 мкм в диаметре (для моноламе-дярных липосом), максимальный — до нескольких микрометров (для мультиламелярных липосом). Помимо фосфолипидов в состав липосом входят обычно холестерин и заряженные амфи-фильные соединения, влияющие на стабильность липосом. Внутрь липосом различными методами могут быть включены самые разнообразные ФАВ.
В отличие от МЧ липосомы не имеют полимерной ковалентной структуры. Они подобны сшитым полимерным агрегатам, если рассматривать гидрофобные контакты между неполярными «хвостами» липидов внутри бислоя как аналоги ковалентных связей. Такие контакты менее прочны, чем ковалентные связи, из чего вытекают два важных следствия. Во-первых, они нарушаются при контакте с клеточной мембраной, в которой тоже нет ковалентных связей между компонентами, приводя к слиянию липосомы с клеткой. В результате содержимое липосомы попадает в клетку. Этот принцип положен в основу использования липосом в качестве транспортной формы для ФАВ. Во-вторых, небольшая прочность липосом, в частности межлипидных контактов, обусловливает постепенный выход из них содержимого как при хранении, так и в ходе циркуляции в кровяном русле.
Потребность в более прочных липосомах возникла также в ходе реализации одной из новейших идей в химиотерапии опухолей. Вместо того чтобы доставлять в опухолевую клетку цитотоксичные ФАВ, «убивающие» клетку изнутри, можно дестабилизировать мембрану такой клетки, т. е. «убить» ее снаружи. Для этого необходимы корпускулы, так как процесс протекает на клеточном уровне. Обычные липосомы могут сливаться с клеткой, но при этом гибнет липосома. Для уничтожения же опухолевой клетки необходимо, чтобы возможность слияния сохранялась, но разрушению подвергалась клетка, т. е. мембрана липосомы должна быть прочнее, чем клеточная мембрана. Проблема целеузнавания будет решаться при этом так же, как и для обычных липосом, действующих на молекулярном уровне, т. е. иммунологическими методами.
Упрочнение стенок липосомы может быть реализовано двумя путями. Первый из них заключается в создании ковалентных связей между фосфолипидами, находящимися в ориентированном состоянии, в виде бислоя, путем полимеризации. Второй путь состоит в покрытии липосом полимерной «сеткой». Взаимодействие между фосфолипидами и покрывающим полимером может иметь как ковалентный, так и электростатический характер. В последнем случае должен образоваться псевдополиэлектролитный комплекс между покрывающим полимером и «псевдополимером» — ориентированными фосфолипидами липосомы. Такой комплекс может быть дополнительно стабилизирован липофильными «хвостами», специально вводимыми во взаимодействующий с липосомой полимер.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



