Светопоглощение эталонных растворов измеряют на фотоколориметре КФК-2 со светофильтром, максимум пропускания которого лежит при 540 нм в кювете с толщиной поглощаемого слоя 1 см.
В качестве раствора сравнения используют один из эталонных растворов. Сначала измеряют светопоглощение каждого из эталонных растворов по отношению к первому из них. Затем измеряют светопоглощение всех последующих растворов по отношению ко второму и т. д.
Результаты измерений вносят в таблицу 3.
Таблица 3
Данные для построения градуировочного графика
и вычисления фактора пересчета (F).
Эталонный раствор | Раствор сравнения | Разность концентраций | А | F | ||
№ | С, мг/мл | № | С0, мг/мл | |||
2 3 4 5 6 | 0,156 0,192 0,228 0,264 0,300 | 1 | 0,12 | 0,036 0,072 0,108 0,144 0,180 | ||
3 4 5 6 | 0,192 0,228 0,264 0,300 | 2 | 0,156 | 0,036 0,072 0,108 0,144 | ||
4 5 6 | 0,228 0,264 0,300 | 3 | 0,192 | 0,036 0,072 0,108 | ||
5 6 | 0,264 0,300 | 4 | 0,228 | 0,036 0,072 | ||
6 | 0,300 | 5 | 0,264 | 0,036 |
4. Вычисление фактора пересчета (F).
Вычисляют значение фактора пересчета для каждого измерения светопоглощения А по формуле: 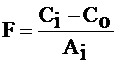
Вычисляют среднее значение (Fср.) полученных результатов.
5. Приготовление раствора с неизвестной концентрацией железа(III).
К анализируемому раствору в мерной колбе емкостью 25 мл добавляют небольшое количество воды, 3 мл 3% раствора сульфосалициловой кислоты и 1 мл 1 М раствора серной кислоты, дистиллированную воду до метки и тщательно перемешивают.
6. Определение содержания железа(III) в растворе с помощью фактора пересчета (F).
Измеряют светопоглощение анализируемого раствора, используя в качестве раствора сравнения эталонный раствор № 1, затем № 2, № 3 и т. д. до получения отрицательного значения относительного светопоглощения. Концентрацию рассчитывают по формуле:
Сх = Ах. F + Со
где Сх – неизвестная концентрация железа(III), мг/мл: Ах – светопоглощение анализируемого раствора; F – фактор пересчета (средний результат); Со – концентрация железа(III) в растворе сравнения, мг/мл.
Содержание железа(III) в мг в анализируемом растворе рассчитывают по формуле: mFe = Cx . V = ________мг, где V – общий объем анализируемого раствора, мл.
7. Определение содержания железа(III) в растворе с помощью градуировочного графика.
По данным таблицы № 3 строят градуировочный график зависимости светопоглощений (Аi), измеренных относительно первого раствора (Со), от концентрации эталонных растворов (мг/мл).
А






![]() 1,2-
1,2-
 1,0-
1,0-
 0,8-
0,8-
 0,6-
0,6-
 0,4-
0,4-
 0,2-
0,2-
![]() | | | | |
| | | | |
0,156 0,192 0,228 0,264 0,300 С, мг/мл
Рис. 3. Градуировочный график для определения содержания железа(III).
При соблюдении основного закона светопоглощения градуировочный график представляет прямую линию, начало которой по оси концентраций смещено от нулевого положения на Со. Измеряют светопоглощение контрольного раствора (Ах) относительно первого стандартного раствора и по графику определяют неизвестную концентрацию железа (Сх, мг/мл). Рассчитывают массу железа(III) в анализируемом растворе по формуле:
mFe(III) = Cмг/мл . V = ______________, мг
где V – общий объем анализируемого раствора, мл.
О Т Ч Е Т
Дифференциальное фотоэлектроколориметрическое определение
железа(III) с сульфосалициловой кислотой в кислой среде
1. Метод анализа:
2. Метод фотометрического определения:
2.1. расчетный (по значению фактора пересчета, F)
2.2. градуировочного графика.
3. Анализируемое вещество:
4. Реагент:
5. Уравнение реакции:
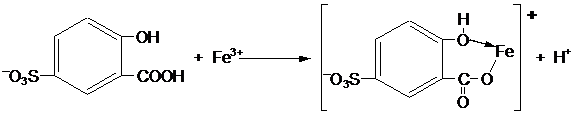
6. Фотометрические характеристики моносульфосалицилата железа (III):
lmax = _________; ε =____________;
Светопоглощение контрольного раствора, Ах =
7. Содержание Fe(III) в контрольном растворе:
7.1. gFe(III) = ______ мг/25 мл (расчетом по значению фактора пересчета, F)
7.2. gFe(III) = ______ мг/25 мл (по градуировочному графику).
Относительная погрешность определения, Е% = _________%.
ФОТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Лабораторная работа № 3
Количественное определение солей кадмия
методом фотометрического титрования.
Метод фотометрического (спектрофотометрического) титрования основан на последовательном измерении светопоглощения А (оптической плотности D) раствора в процессе титрования при заранее заданной длине волны излучения. Если исследуемый раствор подчиняется основному закону светопоглощения, то процесс титрования выражается двумя пересекающимися прямыми линиями. Для определения точки эквивалентности строят кривую титрования в координатах А (D) – (V), где А (D) – светопоглощение (оптическая плотность); V – объем титранта. Излом на кривой титрования соответствует точке эквивалентности.
Сущность лабораторной работы. Количественное определение основано на комплексонометрическом титровании кадмия в присутствии индикатора ксиленолового оранжевого при l = 578 нм. Учитывая, что ни кадмий, ни комплексон III с индикатором не образуют окрашенного комплекса, используют обратное титрование: к раствору, содержащему кадмий, добавляется раствор комплексона III, избыток которого оттитровывается раствором нитрата (ацетата) свинца в присутствии индикатора. При l = 578 нм излучение поглощает практически только комплекс свинца с
ксиленоловым оранжевым. Максимальное развитие окраски комплекса наблюдается в нейтральной среде (рН 6-7).
Реактивы:
1. раствор комплексона III – 0,01 н.
2. раствор нитрата или ацетата свинца – 0,01 н.
3. водный раствор ксиленолового оранжевого, 0,5%.
Лабораторная посуда:
1. бюретка на 10 мл
2. пипетки Мора емкостью 10 мл
3. мерные колбы емкостью 100 мл.
Приборы:
1. колориметр концентрационный, КФК-2
2. титровальное приспособление ТПР-М.
Порядок выполнения работы.
Раствор, содержащий 20-50 мг кадмия, помещают в мерную колбу вместимостью 100 мл (контрольный раствор), разбавляют дистиллированной водой до метки и тщательно перемешивают. Для анализа аликвотную часть анализируемого раствора (VА = 10,00 мл) помещают в кювету, добавляют пипеткой 10,00 мл раствора комплексона III (0,01 н.). Кювету с раствором помещают в кюветное отделение фотоколориметра КФК-2. Устанавливают требуемый светофильтр (l = 540 нм). Закрывают крышку кюветного отделения и ручками «чувствительность» и «установка 100 грубо» и «точно» устанавливают отсчет 100 по шкале колориметра. Открывают крышку кюветного отделения и добавляют в кювету 4-7 капли 0,5% водного раствора индикатора (ксиленолового оранжевого). Закрывают крышку кюветного отделения и через отверстие в крышке вводят в анализируемый раствор стеклянную мешалку, установленную на штанге титровального приспособления ТПР-М. На этой же штанге закрепляется бюретка вместимостью 10 мл с раствором титранта (Pb(NO3)2 или Pb(СН3СОO)2), оттянутый кончик которой вводят в другое отверстие крышки кюветного отделения. Включают перемешивание. Для этого на передней панели титровального приспособления переключатель «сеть» переводят в положение «включено» (загорается зеленая лампочка индикатора). Рукоятка «скорость перемешивания» устанавливается в положение «5». Через ~ 30 секунд снимают значение светопоглощения (Ао) по шкале фотоколориметра. Перемешивание оставляют включенным до окончания титрования. В процессе титрования титрант (0,01 н. раствор Pb(NO3)2 или Pb(СН3СОO)2) приливают из бюретки порциями по 0,5 мл. После добавления каждой порции титранта выдерживают раствор ~ 30 секунд и снимают значения светопоглощения по шкале фотоколориметра. Все значения светопоглощения, используемые для расчетов и построения кривой титрования, должны содержать поправку на разбавление раствора при титровании, т. е.
А = 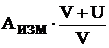 , где
, где
V – первоначальный объем титруемого раствора, (20 мл);
U – объем добавленного титранта, мл.
Титрование заканчивают при добавлении 9 мл титранта. Результаты титрования заносят в таблицу 4.
Таблица 4
Данные для построения кривой фотометрического титрования кадмия
с индикатором ксиленоловым оранжевым
Объем добавленного титранта U, мл | Светопоглощение, Аизм | Светопоглощение с учетом разбавления А = |
0 | ||
0,5 | ||
1,0 | ||
1,5 | ||
2,0 | ||
2,5 | ||
3,0 | ||
3,5 | ||
4,0 | ||
4,5 | ||
5,0 | ||
5,5 | ||
6,0 | ||
6,5 | ||
7,0 | ||
7,5 | ||
8,0 | ||
8,5 | ||
9,0 |
По данным таблицы 4 строят кривую титрования в координатах А - U, где А – светопоглощение с учетом разбавления, U - объем добавленного титранта, мл.
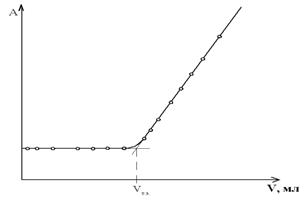
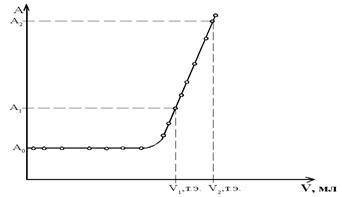
а б
Рис. 4. Образец кривой фотометрического титрования кадмия с ксиленоловым оранжевым.
А


U, мл
Рис. 5. Кривая фотометрического титрования кадмия с ксиленоловым оранжевым.
Объем, соответствующий точке эквивалентности (Uт. э.) определяют:
1) экстрополяцией прямолинейных участков графика кривой титрования (рис. 4, а);
2) если кривая титрования имеет относительно большие прямолинейные участки, определение объема точки эквивалентности проводят расчетным путем. Для этого строят кривую титрования и выбирают 2 точки на кривой после перегиба (т. е. после точки эквивалентности). Расчет Uт. э. проводят по формуле для точки пересечения двух прямых, одна из которых параллельна оси абсцисс (рис. 4, б).
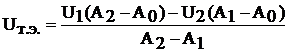 , где
, где
U1 и U2 – объемы титранта, пошедшие на определение 2-х точек после перегиба
А1 и А2 – значения светопоглощения, соответствующие объемам титранта U1 и U2 (рис. 1, б)
А0 – значение светопоглощения до т. э.
Расчет содержания кадмия в растворе проводят по формуле для обратного титрования
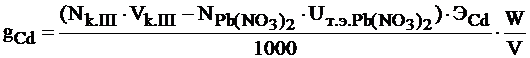
О Т Ч Е Т
Количественное определение солей кадмия
методом фотометрического титрования.
1. Метод анализа:
2. Способ количественного определения:
3. Анализируемое вещество:
4. Титрант:
5. Вспомогательное вещество:
6. Индикатор:
7. Уравнения реакций:
8. Характеристики образующегося комплекса [PbH4R]0:
цвет – красно-розовый;
фотометрические характеристики: lmax = 580 нм; Е = 1,9.104.
9. Значение объема титранта, соответствующее точке эквивалентности
9.1. Vт. э. = ………. мл (по графику)
9.2. Vт. э. = ………. мл (расчетным способом).
10. Содержание Cd2+ в контрольном растворе
g(Cd2+) = ………… (г).
11. Относительная погрешность определения, Е% = …………%.
ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
К У Л О Н О М Е Т Р И Я
Работа 1. Определение кислот.
Определение кислот основано на электрогенерации ионов ОH - из воды на платиновом катоде и последующим их взаимодействии с ионами Н3О+. Вспомогательным реагентом в данном случае является вода, в которую для повышения электропроводности необходимо добавить индифферентный сильный электролит – 0,5 М или 10%-ный раствор сульфата калия или натрия. На электроде будут протекать следующие реакции:
на катоде: 2Н3О+ + 2е– = Н2+ 2Н2О; 2Н2О + 2е– = Н2 + 2ОН–,
а в растворе: ОН– + Н3О+ = 2Н2О. После завершения химической реакции избыток ионов ОН- создаст в растворе щелочную среду, что можно обнаружить с помощью кислотно-основного индикатора (фенолфталеина) или потенциометрически со стеклянным индикаторным электродом.
Приборы и реактивы:
Кулонометрическая установка с электронным секундомером
Магнитная мешалка
Генераторный платиновый электрод
Вспомогательный графитовый электрод
Мерная колба вместимостью 100 мл
Пипетка вместимостью 10 мл
Фенолфталеин 1% спиртовый раствор
Сульфат натрия или калия 10% или 0,5 М раствор
Выполнение работы: Исследуемый раствор кислоты разбавляют дистиллированной водой в мерной колбе вместимостью 100 мл до метки и хорошо перемешивают. В стакан для титрования помещают примерно 10 мл 0,5 М или 10%-ного раствора Na2SO4 (или К2SO4), семь капель фенолфталеина, опускают платиновый генераторный электрод и стержень магнитной мешалки. В анодную камеру наливают 0,5 М (или 10%-ный) раствор Na2SO4 (или К2SO4), опускают вспомогательный графитовый электрод и соединяют оба стакана электролитическим мостиком, заполненным тем же сильным электролитом. При выключенном тумблере «Ячейка» ручкой «Ток» устанавливают ток электролиза 5 мА и включают магнитную мешалку. Для исключения ошибки, связанной с присутствием в растворе СО2, сначала проводят предэлектролиз фонового раствора током 5 мА, включив тумблер «Ячейка». При появлении розовой окраски раствора тумблер «Ячейка» выключают. Затем в стакан с генераторным электродом пипеткой добавляют 10,00 мл анализируемого раствора кислоты, на микрокалькуляторе, служащем электронным секундомером, нажимают клавиши «С», «+» и «1», а затем включают ячейку. После появления розовой окраски раствора такой же интенсивности, как и при предэлектролизе, выключают ячейку и записывают ток электролиза и время продолжительности титрования с точностью до 1 сек.
Титрование повторяют трижды и рассчитывают среднее время электролиза. Содержание кислоты (g) рассчитывают по формуле:

где: I - ток электролиза, А; t - время электролиза, с; М - молярная масса кислоты, г/моль; W - вместимость мерной колбы, мл; V - вместимость пипетки, мл; n – число электронов (для серной кислоты n = 2), F - константа Фарадея, 96485 Кл/моль.
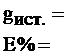
О Т Ч Е Т
Определение серной кислоты кулонометрическим титрованием
1. Анализ:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |




