DpH/DV
 |
 |

V+1/2DV
Рассчитывают содержание карбоната натрия по формуле:
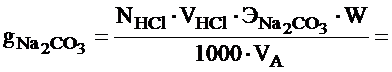
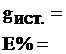
О Т Ч Е Т
Определение массы карбоната натрия
методом потенциометрического титрования.
1. Анализ:
2. Метод:
3. Основное уравнение метода:
4. Схема определения:
5. Титрант:
6. Прием титрования:
7. Способ определения:
8. Уравнение химической реакции:
9. Расчет fэкв(А) и Э(А):
10. Расчет g(А):
11. Относительная погрешность определения Е%:________
Работа 7. Определение содержания FeSO4.∙7H2O методом потенциометрического титрования
Метод потенциометрического титрования основан на экспериментальном определении потенциала (Е) в процессе титрования с последующим определением точки эквивалентности по кривой титрования, построенной в дифференциальной форме. Значения Е в процессе титрования измеряют на потенциометре (рН-метре) с помощью индикаторного платинового электрода в паре с хлоридсеребряным электродом сравнения.
Выполнение работы.
1. Включают прибор в сеть и нажимают клавишу «On/Off» на панели рН-метра. На индикаторе должны появиться цифры. Выбирают режим измерения потенциала (mV), нажимая кнопку «mV/pH» на панели прибора.
2. Определение проводят способом отдельных навесок, для чего контрольный раствор сульфата железа(II) получают в двух стаканчиках: раствор в одном из них для ориентировочного титрования, в другом - для точного титрования. В стаканчик для титрования с 10,00 мл анализируемого раствора сульфата железа (II) добавляют 10 мл 12,5%-ного раствора серной кислоты, стержень магнитной мешалки и опускают электродную пару. При необходимости доливают дистиллированную воду так, чтобы электроды были погружены в раствор на 1 см.
3. Заполняют бюретку 0,01 н. раствором дихромата калия, включают магнитную мешалку и приступают к титрованию.
4. Ориентировочное титрование: добавляют титрант порциями по 1 мл до Е не менее 600 мВ, записывая результаты измерения Е в таблицу:
V, мл | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
Е, мВ |
По данным таблицы строят интегральную кривую титрования в координатах Е - V и определяют примерный объем титранта (Х) в начале скачка титрования.
Е, мВ
 |
 |

V, мл
5. Точное титрование: заполняют бюретку раствором титранта до нулевой отметки, в другой стаканчик с 10,00 мл анализируемого раствора сульфата железа(II) добавляют 10 мл 12,5%-ного раствора серной кислоты, стержень магнитной мешалки, ставят на магнитную мешалку и опускают электродную пару, доливая воду при необходимости. Затем добавляют объем титранта, соответствующий началу скачка титрования (Х) и приступают к точному титрованию, добавляя титрант порциями по 0,1 мл и записывая получаемые при этом значения Е.
Результаты заносят в таблицу:
V, мл | Е | DV | DЕ | V+1/2DV | DЕ/DV |
|
Х,0 | - | - | - | - | ||
0,11 | ||||||
,1 | ||||||
0,1 | ||||||
,2 | ||||||
0,1 | ||||||
,3 | ||||||
0,1 | ||||||
,4 | ||||||
0,1 | ||||||
,5 | ||||||
0,1 | ||||||
,6 | ||||||
0,1 | ||||||
,7 | ||||||
0,1 | ||||||
,8 | ||||||
0,1 | ||||||
,9 | ||||||
0,1 | ||||||
,0 | ||||||
0,1 | ||||||
,1 | ||||||
0,1 | ||||||
,2 | ||||||
0,1 | ||||||
,3 | ||||||
- | - | - | - |
6. Строят дифференциальную кривую титрования в координатах DЕ/DV – V+1/2DV и по максимуму на ней определяют точно точку эквивалентности (DЕ – разность последующего и предыдущего значения Е).
DЕ/DV
 |
 |
V+1/2DV
7. Рассчитывают содержание сульфата железа в растворе (g) в граммах по формуле:
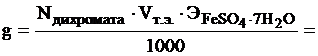
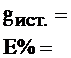
О Т Ч Е Т
Определение содержания FeSO4.∙7H2O методом потенциометрического титрования
1. Анализ:
2. Метод:
3. Основное уравнение метода:
4. Схема определения:
5. Титрант:
6. Прием титрования:
7. Способ определения:
8. Уравнение химической реакции:
9. Расчет fэкв(А) и Э(А):
10. Расчет g(А):
11. Относительная погрешность определения Е%:__________
ХРОМАТОГРАФИЯ
Хроматография – физико-химический метод разделения смесей веществ, основанный на различии в скоростях движения компонентов смеси через неподвижную фазу под действием подвижной фазы.
Хроматография широко применяется в научных исследованиях, в фармации, в медицине, в биологии, а также для мониторинга окружающей среды. В ряде случаев хроматография является лучшим или единственным методом анализа.
Знания, умения и навыки, полученные на занятии по хроматографии, будут использованы при изучении фармацевтической химии, фармакогнозии, токсикологической химии, а также в практической деятельности специалиста провизора.
Цель изучения темы: на основе знания теоретических основ метода хроматографии и приобретенных практических умений научиться применять данный метод для качественного и количественного анализа веществ.
Целевые задачи:
1. Качественный анализ основных компонентов мятного масла.
2. Определение количественного содержания ментола в спиртовом растворе мятного масла методом ГЖХ
3. Количественное определение солей методом ионообменной хроматографии.
4. Решение типовых расчетных задач.
ГАЗОВАЯ ХРОМАТОГРАФИЯ
Теоретические основы. Газовая хроматография – это метод разделения смесей газов, а также паров неразлагающихся жидкостей и твердых веществ при их прохождении через колонку, заполненную сорбентом. В колонке происходит разделение смеси вследствие распределения ее компонентов между движущейся газовой фазой и неподвижной фазой, которая может быть твердой (в газовой хроматографии, ГХ)
и жидкой (газожидкостная хроматография, ГЖХ).
Газовая хроматография широко применяется для определения веществ, обладающих летучестью при температуре колонки до о С. Метод высокочувствителен (до 10-12 г). Для анализа необходимо небольшое количество вещества (объем пробы 1 мкл). Газовая хроматография позволяет проводить одновременно качественный и количественный анализ смесей веществ.
Качественный анализ проводится путем сравнения времени удерживания анализируемого вещества и временем удерживания известного вещества или с табличными величинами.
1 . Определение времени удерживания
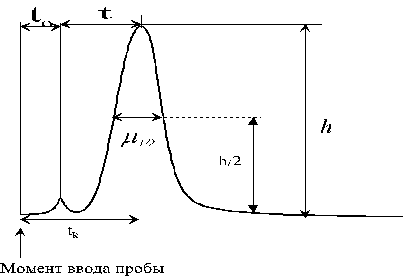
Разделение в хроматографии основано на различной сорбируемости разделяемых веществ. Если вещество не сорбируется, то оно не удерживается на колонке и выходит со скоростью газа - носителя. Сорбирующиеся вещества определенное время удерживаются в колонке. Время от момента ввода пробы в колонку до выхода максимума пика называется временем удерживания tR. В колонке оно складывается из двух составляющих: времени нахождения молекул в газовой фазе (t0) и времени, когда молекулы находятся в сорбируемом состоянии (t). tо определяется по времени удерживания воздуха.
tR = t0 + t
Для характеристики истинной удерживающей способности колонки применяют t (исправленное время удерживания):
t = tR – t0
На практике часто измеряют не время удерживания, а расстояние удерживания (в мм), пропорциональное времени удерживания, т. е. расстояние на хроматограмме от точки, соответствующей моменту ввода пробы, до точки на оси абцисс, отвечающей положению максимума (вершины) пика.
2. ОПРЕДЕЛЕНИЕ ЧИСЛА ТЕОРЕТИЧЕСКИХ ТАРЕЛОК
ПО ПАРАМЕТРАМ ПИКА МЕНТОЛА
Для оценки эффективности колонки пользуются числом теоретических тарелок (N):
N = 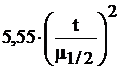 , где m1/2 - ширина пика на половине высоты.
, где m1/2 - ширина пика на половине высоты.
Степень разделения двух компонентов является функцией числа теоретических тарелок. На практике используются колонки с N>500.
Широко используется другая характеристика эффективности колонки - высота, эквивалентная теоретической тарелке (ВЭТТ). ВЭТТ равна общей длине колонки (L), деленной на число теоретических тарелок. ВЭТТ = L/N.
ВЭТТ выражается в мм. ВЭТТ - качественный показатель, позволяющий сравнить эффективность разных колонок.
3. СЕЛЕКТИВНОСТЬ КОЛОНКИ.
Расстояние между максимумами двух пиков является мерой селективности колонки. Чем оно больше, тем более селективна колонка. Количественно селективность оценивают величиной коэффициента разделения (a) .
a = tn+1/ tn
Например, для 2 и 3 пиков a = t3/t2, если a = 1, вещества не делятся. Коэффициент разделения должен быть больше единицы. Полнота разделения двух компонентов количественно выражается критерием разделения К.
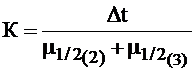
где Dt - расстояние между максимумами пиков разделяемых веществ.
Индексы 2, 3 - номера пиков. При К > 1 разделение достаточно полное.
Лабораторная работа № 1.
Качественный и количественный анализ раствора мятного масла
методом ГЖХ
Цель работы: научиться практически применять метод ГЖХ для анализа раствора мятного масла.
Приборы и реактивы:
1. Хроматограф "Хром-5".
2. Стеклянная хроматографическая колонка, заполненная Реоплекс-% от массы твердого носителя Inerton-супер).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |




