3. Микрошприц.
4. Пенный расходомер.
5. Секундомер.
6. Раствор мятного масла в этаноле.
7. Стандартный раствор ментола в этаноле.
Условия проведения анализа:
газ-носитель азот
длина колонки 1 м
Температуры:
испари
термостата 900
детектора 1500.
Скорость потока газа-носителя (азота) 30 мл/мин.
Скорость потока водорода 30 мл/мин.
Подготовка хроматографа к работе
1. Открыть вентилем баллон с газом-носителем азотом.
2. Редуктором высокого давления на баллоне установить давление азота на входе в прибор 0,8 атм.
3. Проверить наличие потока газа-носителя на выходе из газовой колонки прибора с помощью расходомера с мыльной пленкой.
4. Установить скорость потока азота 30 мл/мин.
5. Установить параметры работы прибора (температуру испарителя, колонок (тер
мостата и детектора) согласно условиям проведения анализа.
6. Включить генератор водорода.
7. Включить компрессор, подающий воздух.
8. Включить сетевую вилку прибора в сеть 220 В и тумблерами включить прибор.
9. Поджечь ДИП.
10. Включить компьютер и запустить программу «Хромос».
Выполнение работы
После установления на хроматографе стабильной нулевой линии в испаритель хро
матографа вводят 1 мкл раствора мятного масла и хроматографируют его.
- По полученной хроматограмме находят значение времени удерживания (расстояния удерживания) каждого компонента смеси в мм, для чего измеряют расстояние от точки, соответствующей моменту ввода пробы, до точки на оси абцисс, отвечающей положению максимума (вершины) пика.
- Затем по таблице № 2 устанавливают качественный состав основных компонентов мятного масла.
- Оценивают эффективность колонки по пику ментола, рассчитав число теоретических тарелок (N) и ВЭТТ (мм). Длина колонки 1 м.
- Рассчитывают коэффициенты разделения (a) и критерий разделения (К) для второго и третьего компонентов смеси (октанола-3 и ментофурана).
- Количественный анализ: расчет массовой доли ментола проводят методами абсолютной калибровки и внутренней нормализации.
Метод абсолютной калибровки
Построение градуировочного графика. Готовят стандартный раствор ментола. В мерную колбу на 25 мл помещают точную навеску ментола массой ~ 0,3 г и доводят до метки спиртом. Рассчитывают концентрацию Сст в г/мл по формуле: ![]() . В испаритель хроматографа вводят 1,0; 2,0; 3,0; 4,0; 5,0 мкл стандартного раствора ментола и хроматографируют их. На хроматограммах измеряют площади пиков ментола по формуле: S = h∙m1/2, по этим данным строят градуировочный график в координатах S ‑ V стандартного раствора.
. В испаритель хроматографа вводят 1,0; 2,0; 3,0; 4,0; 5,0 мкл стандартного раствора ментола и хроматографируют их. На хроматограммах измеряют площади пиков ментола по формуле: S = h∙m1/2, по этим данным строят градуировочный график в координатах S ‑ V стандартного раствора.
Определение концентрации ментола в мятном масле. В тех же условиях хроматографируют VA (1 мкл) пробы спиртового раствора мятного масла с неизвестной концентрацией ментола, определяют площадь пика ментола и по градуировочному графику находят объем стандартного раствора (VX), соответствующий содержанию ментола в образце спиртового раствора мятного масла. Концентрацию ментола в г/мл в спиртовом растворе мятного масла рассчитывают по формуле:
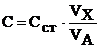 .
.
При выполнении работы точная навеска ментола составила 0,2945 г, а данные для построения градуировочного графика были получены следующие:
Vст. раствора, мкл 1,0 2,0 3,0 4,0 5,0
S, мм2 1384
(График можно построить или рассчитать коэффициенты линейного уравнения по методу наименьших квадратов по формулам, приведенным на стр.9). Рассчитайте концентрацию ментола в г/мл в образце спиртового раствора мятного масла, хроматограмма которого получена Вами.
Метод внутренней нормализации
Рассчитывают площади пиков 5-ти основных компонентов мятного масла, суммируют их. Массовую долю ментола рассчитывают по формуле:
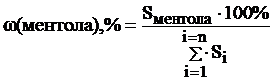 , где
, где
Sментола – площадь пика ментола,
ΣSi – сумма площадей пиков основных компонентов мятного масла.
Результаты качественного, количественного анализа, оценки эффективности колонки и селективности НЖФ представляют в виде таблицы № 1.
Таблица № 1
№ пика | t, мм | Компонент смеси | Высота пика, h, мм | Полуширина пика, m1/2, мм | Площадь пика, S, мм2 | Массовая доля, wi,% |
1. | ||||||
2. | ||||||
3. | ||||||
4. | ||||||
5. |
SSi=
N = ВЭТТ = a = К =
Таблица № 2. Времена удерживания (расстояния удерживания) некоторых компонентов мятного масла.
№ | Наименование вещества | t, мм |
1. | a-пинен | 17 |
2. | камфен | 23 |
3. | b-пинен | 25 |
4. | лимонен | 29 |
5. | цинеол | 32 |
6. | n-цимол | 35 |
7. | октанол-3 | 47 |
8. | ментофуран | 56 |
9. | линалоол | 61 |
10. | ментон | 67 |
11. | изоментон | 74 |
12. | неоментон | 80 |
13. | ментол | 90 |
Лабораторная работа № 2.
Ионообменная хроматография
В основе метода ионообменной хроматографии лежит реакция обмена между растворами и сорбентом. В качестве сорбента применяют специальные синтетические смолы – ионообменные, содержащие активные группы, которые способны к обмену ионами с раствором. Ионообменники, способные к обмену катионов, называются катионитами, анионов – анионитами. Ионообменная хроматография дает возможность проводить количественное определение солей кислотно-основным методом по следующим схемам:
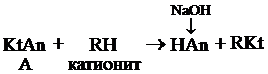 или
или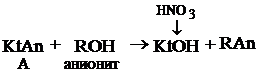
Количественное определение NaCl (KCl, CaCl2, Na2SO4, KNO3) методом ионообменной хроматографии.
Реактивы и оборудование:
1. Стандартные раствора NaOH (0,1 н.), HNO3 (0,1 н.).
2. Сильнокислотный катионит KУ-1 в Н-форме, сильноосновный анионит ЭДЭ-10 в ОН-форме.
3. 1%-ные растворы метилового оранжевого, фенолфталеина.
4. Колонки для хроматографирования с катионитом и анионитом.
5. Конические колбы вместимостью 500 мл.
6. Бюретка вместимостью 25 мл.
Подготовка ионообменной смолы.
Катионит и анионит находятся в колонке в кислой и щелочной среде. Перед проведением анализа ионообменную смолу промывают очищенной водой до нейтральной реакции по метиловому оранжевому (катионит) или фенолфталеину (анионит). Желтая окраска метилоранжа или бесцветная – фенолфталеина указывает на отсутствие кислоты в катионите или основания в анионите.
Выполнение работы.
Колонка с ионитом должна быть заполнена очищенной водой до «зеркала» над поверхностью сорбента. Необходимо следить, чтобы между зёрнами ионита не попадал воздух. В случае попадания воздуха колонку следует перетряхивать или перезаряжать.
Анализируемый раствор вносят в хроматографическую колонку, открывают кран колонки и медленно, по каплям выпускают жидкость из колонки со скоростью 20 – 25 капель в 1 минуту в коническую колбу. Когда над поверхностью ионита останется слой жидкости высотой ~2-3 см, в колонку наливают очищенную воду порциями по 5-10 мл до нейтральной реакции жидкости, вытекающей из колонки (по метиловому оранжевому – желтый цвет, по фенолфталеину – бесцветный). Промывную жидкость и пробы на реакцию среды выливают в ту же коническую колбу. В полученный раствор при необходимости добавляют 2-3 капли индикатора,: и весь раствор оттитровывают 0,1 н. раствором NaOH (катионит) до желтой окраски индикатора или 0,1 н. раствором HNO3 (анионит) до бесцветного раствора. Содержание соли (gА) вычисляют по формуле:
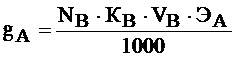
gист.= Е% = _______%.
После окончания анализа ионит регенерируют. Для этого в колонку заливают 1 н. раствор HCl (катионит) или NaOH (анионит), выпустив из колонки немного раствора, чтобы регенерирующий раствор полностью прореагировал с ионитом.
ОТЧЕТ
о количественном определении _______ методом ионообменной хроматографии.
1 Анализ:
2. Метод:
3. Схема определения:
4. Титрант:
5. Индикатор:
6. Подвижная фаза:
7. Неподвижная фаза:
8. Механизм хроматографического разделения:
9. Способ определения:
10. Прием титрования:
11. Уравнения реакций:
12. Расчет fэкв и Э(А):
13. Расчет g(А):
14. Расчет относительной погрешности Е% = __________%.
Обучающие задачи с эталоном решения
1. Рассчитать число теоретических тарелок (N) и высоту, эквивалентную теоретической тарелке (ВЭТТ) для колонки длиной 1 м, если при хроматографировании вещества расстояние удерживания составляет 7,5 см, а ширина пика на половине высоты 0,4 см.
Решение: ![]() . Подставив значения в формулу, получаем
. Подставив значения в формулу, получаем 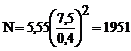 ; ВЭТТ =
; ВЭТТ = 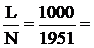 0,5 мм.
0,5 мм.
Ответ: N = 1951; ВЭТТ = 0,5 мм.
2. Рассчитать массовую долю (%) каждого компонента смеси по данным, полученным методом ГЖХ, считая поправочные коэффициенты равными единице.
Компоненты смеси | h, высота пика, мм | m1/2, полуширина пика, мм | S, площадь пика, мм2 | w, %, массовая доля компонента |
a-пинен | 17 | 2 | 34 | 2,47 |
Октанол-3 | 37 | 4 | 148 | 10,74 |
Ментофуран | 22 | 5 | 110 | 7,98 |
Ментон | 62 | 6 | 372 | 27,00 |
Ментол | 102 | 7 | 714 | 51,81 |
Решение: расчеты проводим по методу внутренней нормализации, согласно которому 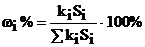 . По формуле S = h·m1/2 найдем площади пиков компонентов смеси и занесем их в таблицу. Поправочные коэффициенты ki считаем равными единице. Найдем суммарную площадь пиков:
. По формуле S = h·m1/2 найдем площади пиков компонентов смеси и занесем их в таблицу. Поправочные коэффициенты ki считаем равными единице. Найдем суммарную площадь пиков: ![]() Si = 34 + 148 + 110 + 372 + 714 = 1378 мм2. Отсюда массовая доля (%) равна w(a-пинена) =
Si = 34 + 148 + 110 + 372 + 714 = 1378 мм2. Отсюда массовая доля (%) равна w(a-пинена) =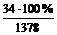 = 2,47%. Аналогично находим массовые доли (%) остальных компонентов смеси и заносим их в таблицу.
= 2,47%. Аналогично находим массовые доли (%) остальных компонентов смеси и заносим их в таблицу.
3. Рассчитать массовую долю ментола в растворе мятного масла (r = 0,83 г/мл), если при хроматографировании 1 мкл образца площадь пика ментола на хроматограмме равна 427 мм2, а данные для построения градуировочного графика с использованием стандартного раствора ментола следующие:
m, мкг
S, мм2
Решение. Построим градуировочный график в координатах S - m.

По графику определим массу ментола (m = 20 мкг). Найдем массовую долю ментола в растворе:
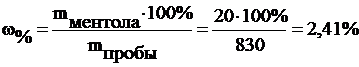
(mпробы = r. V = 0,83 . 1,= 0,8г = 830 мкг).
Задачи для самостоятельного решения
1. Рассчитайте толщину поглощающего слоя (см) для измерения светопоглощения раствора сульфата кобальта, содержащего 0,5 мг соли в 50 мл раствора, если e = 4000, А = 0,52, М(СоSО4) = 155 г/моль. (Ответ: 2 см)
2. Определите содержание меди (в %) в 10 г образца, если 1 г его растворили в мерной колбе вместимостью 100 мл. Светопоглощение полученного раствора в кювете с толщиной поглощающего слоя 3 см составило 0,675, а молярный коэффициент поглощения равен 45000.
(Ответ: 3,2.10-3 %)
3. Рассчитайте, сколько времени потребуется для завершения кулонометрического титрования 5,58 мг железа (II) электрогенерированным ионом церия (IV) при постоянном токе электролиза, равным 5,00 мА. (Ответ: 1928 с)
4. Рассчитайте, при каком значении тока следует проводить кулонометрическое титрование 3,16 мг натрия тиосульфата пятиводного электрогенерированным иодом в присутствии крахмала, чтобы для появления синей окраски раствора потребовалось пропускать ток не менее 100 с. (Ответ: 12,3 мА)
5. Анализируемый раствор метиламина CH3NH2 объемом 20,00 мл разбавили в мерной колбе до 100,0 мл, затем 10,00 мл полученного раствора оттитровали потенциометрически 0,1000 н. раствором HCl. Построить кривую титрования в координатах: DpH/DV - V+1/2DV и определить молярную концентрацию эквивалента исходного раствора метиламина по следующим данным:
V(HCl),мл | 10,00 | 12,00 | 14,00 | 14,50 | 14,90 | 15,00 | 15,10 | 15,50 | 16,00 |
pH | 10,40 | 10,12 | 9,56 | 9,18 | 8,42 | 6,02 | 3,52 | 2,85 | 2,55 |
(Ответ: 0,7525 н.)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |




