DpH/DV
 |
 |

V+1/2DV
7. Рассчитывают содержание уксусной кислоты в растворе (g) в граммах по формуле (К – поправочный коэффициент к нормальности NaOH):
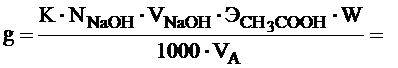
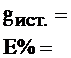
О Т Ч Е Т
Определение содержания CH3COOH методом потенциометрического титрования
1. Анализ:
2. Метод:
3. Основное уравнение метода:
4. Схема определения:
5. Титрант:
6. Прием титрования:
7. Способ определения:
8. Уравнение химической реакции:
9. Расчет fэкв(А) и Э(А):
10. Расчет g(А):
11. Относительная погрешность определения Е%:
Работа 5. Определение содержания фосфорной кислоты методом потенциометрического титрования
Фосфорная кислота Н3РО4 имеет три константы кислотности: К1 = 7,1.10-3, К2 = 6,3.10-8 и К3 = 5.10-13. Соотношение К1:К2 ≈ 105 и К2:К3 ≈ 105, то есть больше критерия 104 , поэтому на кривой титрования будут наблюдаться два скачка титрования, соответствующие оттитровыванию первого и второго протонов. Третий скачок у фосфорной кислоты отсутствует, так как величина третьей константы кислотности меньше 10-8. Соответственно, фактор эквивалентности для фосфорной кислоты будет равен 1 при ее определении по первому скачку титрования и ½ при определении по второму скачку титрования.
Выполнение работы.
1. Включают прибор в сеть и нажимают клавишу «On/Off» на панели рН-метра. На индикаторе должны появиться цифры. Выбирают режим измерения рН, нажимая клавишу «mV/pH», на индикаторе справа символ «mV» должен смениться на символ «рН».
2. Анализируемый раствор получают в мерной колбе вместимостью 100,0 мл, доводят до метки и тщательно перемешивают. В стаканчик для титрования пипеткой помещают 10,00 мл анализируемого раствора кислоты, стержень магнитной мешалки и опускают электродную пару. При необходимости доливают дистиллированную воду так, чтобы электроды были погружены в раствор на 1 см.
3. Заполняют бюретку 0,1 н. раствором щелочи, включают магнитную мешалку и приступают к титрованию.
4. Ориентировочное титрование: добавляют щелочь порциями по 1 мл до рН не менее 12, записывая результаты измерения рН в таблицу:
V, мл | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
рН |
По данным таблицы строят интегральную кривую титрования в координатах рН - V и определяют примерный объем титранта (Х) в начале каждого скачка титрования.
рН
 |
 |

V
5. Точное титрование: новую аликвотную часть 10,00 мл анализируемого раствора помещают в стаканчик для титрования, заполняют бюретку до нулевой отметки, добавляют объем титранта, соответствующий началу первого скачка титрования (Х1) и приступают к точному титрованию, добавляя титрант порциями по 0,1 мл и записывая получаемые при этом значения рН. После прохождения первого скачка титрования (≈1-2 мл раствора титранта или рН не менее 7) добавляют объем титранта, соответствующий началу второго скачка титрования (Х2) и приступают к точному титрованию аналогично первому скачку.
Результаты точного титрования заносят в таблицы:
V, мл | рН | DV | DpH | V+1/2DV | DpH/DV |
|
Х1,0 | - | - | - | - | ||
0,11 | ||||||
,1 | ||||||
0,1 | ||||||
,2 | ||||||
0,1 | ||||||
,3 | ||||||
0,1 | ||||||
,4 | ||||||
0,1 | ||||||
,5 | ||||||
0,1 | ||||||
,6 | ||||||
0,1 | ||||||
,7 | ||||||
0,1 | ||||||
,8 | ||||||
0,1 | ||||||
,9 | ||||||
0,1 | ||||||
,0 | ||||||
0,1 | ||||||
,1 | ||||||
0,1 | ||||||
,2 | ||||||
0,1 | ||||||
,3 | ||||||
- | - | - | - |
V, мл | рН | DV | DpH | V+1/2DV | DpH/DV |
|
Х2,0 | - | - | - | - | ||
0,11 | ||||||
,1 | ||||||
0,1 | ||||||
,2 | ||||||
0,1 | ||||||
,3 | ||||||
0,1 | ||||||
,4 | ||||||
0,1 | ||||||
,5 | ||||||
0,1 | ||||||
,6 | ||||||
0,1 | ||||||
,7 | ||||||
0,1 | ||||||
,8 | ||||||
0,1 | ||||||
,9 | ||||||
0,1 | ||||||
,0 | ||||||
0,1 | ||||||
,1 | ||||||
0,1 | ||||||
,2 | ||||||
0,1 | ||||||
,3 | ||||||
- | - | - | - |
6. Строят дифференциальную кривую титрования в координатах DрН/DV – V+1/2DV и по максимуму на ней определяют точно первую и вторую точку эквивалентности (DрН – разность последующего и предыдущего значения рН). Построение интегральной и дифференциальной кривой можно выполнить на компьютере в программе «Обработка кривых потенциометрического титрования», разработанной в среде электронных таблиц «Excel».

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |




