, ,
, ,
ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Государственное образовательное учреждение высшего профессионального образования «Пятигорская государственная фармацевтическая академия»
Кафедра аналитической химии
, ,
,
ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Рабочая тетрадь
для студентов к занятиям
по аналитической химии в IV семестре
Пятигорск 2010
УДК 543.4'5 (076.5)
ББК 24.46я73
Ф50
Рецензенты: докт. хим. наук, проф. ;
академик РАО, проф.
, ,
, ,
Ф 50 Физико-химические методы анализа: рабочая тетрадь для студентов к занятиям по аналитической химии в IV семестре / [и др.]. – Пятигорск: Пятигорская ГФА, 2010. – 52 с.
Рабочая тетрадь к циклу лабораторных работ по физико-химическим методам анализа предназначена студентам 2 курса очного отделения фармацевтической академии для подготовки и выполнения лабораторных работ по аналитической химии в соответствии с учебным планом и «Примерной программой по дисциплине аналитическая химия» (М.: Минобразование России, 2002.) специальности 060108 «Фармация». Приведены образцы решения задач, образцы оформления отчета о проделанной работе, список литературы.
Рекомендовано для использования в учебном процессе на кафедре аналитической химии ПУМК по химическим дисциплинам Минздравсоцразвития РФ, июнь, 2007 г.
УДК 543.4'5 (076.5)
ББК 24.46я73
ãПятигорская государственная фармацевтическая академия, 2010
Оптические методы анализа
Лабораторная работа № 1
Фотоэлектроколориметрическое определение никеля (II) реакцией с диметилглиоксимом в присутствии окислителей
СУЩНОСТЬ РАБОТЫ: Определение никеля основано на измерении интенсивности красно-бурой окраски растворов, образующейся при взаимодействии никеля(II) с диметилглиоксимом в щелочных растворах в присутствии окислителей.
В условиях проведения реакции происходит окисление никеля, вероятно до никель(III). Определение состава соединения указывает на соотношение Ni: DimГ = 1:3. Для соединения образующегося в щелочной среде, lmax = 470 нм, Е = 1,3.104. В качестве окислителей могут применяться иод, бром, персульфат, пероксид водорода и т. д. Лучше всего использовать иод, так как в его присутствии не окисляется избыток диметилглиоксима. Определению мешают вещества, имеющие собственную окраску и катионы, образующие гидроксиды в щелочной среде.
Реактивы: нитрат никеля Ni(NO3)2.6H2O;
иод 0,05 М раствор;
диметилглиоксим 1% раствор в 20% растворе щелочи;
гидроксид натрия, 1 н. раствор;
HCl конц.;
H2SO4 конц.
Лабораторная посуда: Бюретки на 25 мл;
Пипетки градуированные на 10 и 5 мл;
Колбы мерные вместимостью 100 и 50 мл.
Приборы: Колориметр концентрационный КФК-2.
ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ:
1. Приготовление 100 мл стандартного раствора, содержащего 0,1 мг/мл никеля (раствор «А»).
Для приготовления стандартного раствора берут точную навеску Ni(NO3)2.6H2O, равную вычисленной по формуле:
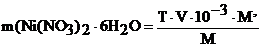 (г), где
(г), где
Т – титр стандартного раствора – 0,1 мг/мл;
V – объем раствора – 100 мл;
М’ – молярная масса соли Ni(NO3)2*6H2O (290,79 г/моль);
М – молярная масса никеля (58,69 г/моль);
10-3 – коэффициент перевода мг в г.
Взятую на аналитических весах навеску количественно переносят в мерную колбу вместимостью 100 мл, растворяют в небольшом количестве воды, добавляют 0,2 мл концентрированной серной кислоты, объем доводят до метки и тщательно перемешивают. Получают раствор А.
2. Приготовление стандартного раствора с содержанием никеля(II) 0,01 мг/мл (раствор Б).
Раствор Б готовится в день употребления. В мерную колбу вместимостью 100 мл отмеривают по бюретке 10 мл раствора с Т = 0,1 мг/мл (раствора «А»), добавляют 2 капли конц. HCl, очищенную воду до метки и тщательно перемешивают.
3. Приготовление эталонных растворов.
В 5 мерных колб вместимостью 50 мл вносят, отмеривая по бюретке 2, 4, 6, 8, 10 мл стандартного раствора с Т = 0,01 мг/мл (раствор Б). Затем в каждую колбу добавляют 1 каплю HCl (1:1), 1 мл раствора йода, 5 мл 1 н. NaOH и 1 мл раствора диметилглиоксима. Полученную смесь доводят водой до метки и тщательно перемешивают.
4. Приготовление раствора сравнения.
В мерную колбу вместимостью 50 мл вносят, сливая по бюретке, 5 мл дистиллированной воды, 1 каплю HCl (1:1), 1 мл раствора йода, 5 мл 1 н. NaOH и 1 мл раствора диметилглиоксима. Полученную смесь доводят водой до метки и тщательно перемешивают.
5. Выбор светофильтра.
Эта операция необходима для выбора диапазона длин волн, где ошибка в определении содержания Ni(III) будет наименьшей. Берут эталонный раствор № 3, помещают в кювету с толщиной поглощающего слоя (![]() ) 3 см и производят измерение светопоглощения (оптической плотности, А) на всех светофильтрах (при всех длинах волн, l) относительно раствора сравнения. Результаты измерений заносят в таблицу № 1.
) 3 см и производят измерение светопоглощения (оптической плотности, А) на всех светофильтрах (при всех длинах волн, l) относительно раствора сравнения. Результаты измерений заносят в таблицу № 1.
Таблица № 1
Выбор светофильтра (lmax). Эталонный раствор Ni(II) № 3 (Т = 1,2*10‑3 мг/мл). Фотоколориметр КФК-2; ![]() = 3 см;
= 3 см; ![]() = 50 мл.
= 50 мл.
Номер светофильтра | l | Аi |
1 | 315 нм | |
2 | 364 нм | |
3 | 400 нм | |
4 | 440 нм | |
5 | 490 нм | |
6 | 540 нм |
По полученным данным строят кривую (спектр поглощения) в координатах «светопоглощение (А) - № светофильтра (l)» (рис. 1).
Отмечают участок кривой, для которого выполняются следующие условия:
1) Светопоглощение имеет наибольшую величину.
2) Ход кривой примерно параллелен горизонтальной оси (абсцисс).
![]() А
А





 1,0-
1,0-
-
 0,8-
0,8-
-
 0,6-
0,6-
-
 0,4-
0,4-
-
 0,2-
0,2-
-
![]() 0 - | | l, нм
0 - | | l, нм
Рис. 1. Спектр поглощения комплексного соединения Ni(II) с ДimГ в щелочном растворе в присутствии йода.
6. Измерение светопоглощения (оптической плотности) эталонных растворов и построение градуировочного графика.
Приготовленные 5 эталонных растворов фотоколориметрируют при выбранном светофильтре (lmax) в кювете с толщиной поглощающего слоя 3 см относительно раствора сравнения. Результаты измерений (Аi) заносят в таблицу № 2. Рассчитывают для каждого эталонного раствора титр по формуле: ![]() , молярную концентрация (Сi, моль/л) по формуле:
, молярную концентрация (Сi, моль/л) по формуле: 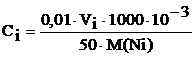 и массовую долю (ω, %) по формуле:
и массовую долю (ω, %) по формуле: 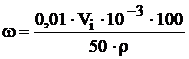 , где 0,01 - титр раствора Б; Vi – объем раствора Б; 1000 – 1 л раствора; 50 – вместимость мерной колбы; 10-3 – коэффициент пересчета мг в г; M(Ni) – молярная масса никеля; 100 – 100 г раствора; r - плотность раствора ~ 1 г/мл.
, где 0,01 - титр раствора Б; Vi – объем раствора Б; 1000 – 1 л раствора; 50 – вместимость мерной колбы; 10-3 – коэффициент пересчета мг в г; M(Ni) – молярная масса никеля; 100 – 100 г раствора; r - плотность раствора ~ 1 г/мл.
Таблица № 2
Светопоглощение эталонных растворов никеля(II)
№ эталонного раствора | Объем стандартного раствора (р-ра Б), Vi, мл | Титр эталонного раствора (Ti), мг/мл | Сi моль/л | ωi, % | Аi |
|
|
1 | 2 | 0,4*10-3 | |||||
2 | 4 | 0,8*10-3 | |||||
3 | 6 | 1,2*10-3 | |||||
4 | 8 | 1,6*10-3 | |||||
5 | 10 | 2,0*10-3 | |||||
Средние значения: |
По данным таблицы № 2 строят градуировочный график, откладывая на 3-х осях абсцисс титр никеля(II) в эталонных растворах (мг/мл), Сi (моль/л) и ω (%), а на оси ординат – светопоглощение (А) (рис. 2).
А






![]() 1,2-
1,2-
 1,0-
1,0-
 0,8-
0,8-
 0,6-
0,6-
 0,4-
0,4-
 0,2-
0,2-
![]() 0 | | | | |
0 | | | | |
0 0,4 0,8 1,2 1,6 2,0 Ti.103, мг/мл
0 0,68 1,36 2,04 2,73 3,4 С.105, моль/л
ω.105 , %
Рис. 2. Градуировочный график для определения содержания Ni(II) в растворе.
При соблюдении закона Бугера-Ламберта-Бера получают прямую линию, проходящую через начало координат.
7. Вычисление молярного и удельного коэффициентов поглощения диметилглиоксимата никеля.
Для каждого эталонного раствора рассчитывают ![]() и
и ![]() , затем рассчитывают средние значения молярного и удельного коэффициентов поглощения диметилглиоксимата никеля по данным таблицы № 2. Формулы расчета:
, затем рассчитывают средние значения молярного и удельного коэффициентов поглощения диметилглиоксимата никеля по данным таблицы № 2. Формулы расчета:
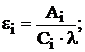
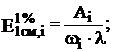 где
где
Аi– светопоглощение i-того эталонного раствора;
Сi – молярная концентрация i-того эталонного раствора, моль/л;
l – толщина поглощающего слоя, см;
ωi – массовая доля никеля в i-том эталонном растворе, %.
8. Приготовление раствора с неизвестной концентрацией (контрольного раствора).
В мерную колбу вместимостью 50 мл, содержащую неизвестное количество никеля(II), последовательно добавляют те же реагенты и в тех же количествах, что и для приготовления эталонных растворов. Измеряют светопоглощение (Ах) приготовленного раствора в кювете с l = 3 см относительно раствора сравнения.
9. Определение содержания никеля(II) в анализируемом (контрольном) растворе с помощью градуировочного графика.
9.1. По градуировочному графику находят титр анализируемого раствора (Тх, мг/мл), который соответствует светопоглощению Ах и рассчитывают массу никеля(II) в анализируемом растворе по формуле:
m(Ni) = (Tx * V), мг
где V – общий объем анализируемого раствора (50 мл).
9.2. По градуировочному графику находят молярную концентрацию никеля(II) в анализируемом растворе (Сх, моль/л), которая соответствует оптической плотности Ах и рассчитывают массу никеля(II) в анализируемом растворе по формуле: 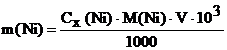 , мг.
, мг.
9.3. По градуировочному графику находят массовую долю никеля(II) в анализируемом растворе (ωx, %), которая соответствует оптической плотности Ах и рассчитывают массу никеля(II) в анализируемом растворе по формуле: 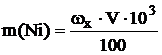 , мг
, мг
10. Определение содержания массы никеля(II) по среднему молярному и среднему удельному коэффициентам поглощения (![]() и
и ![]() ). Зная Ах и
). Зная Ах и ![]() или Ах и
или Ах и ![]() можно рассчитать массу никеля по формулам:
можно рассчитать массу никеля по формулам:
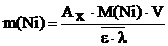 , мг или
, мг или 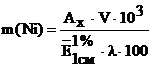 , мг
, мг
где V – общий объем анализируемого раствора (50 мл); 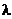 = 3 см; 103 – коэффициент пересчета г в мг.
= 3 см; 103 – коэффициент пересчета г в мг.
Для уменьшения погрешности определения концентрации, связанной с неточностями при ручном построении градуировочного графика, его наилучшие параметры можно рассчитать по методу наименьших квадратов.
Представим уравнение прямой в виде у=а+bх, где у – аналитический сигнал (оптическое светопоглощение А), х – концентрация (выраженная в моль/л или в % или в виде титра, г/мл), а и b – константы. Наилучшие значения а и b вычисляют по формулам:
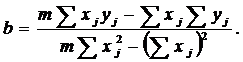 где j – номер точки, m – общее количество точек.
где j – номер точки, m – общее количество точек.
Для оценки погрешности в определении а и b вычисляют:
Стандартное отклонение точек от найденной зависимости
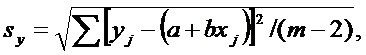
Стандартное отклонение рассчитанного значения наклона (b) градуировочной зависимости:
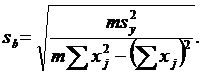
Стандартное отклонение рассчитанного значения отрезка, отсекаемого на оси ординат (а):

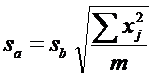
Границы доверительного интервала рассчитанного значения наклона регрессионной зависимости обозначают ±Δb. Границы доверительного интервала, соответствующего уровню доверительной вероятности P:
Δb = tp,f .sb.
Границы доверительного интервала для рассчитанного значения отрезка, отсекаемого на оси ординат обозначают ±Δa. Границы доверительного интервала, соответствующего уровню доверительной вероятности P:
Δa = tp,f .sa.
Если при этом а будет < Δa, то значение а считают незначимым и переходят к уравнению прямой вида у=b’x. Значение b’ рассчитывают по формуле: 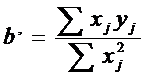 , стандартное отклонение точек от найденной зависимости
, стандартное отклонение точек от найденной зависимости 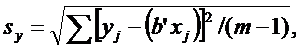 и стандартное отклонение рассчитанного значения наклона регрессионной зависимости:
и стандартное отклонение рассчитанного значения наклона регрессионной зависимости: 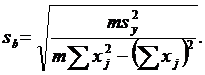
Границы доверительного интервала (±Δb), соответствующего уровню доверительной вероятности Р: Δb = tp,f .sb.
Погрешность определения концентрации х, определяемой по градуировочному графику, зависит от следующих параметров: числа параллельных измерений уj, равное n, числа точек на графике m, разброса точек относительно прямой, мерой которого служит sу, и удаленности значения у от среднего значения ![]() на графике, то есть центра графика. Стандартное отклонение концентрации рассчитывают по уравнению:
на графике, то есть центра графика. Стандартное отклонение концентрации рассчитывают по уравнению:
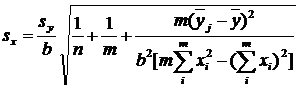 , а доверительный интервал Δх = sх. tР, f.
, а доверительный интервал Δх = sх. tР, f.
Расчет по этим формулам можно провести с использованием компьютера.
О Т Ч Е Т
Определение никеля с диметилглиоксимом в присутствии окислителя методом прямой фотометрии
1. Метод анализа:
2. Метод фотометрического определения:
2.1. по градуировочному графику (графически и по уравнению прямой)
2.2. расчетный (по значению ![]() и Е
и Е![]() )
)
3. Определяемое вещество:
4. Анализируемое вещество:
5. Реагент:
6. Вспомогательное вещество:
7. Уравнения реакций, лежащих в основе определения:
7.1. 3I2 + 6OH- ® IO3- + 5I- + 3H2O
7.2. IO3- + 6Ni2+ + 3H2O ® 6Ni3+ + I - + 6OH-
7.3. Ni3+ + 3H2R + 3OH - ® 2[Ni(HR)3]o + 3H2O
-------
2Ni2+ + I2 + 6H2R + 6OH - ® 2[Ni(HR)3]o + 2I - + 6H2O
8. Фотометрические характеристики комплексного соединения – продукта фотометрической реакции [Ni(HR)3]o
lmax = ; ![]() = ; Е
= ; Е![]() =
=
9. Чувствительность (предел) определения (при А = 0,05)
9.1. по градуировочному графику
……. мг/мл; ……. моль/л; ……. %
9.2. по значениям ![]() и
и ![]() : С(Ni2+)min =
: С(Ni2+)min = ![]() ;
;
С(Ni2+)min = 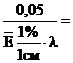
10. Чувствительность градуировочного графика
tg a = b =
11. Интервал определяемых содержаний Ni2+ в растворе (по прямолинейности градуировочного графика) при l = ……… и ![]() = 3,0 см.
= 3,0 см.
1) ……… - ………, мг/мл; 2) ……… - ………, моль/л
3) ……… - ………, %
12. Светопоглощение контрольного раствора Ах = ……….
13. Содержание никеля в контрольном растворе:
13.1. по градуировочному графику: ..........;
по Тх ……. мг; по Сi ……. мг; по ωi ……. мг
13.2. по значению e: ……….. мг; по значению Е![]() : ……….. мг.
: ……….. мг.
14. Среднее содержание никеля в контрольном растворе: .……….. мг.
15. Истинное содержание никеля в контрольном растворе: ………. мг.
16. Относительная погрешность определения …………….……….. %.
Лабораторная работа № 2.
Дифференциальное фотоэлектроколориметрическое определение
железа(III) с сульфосалициловой кислотой в кислой среде
Сущность лабораторной работы.
Определение основано на образовании в кислой среде окрашенного в фиолетовый цвет моносульфосалицилата железа(III) состава 1:1.
Для соединения образующегося в кислой среде lmax = 510 нм, Е = 1,8.103. В качестве раствора сравнения используют моносульфосалицилат железа(III) известной концентрации.
Концентрацию железа(III) в исследуемом растворе определяют либо при помощи градуировочного графика, либо с использованием фактора пересчета (F), концентрация железа(III) в исследуемом растворе и в эталонных растворах должна быть больше, чем в растворе сравнения.
Реактивы: железо-аммонийные квасцы
сульфосалициловая кислота, 10% раствор
кислота серная, концентрированная
кислота серная, 1 М раствор.
Лабораторная посуда: колбы мерные, вместимостью 100 и 25 мл
бюретки
пипетки, емкостью 10 мл.
Приборы: фотоколориметр КФК-2.
Методика выполнения лабораторной работы:
1. Приготовление стандартного раствора, содержащего 1 мг/мл железа (III).
Для приготовления раствора берут навеску железо-аммонийных квасцов, точно равную рассчитанной по формуле:
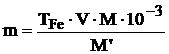 ,
,
где:
m – навеска
Т – титр железа(III), мг/мл
V – общий объем стандартного раствора железа(III), мл
М – молярная масса железа, г/моль
М’ – молярная масса NH4Fe(SO4)2.12H2O, г/моль.
Навеску, взвешенную на аналитических весах, количественно переносят в мерную колбу, емкостью 100 мл, растворяют при нагревании в небольшом количестве дистиллированной воды с добавкой 1 мл концентрированной серной кислоты. После охлаждения объем раствора доводят до метки водой и тщательно перемешивают.
2. Приготовление эталонных растворов.
В шесть мерных колб емкостью 25 мл вводят из бюретки последовательно 3,0; 3,9; 4,8; 5,7; 6,6; 7,5 мл стандартного раствора соли железа(III), содержащего 1 мг/мл железа. Затем в каждую колбу добавляют по 3 мл 3% раствора сульфосалициловой кислоты и по 1 мл 1 М раствора серной кислоты, разбавляют дистиллированной водой, доводят до метки и тщательно перемешивают.
3. Измерение светопоглощения (оптической плотности) эталонных растворов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |




