2. Метод:
3. Основное уравнение метода:
4. Схема определения:
5. Титрант:
6. Прием титрования:
7. Способ определения:
8. Уравнение электрохимической реакции:
9. Уравнение химической реакции:
10. Расчет fэкв(А) и Э(А):
11. Расчет g(А):
12. Относительная погрешность определения Е%:
Работа 2. Определение тиосульфата натрия.
Определение тиосульфата натрия основано на его титровании электрогенерированным иодом. В качестве вспомогательного реагента служит иодид калия, который берут в большом избытке по отношению к определяемому веществу. В процессе электролиза из вспомогательного реагента на генераторном платиновом аноде образуется свободный иод (электрогенерированный титрант): на аноде: 2I– – 2e– = I2
На вспомогательном электроде (катоде) выделяется водород:
на катоде: 2H2O + 2e– = H2 + 2OH–
Образующиеся в растворе гидроксид-ионы необходимо нейтрализовывать, для чего в раствор перед титрованием добавляют 1-2 мл 0,01 М раствора серной кислоты. Образующийся иод реагирует в растворе с тиосульфат-ионами:
I2 + 2S2O32- = 2I– + S4O62–
После окисления всего количества тиосульфат-ионов в растворе появляется свободный иод, образующий с крахмалом синее окрашивание.
Приборы и реактивы:
Кулонометрическая установка с электронным секундомером
Магнитная мешалка
Генераторный платиновый электрод
Вспомогательный платиновый электрод
Мерная колба вместимостью 100 мл
Пипетка вместимостью 10 мл
Иодид калия или аммония, 0,1 М раствор
Крахмал 1% раствор
Серная кислота 0,01 М раствор
Выполнение работы: Исследуемый раствор тиосульфата натрия разбавляют в мерной колбе вместимостью 100 мл до метки и хорошо перемешивают. В стакан для титрования помещают примерно 10 мл 0,1 М раствора КI, 1-2 мл раствора крахмала и 1-2 мл 0,01 М раствора серной кислоты, опускают платиновые электроды и стержень магнитной мешалки.
При выключенном тумблере «Ячейка» ручкой «Ток» устанавливают ток электролиза 15 мА и включают магнитную мешалку. Сначала проводят предварительный электролиз фонового раствора током 15 мА, включив на некоторое время тумблер «Ячейка». При появлении синей окраски раствора тумблер «Ячейка» выключают. Затем в стакан с электродами пипеткой добавляют 10,00 мл анализируемого раствора тиосульфата натрия, на микрокалькуляторе, служащем электронным секундомером, нажимают клавиши «С», «+» и «1», а затем включают ячейку и записывают фактический ток электролиза. После появления синей окраски раствора такой же интенсивности, как и при предварительном электролизе, выключают ячейку и записывают время окончания титрования с точностью до 1 сек. Рассчитывают количество прошедшего электричества по формуле:
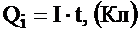 , где I - ток электролиза, t - время электролиза, с.
, где I - ток электролиза, t - время электролиза, с.
Титрование повторяют дважды, добавляя аликвотную часть (10,00 мл) анализируемого раствора тиосульфата натрия в тот же стакан, и рассчитывают среднее количество электричества, затраченного на электролиз: Qср. = (Q1 + Q2 + Q3)/3.
Содержание тиосульфата натрия (g) рассчитывают по формуле:

где Q – количество электричества, Кл
М – молярная масса Na2S2O3·5H2O, г/моль (М = 248,17 г/моль)
W – вместимость мерной колбы, мл (100 мл)
V – вместимость пипетки, мл (10 мл)
F – константа Фарадея, 96485 Кл/моль
n – число электронов (для тиосульфата натрия n = 1).
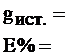
О Т Ч Е Т
Определение тиосульфата натрия.
1. Анализ:
2. Метод:
3. Основное уравнение метода:
4. Схема определения:
5. Титрант:
6. Прием титрования:
7. Способ определения:
8. Уравнение электрохимической реакции:
9. Уравнение химической реакции:
10. Расчет fэкв(А) и Э(А):
11. Расчет g(А):
12. Относительная погрешность определения Е%:
АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Работа 3. Определение содержания сульфата железа (II)
методом амперометрического титрования
Определение сульфата железа(II) методом амперометрического титрования основано на титровании его стандартным раствором дихромата калия с индикацией точки эквивалентности по току окисления ионов Fe2+ на платиновом электроде. В процессе титрования на электроде протекает электродная реакция: Fe2+ - e - = Fe3+ , a в растворе химическая реакция: 6Fe2+ + Cr2O72– + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O
За счет протекания химической реакции концентрация ионов Fe2+ в растворе в процессе титрования уменьшается, следовательно, уменьшается и ток, величина которого пропорциональна концентрации. После завершения химической реакции величина тока остается постоянной, поэтому момент прекращения уменьшения тока, определяемый как точка пересечения двух прямых на кривой титрования, и будет соответствовать точке эквивалентности. Так как индикаторный электрод имеет маленькую площадь, доля электрохимического окисления железа по сравнению с химическим пренебрежимо мала, и содержание железа в растворе можно рассчитать по обычной формуле титриметрического анализа.
Выполнение работы на амперометрической установке АУ-4М.
1. Включают вилку прибора в сеть и переводят тумблер «Сеть» в положение «Вкл», на передней панели должна загореться индикаторная лампочка.
2. Рукояткой «наложение» устанавливают напряжение 1,2 В.
3. В стаканчик для титрования помещают 10,00 мл анализируемого раствора, стержень магнитной мешалки, добавляют ≈10 мл 12,5% раствора серной кислоты и опускают в стакан электродную пару. При необходимости доливают дистиллированную воду таким образом, чтобы электроды были погружены в раствор на 1 см.
4. Заполняют бюретку 0,01 н. раствором дихромата калия до нулевой отметки, включают магнитную мешалку ручкой «мотор» и приступают к титрованию, установив ручку «время между титрованиями» в положение 15 сек. При необходимости остановить процесс титрования эту ручку переводят в положение «выкл».
5. Результаты титрования запишите в таблицу:
V, мл | ||||||||||||||||||||||||
I, мкА |
Титрование заканчивают тогда, когда получатся 3-4 примерно постоянных значения величины тока. По данным таблицы строят кривую титрования в координатах I - V и определяют объем титранта в точке эквивалентности, соответствующий точке пересечения двух прямых.










![]() I
I
V

6. Повторяют титрование еще раз, начиная с п.3, и рассчитывают среднее значение двух определений.
V, мл | ||||||||||||||||||||||||
I, мкА |










![]() I
I
V

7. Рассчитывают содержание FeSO4.7H2O в растворе (g) в граммах по формуле:
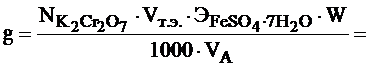
О Т Ч Е Т
Определение содержания сульфата железа (II)
методом амперометрического титрования
1. Анализ:
2. Метод:
3. Основное уравнение метода:
4. Схема определения:
5. Титрант:
6. Прием титрования:
7. Способ определения:
8. Уравнение электрохимической реакции:
9. Уравнение химической реакции:
10. Расчет fэкв(А) и Э(А):
11. Расчет g(А):
12. Относительная погрешность определения Е%:
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Работа 4. Определение содержания CH3COOH методом потенциометрического титрования
Метод потенциометрического титрования основан на экспериментальном определении рН в процессе титрования с последующим определением точки эквивалентности по кривой титрования, построенной в дифференциальной форме. Значения рН в процессе титрования измеряют на рН-метре с помощью индикаторного стеклянного электрода в паре с хлоридсеребряным электродом сравнения.
Выполнение работы.
1. Включают прибор в сеть и нажимают клавишу «On/Off» на панели рН-метра. На индикаторе должны появиться цифры. Выбирают режим измерения рН, нажимая клавишу «mV/pH», на индикаторе справа символ «mV» должен смениться на символ «рН».
2. Анализируемый раствор получают в мерной колбе вместимостью 100,0 мл, доводят до метки и тщательно перемешивают. В стаканчик для титрования пипеткой помещают 10,00 мл анализируемого раствора кислоты, стержень магнитной мешалки и опускают электродную пару. При необходимости доливают дистиллированную воду так, чтобы электроды были погружены в раствор на 1 см.
3. Заполняют бюретку 0,1 н. раствором щелочи, включают магнитную мешалку и приступают к титрованию.
4. Ориентировочное титрование: добавляют щелочь порциями по 1 мл до рН не менее 11, записывая результаты измерения рН в таблицу:
V, мл | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
рН |
По данным таблицы строят интегральную кривую титрования в координатах рН - V и определяют примерный объем титранта (Х) в начале скачка титрования.
рН
 |
 |

V
5. Точное титрование: новую аликвотную часть 10,00 мл анализируемого раствора помещают в стаканчик для титрования, заполняют бюретку до нулевой отметки, добавляют объем титранта, соответствующий началу скачка титрования (Х) и приступают к точному титрованию, добавляя титрант порциями по 0,1 мл и записывая получаемые при этом значения рН.
Результаты заносят в таблицу и рассчитывают изменение рН (DрН – разность последующего и предыдущего значения рН) на единицу объема титранта (заполняют все столбцы таблицы):
V, мл | рН | DV | DpH | V+1/2DV | DpH/DV |
|
Х,0 | - | - | - | - | ||
0,11 | ||||||
,1 | ||||||
0,1 | ||||||
,2 | ||||||
0,1 | ||||||
,3 | ||||||
0,1 | ||||||
,4 | ||||||
0,1 | ||||||
,5 | ||||||
0,1 | ||||||
,6 | ||||||
0,1 | ||||||
,7 | ||||||
0,1 | ||||||
,8 | ||||||
0,1 | ||||||
,9 | ||||||
0,1 | ||||||
,0 | ||||||
0,1 | ||||||
,1 | ||||||
0,1 | ||||||
,2 | ||||||
0,1 | ||||||
,3 | ||||||
- | - | - | - |
6. Строят дифференциальную кривую титрования в координатах DрН/DV – V+1/2DV и по максимуму на ней определяют точно точку эквивалентности.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |




