1) экстинкция;
2) удельный коэффициент экстинкции;
3) толщина поглощающего слоя;
4) поглощение;
5) молярный коэффициент экстинкции
6) абсорбция
) А;
) Т;
) ε;
) Е;
е) l.
3. Молярный и удельный коэффициенты экстинкции зависят от:
a) природы поглощающей среды;
b) частоты поглощаемого света;
c) температуры;
d) толщины поглощающего слоя.
4. Экстинкция смеси веществ, не взаимодействующих между собой и подчиняющихся закону светопоглощения (при λ=const и l=const), равна:
a) экстинкции компонента в преобладающей концентрации;
b) сумме экстинкций компонентов.
5. Установить соответствие между областью электромагнитного спектра и интервалом длин волн:
1) ИК; а) 185 – 390 нм;
2) микроволновая; b) 0,76 - 1000 мкм;
3) рентгеновская; c) 390 – 760 нм;
4) УФ; d) 0,1 – 10 см;
5) видимая; e) ›10 -12 м.
II. Семинар «Токсикологическая характеристика парацетамола Спектрофотометрический анализ».
Образцы вопросов и задач, входящих в карточки индивидуального задания:
1. Каковы механизмы биотрансформации парацетамола?
2. Напишите реакцию дезацетилирования парацетамола. Назовите органы-мишени образующегося метаболита?
3. Прогнозируйте продукты окисления парацетамола при биотрансформации. Какие ферменты катализируют эти процессы? Назовите первичные органы-мишени продуктов биоокисления парацетамола.
4. Какие продукты второй фазы биотрансформации парацетамола известны? Запишите реакции их образования.
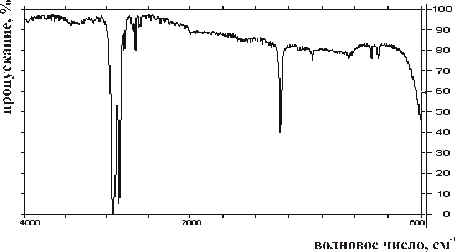
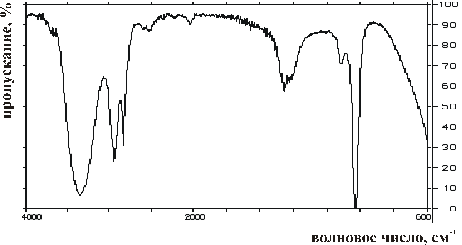
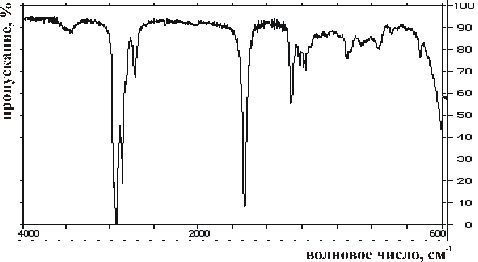
Задание 1. Произошло отравление одним из трех органических веществ. Известно, что среди них есть метанол CH3OH, циклогексан C6H12 и октаналь C8H16O. Предварительные клинические признаки свидетельствуют об отравлении метанолом.
1) Используя полученные ИК-спектры испытуемых веществ, идентифицируйте предполагаемый яд;
2) Ответ обоснуйте, сделав отнесение характеристических полос, соответствующих разным функциональным группам (см. Приложение12.3).
1.
2. |
3
|
Задание 2. На одежде предполагаемого преступника была обнаружена органическая жидкость, ИК-спектр которой представлен ниже. Место преступления сильно загрязнено смесью углеводородов, среди которых не были обнаружены следы кетонов, альдегидов, кислот и спиртов.
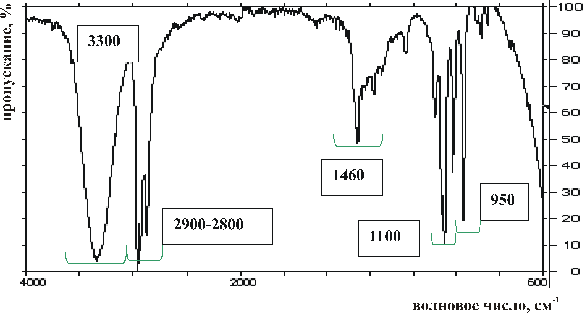
Используя ИК-спектр органического вещества с одежды подозреваемого, дайте заключение:
0) загрязнена ли одежда подозреваемого в преступлении углеводородным растворителем;
1) идентичны ли растворители на одежде и на месте преступления.
Для ответа на вопросы сделайте отнесение полос на ИК – спектре органической жидкости, найденной на одежде предполагаемого преступника (см. Приложение 12.3. 12.3).
III. Лабораторная работа: Химико-токсикологический анализ таблеток, найденных на месте происшествия (на примере парацетамола)
В лабораторию для проведения химико-токсикологического анализа с места происшествия поступил образец – белый порошок. По словам пострадавшего, для снятия симптомов простуды им было принято лекарственное средство, хранившееся в домашней аптечке и использованное ранее с этой же целью.
Предварительные скрининговые испытания позволили предположить, что исследуемый порошок – парацетамол.
Проведите следующие подтверждающие испытания:
1. Качественный анализ порошка
- Укажите цвет, фазовое состояние (аморфный или кристаллический), запах, растворимость в воде, растворе щелочи, эфире и этаноле лекарственного вещества исследуемого образца; Проведите кислотный гидролиз лекарственного вещества с последующим окислением K2Cr2O7 и укажите окраску испытуемой пробы. Запишите соответствующие химические реакции; Для идентификации парацетамола в биопробе проведите извлечение из подкисленного раствора хлороформом. ТСХ система хлороформ:этанол (99:1). Проявите 5%– ным FeCl3 (синее окрашивание пятен); Получите УФ– спектр 0,0008 %-ного водного раствора исследуемого порошка в интервале длин волн от 200 до 400 нм.
Методика
1. Около 0,045 г (точная навеска) исследуемого порошка поместите в мерную колбу вместимостью 100 мл; добавьте 60 мл воды, перемешайте в течение 10 мин, доведите объем раствора водой до метки.
2. Один мл полученного раствора поместите в мерную колбу вместимостью 50 мл, доведите объем раствора водой до метки и перемешайте.
3. Получите спектр поглощения исследуемого раствора в интервале длин волн 200 – 400 нм, используя кварцевую кювету толщиной 10 мм.
4. Наличие полосы поглощения с максимумом при 243 нм позволяет сделать вывод, что исследуемый порошок содержит парацетамол.
2. Количественный анализ
Измерения проводят с использованием раствора рабочего стандартного образца (РСО).
Методика
1. Для приготовления рабочего стандартного образца около 0,04 г (точная навеска) стандартного образца парацетамола поместите в мерную колбу вместимостью 100 мл, добавьте 60 мл воды, перемешайте до растворения, доведите объем раствора водой до метки;
2. Один мл полученного раствора перенесите в мерную колбу вместимостью 50 мл и вновь доведите объем раствора до метки;
3. На спектрофотометре СФ – 201 (или любом ином):
o Введите программу “Фотометрическое измерение” (режим-Fotometr);
o Установите нулевой образец (воду очищенную) на позицию “0” кюветного держателя;
o Закройте крышку камеры и нажмите кнопку “Измерения”;
o Установите кюветы с РСО парацетамола и исследуемым образцом на соответствующие позиции (№1 и №2) кюветодержателя;
o Поочередно выделяйте на дисплее прибора (в правом нижнем углу) нужную позицию кюветодержателя с нажатием кнопки “Измерение”;
o Снимите показания поглощения А раствора стандартного образца и исследуемого раствора парацетамола;
o Рассчитайте содержание лекарственного вещества (%) в исследуемом порошке парацетамола.
Сделайте заключение по результатам эксперимента, в котором укажите:
1. Парацетамол является (не является) действующим лекарственным веществом в исследуемом порошке, обнаруженном на месте происшествия.
2. Содержание действующего вещества в испытуемом образце составляет 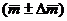 г.
г.
Литература
1. Материалы лекций.
2. Биоорганическая химия: Учебник для вузов / , – М.: Дрофа, 2004. – С.513-518.
3. Электронные спектры в органической химии / . – М.: Химия, 1973. – С.18-32.
4. Аналитическая химия / Т. 2. – М.: Высш. шк., 2001.С. 307-341.
5. Энциклопедия лекарств. – М.: 2005. – С.686-687.
6. European Pharmacopoeia 4TH Edition, 2002. – С. 34-37.
2. Атомно-абсорбционная спектрометрия, атомно-эмиссионная спектрометрия с индуктивно-связанной плазмой
Структура занятия:
I. Входной тест.
II. Семинар: основные принципы атомной спектрометрии. Способы минерализации биологических материалов при элементном анализе.
III. Лабораторная работа «Определение цинка в волосах человека методом ААС».
Целевые задачи:
- познакомиться с принципиальными схемами атомно-абсорбционного и атомно-эмиссионного спектрометров.
- освоить методику количественного определения элементов в волосах человека методом атомно-абсорбционной спектрометрии.
Краткое теоретическое введение
Для изучения содержания s-, p - и d-элементов в организме человека в норме и при отравлениях широко используются методы атомно-абсорбционной спектрометрии (ААС) и атомно-эмиссионной спектрометрии с индуктивно-связанной плазмой (АЭС-ИСП), отличающиеся высокой чувствительностью, низким пределом обнаружения и пределом количественной оценки. Методы позволяют в одной пробе биосубстрата (волосы, ногти, кровь, моча, продукты питания и др.) одновременно определить содержание десятков химических элементов, что очень важно для характеристики их взаимного влияния и комбинированного воздействия на биохимические процессы в организме.
Атомно-абсорбционная спектрометрия (ААС).
Впервые использование атомных спектров поглощения для спектрального анализа было предложено в 1955 г. С этого времени началось развитие атомно-абсорбционной спектрофотометрии как нового метода аналитической химии, характеризующегося высокой чувствительностью и селективностью, простотой выполнения и, сравнительно с эмиссионными методами анализа, значительно меньшим числом эффектов, мешающих анализу. В настоящее время одной из крупнейших фирм в области аналитического приборостроения Varian Inc. (США) принадлежит более 70% ключевых патентов в области атомной абсорбции.
Метод ААС основан на явлении селективного поглощения свободными атомами ультрафиолетового и видимого излучения характеристических частот. Через слой атомных паров пробы, получаемых с помощью атомизатора, пропускают излучение в диапазоне 190-850 нм. В результате поглощения квантов света атомы переходят в возбужденные энергетические состояния (рис.13.1).
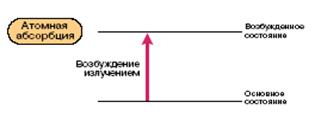
Рис.13.1. Возбуждение атомов элементов при поглощении квантов света.
Этим переходам в атомных спектрах соответствуют так называемые резонансные линии, характерные для данного элемента. Мерой концентрации элемента служит абсорбция A = lg(I0/I), где I0 и I-интенсивности излучения от источника соответственно до и после прохождения через поглощающий слой (закон Бугера-Ламберта-Бера).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |