c) длины хроматографической колонки
d) температуры
10. Жидкостная хроматография основана на теории:
а) обратимого и стехиометрического обмена ионами
b) абсорбции света
c) адсорбции вещества из раствора
d) различия в размерах молекул
11. Селективность адсорбции зависит от:
а) энергии взаимодействия между веществом и адсорбентом
b) диффузии вещества в слое сорбента
с) подвижности вещества
d) растворимости компонентов разделяемой смеси в подвижной и неподвижной фазах
12. Эффективность хроматографической колонки зависит от:
а) коэффициентов диффузии в обеих фазах
b) длины колонки
c) диаметра колонки
d) давления при вводе пробы
e) хорошей растворимости компонентов в подвижной фазе
13. Эффективность хроматографической колонки возрастает с:
а) уменьшением высоты теоретической тарелки (ТТ)
b) увеличением высоты ТТ
с) увеличением числа ТТ
d) уменьшением числа ТТ
14. Основные узлы приборов ВЭЖХ:
а) блок питания
b) колонка
с) резервуар с растворителем
d) насос высокого давления
е) секундомер
f) дозатор
g) детектор
h) термостат
15. Требования, предъявляемые к адсорбентам в ВЭЖХ:
а) селективность
b) механическая прочность
с) отсутствие глубоких пор
d) химическая инертность по отношению к разделяемой смеси
16. Детекторы, используемые в ВЭЖХ:
а) рефрактометрический
b) ИК-спектрофотометрический
с) поляриметрический
d) УФ-спектрофотометрический
е) транспортного типа
II. Лабораторная работа «Определение кислоты никотиновой методом хроматографии в тонком слое»
Материалы и оборудование:
- раствор кислоты никотиновой (0,125 г никотиновой кислоты растворяют в 2,5 мл спирта);
- стандартный образец никотиновой кислоты;
- система растворителей (подвижная фаза): гексан : этанол 95% : концентрированный аммиак в объемном соотношении 1:1:0,02;
- хроматографические камеры фирмы DESAGA H 50x50 (Приложение 14.1).
- стеклянные пластинки 50х50 мм для высокоэффективной ТСХ (например, «Silufol»).
Методика определения
1. Наполните хроматографическую камеру 1,5 мл заранее приготовленной смесью растворителей (подвижная фаза);
2. Отметьте на хроматографической пластинке с обратной стороны линию старта на расстоянии приблизительно 6 мм от края пластинки; с помощью капилляра нанесите 0,5 мкл раствора никотиновой кислоты и 0,5 мкл стандартного образца, используя шаблон.
3. Высушенную хроматографическую пластинку помещают в камеру сорбентом вниз; камеру закрывают покровным стеклом и оставляют на несколько минут для прохождения фронта растворителя на 3-4 см;
4. Извлеките пластинку из камеры, отметьте линию фронта растворителя, высушите на воздухе и рассматрите под УФ-лампой при длине волны 254 нм.
5. Обведите зоны адсорбции;
6. Определите величины Rf и Rs;
7. Сделайте вывод о соответствии определяемого токсиканта стандартному образцу по величинам Rf и Rs.
III. Лабораторная работа «Определение содержания гемцитабина в лиофилизированном порошке методом высокоэффективной жидкостной хроматографии (ВЭЖХ)».
Гемцитабин (2',2'-дифтородезоксицитидин)– цитотоксический агент с широким спектром противоопухолевой активности, применяемый при раке поджелудочной железы, легких, яичников, молочной железы, мочевого пузыря. От качества препарата (например, соответствия его содержания количеству, заявленному в нормативной документации) зависит его эффективность и безопасность. Количественное содержание гемцитабина в лекарственных препаратах определяют методом калибровки по стандартному образцу. В качестве стандарта для проверки пригодности хроматографической системы используют дезоксицитидин - вещество, близкое по физико-химическим свойствам к исследуемому веществу (Приложение 14.2).
Материалы и оборудование:
- хроматограф с детектором для ультрафиолетового и видимого диапазонов, с термостатированием колонок, насосом краном-инжектором, например - Metrohm 844 UV/VIS Compact IC (Швейцария);
- хроматографическая колонка - PRONTOSIL С18 ace-EPS 5µ 150х4.6 (США);
- дезоксицитидин - стандарт для проверки пригодности хроматографической системы (Sigma-Aldrich, США);
- гемцитабин - лиофилизированный порошок для приготовления раствора для инъекций
- подвижная фаза: ацетатный буфер (рН 5,0):ацетонитрил в объемном соотношении 97,5:2,5; изократические условия элюирования
- скорость потока элюента - 1мл/мин
- объём вводимой пробы - 20 мкл
- рабочая длина волны 268 нм
Методика определения
0. Приготовьте подвижную фазу по следующей методике:
- приготовление ацетатного буфера: 5,44 г аммония ацетата о. с.ч. растворяют в 400мл бидистилированной воды и добавляют 2,4 мл ледяной уксусной кислоты до рН 5,0
- полученный буфер фильтруют через мембранный фильтр с диаметром пор 0,45мкм, смешивают 390мл профильтрованного буфера с 10 мл ацетонитрила марки «для хроматографии»
1. Приготовьте раствор эталонного стандарта, точно взвесив 10 мг стандартного образца гемцитабина, который затем необходимо перенести в мерную колбу емкостью 50 мл и довести до объема водой для инъекций (р-р А). Приготовте растворы эталонных стандартов для калибровки, содержащие 0,05, 0,1 и 0,15 мг/мл(точно взвесьте 2,5, 5,0 и 7,5 мг эталонного стандарта и перенесите навески в три мерные колбы емкостью 50 мл и доведите до метки водой для инъекций.
Приготовьте раствор для проверки пригодности системы: точную навеску (10мг) дезоксицитидина перенесите в мерную колбу на 50 мл, растворите в воде для инъекций, доведя объем раствора до метки и перемешайте. 40,0 мл этого раствора помещают в мерную колбу на 50 мл, содержащую 10,0 мл стандартного раствора гемцитабина(р-р А), доводят объем водой для инъекций до метки и перемешивают.
2. Приготовление образца для анализа.
Взвешивают флакон с пробкой, затем переносят содержимое флакона в колбу на 200мл и доводят объем до метки водой для инъекций; флакон и пробку ополаскивают метанолом, дают высохнуть и снова взвешивают, рассчитывают вес взятого образца. Затем аликвоту(10мл) полученного раствора переносят в колбу на 100 мл и доводят водой до метки.
3. При проверке хроматографической системы была получена следующая хроматограмма (рис. 14.3).
Определите тип хроматографического разделения (абсорбционная, распределительная, эксклюзивная или аффинная хроматография) и его модификацию (обращено-фазовый или нормально-фазовый вариант).
Рассчитайте и оцените параметры пригодности хроматографической системы (эффективность по показателям ЧТТ, ВЭТТ, ПВЭТТ), а также параметры разделения двух компонентов анализируемой смеси (селективность, k’, Rs).
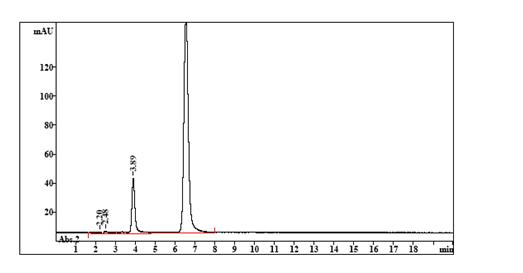 |
Рис. 14.3. Хроматограмма гемцитабина (время удерживания 6,55 мин) и дезоксицитидина (время удерживания 3,89 мин).
4. При хроматографическом определении растворов эталонных стандартов для калибровки были получены следующие данные:
Концентрация эталонного стандарта, мг/мл | АUC, mAU*c |
0,05 0,1 0,15 | 590,77 1181,41 1773б15 |
Вычислите площадь пика гемцитабина анализируемого образца на полученной хроматограмме, приближенно считая пик равнобедренным треугольником: S(мм2)=а1/2•h, где а1/2 – полуширина пика (мм); h – высота пика (мм) (рис. 13.4).
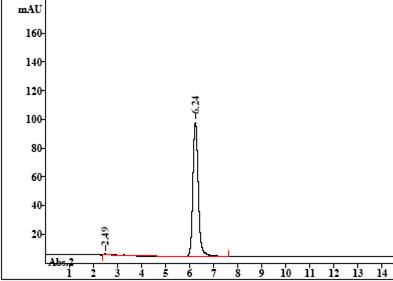 |
По полученным результатам сделайте вывод о содержании действующего вещества в испытуемом образце и его соответствии нормативной документации. Содержание гемцитабина гидрохлорида 95-105% от величины, заявленной на этикетке (190-210 мг).
Литература
1. Материалы лекций.
2. Токсикологическая химия Под ред. . 2--е изд., испр. – М.: ГЭОТАР-Медиа, 2006. – С.186-217.
3. Основы аналитической токсикологии / Дж. и соавт.– Женева: Всемирная организация здравоохранения, 1997. – С.72-76.
4. Растворители для ВЭЖХ / - М.:Бином, 2006. – 704 с.
5. Практическая высокоэффективная жидкостная хроматография /, , - М.: Химия, 1986. -278 с.
6. Высокоэффективная жидкостная хроматография в биохимии: Пер. с англ./Под ред. А. Хеншен. – М.: Мир, 1988. – 688с.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |




