d) обусловленные переходами электронов с первого возбужденного уровня на второй.
2. Преимущества дифракционной решетки как диспергирующего элемента перед
призмой:
a) механическая прочность;
b) высокая разрешающая способность;
c) термостойкость.
3. Наивысшую температуру имеет пламя:
a) закись азота - ацетилен;
b) воздушно-ацетиленовая смесь;
c) газовая горелка, использующая природный газ;
4. Качественный спектральный анализ основан на определении параметра спектрограммы:
a) количество атомов, находящихся в возбужденном состоянии;
b) расстояние между спектральными линиями примеси и основы исследуемого образца;
c) длина волны спектральных линий;
d) контрастность изображений спектральных линий.
5. Основная роль источника излучения:
) расплавление пробы;
a) возбуждение атомов и ионов;
b) диссоциация молекул;
c) освещение щели спектрографа.
6. К ультрафиолетовой части спектра относится область длин волн (нм):
a) 400 - 800;
b) 180 - 400;
c) 0,1 - 10;
d) 800 - 1000.
7. Функция диспергирующего элемента в спектрографе:
) служит для фокусировки излучения;
a) служит конденсором;
b) регистрирует спектр;
c) разлагает излучение по длинам волн.
8. Интенсивность (I) спектральной линии связана с концентрацией (С) (а, в, К – коэффициенты):
) I = K/C;
a) I = aCв;
b) I = KC;
c) I= a lgC.
9. Длина волны света связана с энергией кванта:
) прямо пропорционально;
a) не зависит от энергии;
b) обратно пропорционально;
c) зависит только в видимой области спектра.
10. Квантометры (полихроматоры) – это спектральные приборы, позволяющие:
) быстро сканировать по всему спектру;
a) определять одновременно несколько элементов;
b) получить излучение света отдельными квантами;
c) менять ширину входной щели.
12. Монохроматоры – это спектральные приборы, позволяющие
) использовать только призму для разложения излучения в спектр;
a) выделять только узкий участок спектра;
b) использовать несколько выходных щелей;
c) использовать источники возбуждения, дающие монохроматическое излучение.
II. Семинар «Основные принципы атомной спектрометрии. Способы минерализации биологических материалов при элементном анализе».
Вопросы для обсуждения на семинаре:
Основной принцип атомной спектрометрии. Схемы переходов электрона на атомных орбиталях. Что такое индуктивно-связанная плазма? Какие источники возбуждения атома используют в АЭС? Разрешающая способность измерительного прибора на примере АЭС-ИСП. Монохроматор и полихроматор: основное предназначение, сходство и отличие. Способы регистрации спектров в атомной спектрометрии. Валидационные характеристики методов ААС и АЭС-ИСП. Принципиальная схема атомно-абсорбционного спектрометра. Разновидности атомизаторов в ААС. Требования, предъявляемые к пламенным атомизаторам. Достоинства и недостатки электротермических атомизаторов? Способы пробоподготовки биообъекта для проведения атомной спектрометрии. Виды минерализации.III. Лабораторная работа «Определение цинка в волосах человека методом ААС».
1. Пробоподготовка образцов волос для ААС.
Методы пробоподготовки биопроб к анализу для определения их элементного состава заключаются в разрушении биологического материал. Это достигается путем «сухой» или «мокрой» минерализации. «Сухая» минерализация - это высокотемпературное «озоление» биоматериала, в результате которой образуется сухой остаток твердых оксидов металлов и амфотерных элементов («зола»). «Мокрая» минерализация – это окисление биоматрицы с использованием растворов веществ-окислителей (HNO3, H2SO4, HClO4, H2O2, KMnO4). В обоих случаях биологическая матрица (Б) окисляется до газообразных оксидов углерода и серы, воды, азота и др. Одновременно происходит образование твердых оксидов, содержащих определяемый металл или амфотерный элемент (ЭхОy):
![]()
Процесс минерализации анализируемой биопробы сопровождается ее концентрированием, т. к. из большой навески биоматериала образуется остаток (раствор или твердый остаток), преимущественно содержащий определяемый элемент (элементы). После растворения или разведения полученного в результате минерализации остатка аликвота полученного раствора вводится в тот или иной анализатор, например, в атомно-абсорбционный спектрометр.
При анализе кожи, ногтей, волос целесообразно использовать «сухое» озоление, что позволяет получить минимальный объем пробы с высоким содержанием металлов или амфотерных элементов. Термическое разложение (сухую минерализацию) волос проводят в кварцевых тиглях. Кварц достаточно инертен, не выделяет в пробу загрязнений и не сорбирует определяемые элементы.
Точную навеску волос (волосы не требуют предварительного высушивания до постоянной массы) помещают в кварцевые тигли и озоляют в муфельной печи при 400±2ºC в течение 15-30 мин (в зависимости от массы пробы). После охлаждения тигля определяют массу образовавшейся золы. Содержимое охлажденных тиглей смачивают концентрированной азотной кислотой (НNO3) с добавлением нескольких капель 30% пероксида водорода (H2O2), подсушивают на электроплитке с асбестовым покрытием и снова прокаливают в муфельной печи в течение 30-40 минут при 400ºC. Если в пробе остаются темные вкрапления (частички углерода или карбидов металлов) процесс повторют до образования серого, почти белого остатка. Для перевода пробы в раствор содержимое тигля растворяют в 2 мл концентрированной НNO3, упаривают на водяной бане до «мокрых солей», затем остаток растворяют при нагревании в 5 мл 1 моль/л НNO3. Количественно переносят содержимое тигля в мерную колбу или пробирку (объемом 10 или 25 мл), промывая тигель дистиллированной водой, объем доводят до метки водой. Если процесс деструкции биоматериала прошел до конца, то раствор в мерной колбе представляет собой прозрачную и бесцветную жидкость. Параллельно с исследуемой пробой готовят контрольную пробу на реактивы (все вещества и операции как для анализируемой пробы, за исключением осадка в тигле).
Содержание металла в пробе определяют с помощью калибровочной кривой, для построения которой используют стандартные образцы (СО) - водные растворы цинка хлорида. Стандартные растворы готовят с добавлением азотной кислоты, которая использовалась для получения конечного раствора анализируемой пробы – 1 моль/л HNO3. Серия калибровочных растворов состоит из 6 растворов с концентрацией цинка: 0,4, 0,8, 1,2, 1,6, 2,0 мкг/кг. Сначала готовят раствор с большей концентрацией (2 мкг/мл), а затем получают рабочие калибровочные растворы путем последовательного разбавления исходного. Калибровочную прямую проводят. осуществляя автоматическую линеаризацию, например в программе Origine (рис. 13. 4).
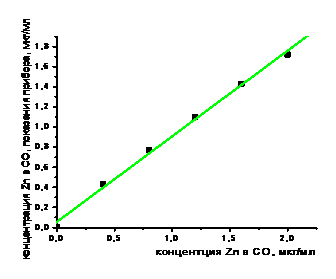
Рис. 13.4. Калибровочный график для определения цинка в волосах, полученный с использованием стандартного образца (СО) соли цинка
Анализ исследуемых растворов проводят при следующих настройках атомно-абсорбционного спектрометра (например, AAS30):
Лампа с полым катодом – цинковая
Длина волны (Zn) – 213,9 нм
Щель монохроматора – 0,2 мм;
Ток для лампы – 5А;
Пламя – ацетилен/воздух (расход: 90/650 л/ч);
Режим – однолучевой;
Режим индикации – концентрация.
Результаты измерений внесите в таблицу:
№ образца волос | Масса волос до озолени, мг | Масса сухого остатка после озоления, мг | Объем раствора, мл | Концентрация цинка в пробе (показания прибора), мкг/мл | Концентр. Zn в образце волос, мкг/г | Относительная ошибка среднего результата При доверительной вероятности Р=0.95 |
Контрольная проба | - | - | 25 | |||
1 | 25 | |||||
… | 25 | |||||
5 | 25 |
Литература
0. Материалы лекций.
0. Токсикологическая химия: учебник для вузов / под ред. . – М.: ГЭОТАР-Медиа, 2006. – С. 217-238.
0. , Макаренко спектрального анализа в судебной медицине.-М.: МНПП ЭСИ.- 1994.-360 с.
0. Дробышев атомного спектрального анализа.-С-Пб.: СПб Университет.- 2000. 314 с.
0. Аналитическая атомно-абсорбционная спектрокопия.- М.: Мир.- 1976. 358 с.
0. Брицке -абсорбционный спектрохимический анализ. - М.: Химия. - 1982. 224 с.
3. Применение хроматографических методов в
химико-токсикологическом анализе
Структура занятия
I. Входной тест по теме занятия.
II. Лабораторная работа «Определение никотиновой кислоты методом хроматографии в тонком слое сорбента».
III. Лабораторная работа «Определение содержания гемцитабина в лиофилизированном порошке методом высокоэффективной жидкостной хроматографии (ВЭЖХ)».
Целевые задачи:
- ознакомиться с классификацией хроматографических методов анализа;
- изучить методику проведения хроматографирования в тонком слое;
- освоить принципы, лежащие в основе определения ксенобиотиков методом высоко-эффективной жидкостной хроматографии (ВЭЖХ).
Краткое теоретическое введение
Хроматографией называется разделение веществ, основанное на распределении компонентов смеси между неподвижной (стационарной) и подвижной (мобильной) фазами.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |




