В целом же промышленность строительных материалов не имеет принципиальных технических и технологических препятствий для организации своей деятельности по безотходной технологии.
Контрольные вопросы
1. Основные экологические проблемы производства строительных материалов.
2. Какое отличие в технологии получения красного и силикатного кирпича и какое это имеет значение при утилизации отходов?
3. Какие основные составляющие гидравлических вяжущих?
4. Какие показатели определяют свойства цемента?
5. В чём отличие керамзита от аглопорита?
6. Что такое «шлакоситал» и как его производят?
7. Что такое «клинкер»?
8. Что такое «пушонка» и «кипелка»?
9. Расшифруйте C3A и C3S.
10. Что означает (расшифруйте) C4AF?
11. Какие причины мешают широкому внедрению замкнутых водооборотных систем в производстве строительных материалов?
12. Какие причины мешают широкому использованию отходов горнодобывающих отраслей для производства строительных материалов?
10. Экологические проблемы химической промышленности.
Производство неорганических веществ
«В химии нет отходов, а есть неиспользованное сырье»
Химическая промышленность – одна из ведущих отраслей тяжелой индустрии. Она является научно-технической и материальной базой химизации народного хозяйства и играет исключительно важную роль в развитии производительных сил, укреплении оборонной мощи государства, в обеспечении жизненноважных потребностей общества.
Ассортимент химической продукции насчитывает десятки тысяч наименований. Наиболее крупнотоннажные отрасли – это производство кислот, солей, аммиака, соды, минеральных удобрений и некоторых других продуктов. Без удобрений и химических средств защиты растений человечество не может прокормиться, обеспечить себя продуктами питания [33].
10.1. Комплексная переработка фосфатного сырья
Сырьем для получения фосфорных удобрений и других соединений фосфора служат апатитовые и фосфоритовые руды. Основным полезным соединением фосфатных руд является Са3(РО4)2, входящий в состав минералов апатитовой группы с общей формулой 3Са3(РО4)2 ![]() СаХ2, где Х – может быть F-, Сl- или группа ОН-.
СаХ2, где Х – может быть F-, Сl- или группа ОН-.
Общее мировое потребление фосфатного сырья в настоящее время составляет более 150 млн. т в год, из них около 90% расходуется на производство удобрений, кормовых добавок и пестицидов. Фосфор, как известно, является одним из основных элементов жизни и связан с энергообменом в клетке. Разведанные мировые запасы фосфатного сырья составляют около 26 млрд. т, в том числе в России около 8 млрд. т. Прогноз показывает, что разведанных запасов фосфора будет достаточно не более чем на 150 лет. Поэтому ученые уже сейчас думают о более рациональном использовании имеющихся фосфатных руд и возможности их добычи из мирового океана в будущем.
Апатитовый концентрат является основным сырьем для получения большинства фосфорных удобрений в нашей стране. Его получают из апатитонефелиновых руд Хибинского месторождения. Методом флотации разделяют апатитовую и нефелиновую фракции.
Химический состав хибинского фторапатита, (%): СаО – 55,5; Р2О5 – 42,3; F – 3,8.
В структуре минерала кальций изоморфно замещается стронцием, марганцем, кадмием, церием, иттрием и другими элементами. Апатит перерабатывают, разлагая его минеральными кислотами. Наиболее широко распространен сернокислотный способ вскрытия апатита, позволяющий использовать более 90% фосфора и до 50% фтора. В ряде случаев применяют для разложения смесь серной и азотной кислот или одну азотную кислоту. Редкоземельные элементы и стронций (замещающие кальций) извлекаются при азотнокислотном вскрытии фосфатного сырья. Разложение апатита серной, азотной кислотами или их смесью дает возможность получать, как простые, так и сложные фосфорные удобрения: суперфосфат, двойной суперфосфат, аммофос, нитрофоску и др.
Одной из основных стадий производства сложных удобрений является получение фосфорной кислоты.
Экстракционную фосфорную кислоту (ЭФК) получают разложением апатита или фосфорита серной кислотой с образованием фосфорной кислоты и фосфогипса по реакции:
Са5 (РО4)3 F + 5Н2SО4 + nH2О![]() 3Н3 РО4 + 5СаSО4
3Н3 РО4 + 5СаSО4 ![]() nН2О + НF.
nН2О + НF.
Выделяющийся, в результате реакции HF далее взаимодействует с соединениями кремния и водой с образованием SiF4 в газовой и Н2 SiF6 в жидкой фазах.
В зависимости от условий проведения процесса различают дигидратный метод получения ЭФК (n=2), полугидратный (n=0.5) и ангидридный (n=0). В промышленности нашли распространение первые два метода, из них дигидратный встречается чаще. Принципиальная технологическая схема производства ЭФК в дигидратном режиме представлена на рис.10.1.
Нейтрализацией ЭФК аммиаком с последующей упаркой, сушкой и грануляцией получают наиболее распространенное сложное удобрение – аммофос, смешением его с KCl – аммофоску.
Помимо получения фосфорных удобрений, при переработке фосфатного сырья утилизируют соединения фтора (вызвано в первую очередь санитарными требованиями ввиду высокой токсичности всех соединений фтора, особенно газообразных) и фосфогипс. Полностью извлекать фтор из апатита не удается и полезно используется только 30-50% от его общего содержания:
- путём улавливания фтора из газовой фазы на стадии получения ЭФК и её упаривания,
- и осаждением в виде фторсиликата натрия.
С производством экстракционной фосфорной кислоты связано образование одного из самых крупнотоннажных отходов химической промышленности – фосфогипса, представляющего собой дигидрат сульфата кальция, содержащий ряд примесей, в том числе фосфаты и фториды.
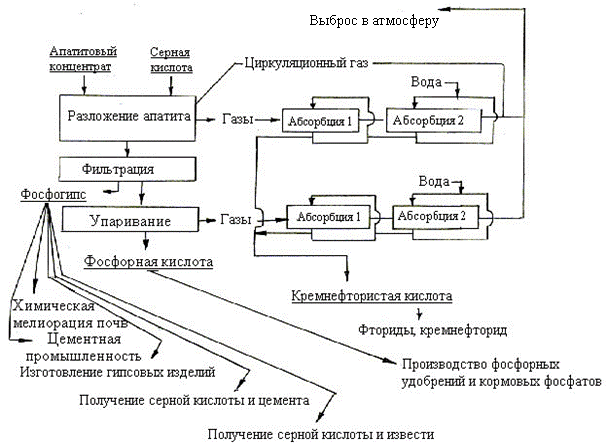 |
Рис. 10.1. Принципиальная технологическая схема производства экстракционной фосфорной кислоты в дигидратном режиме
Промышленной практикой доказаны техническая возможность и экономическая целесообразность использования фосфогипса в следующих направлениях:
- в сельском хозяйстве для химической мелиорации солонцовых почв вместо природного гипса;
- в цементной промышленности в качестве минерализатора при обжиге и как добавка к цементному клинкеру при помоле;
- для производства гипсовых вяжущих и изделий из них;
- для получения цемента;
- для получения серной кислоты и извести и т. д.
В промышленном масштабе также осуществлена переработка фосфогипса на сульфат аммония и мел.
Наиболее полно используют все компоненты фосфатного сырья при азотнокислотной переработке, рис. 10.2.
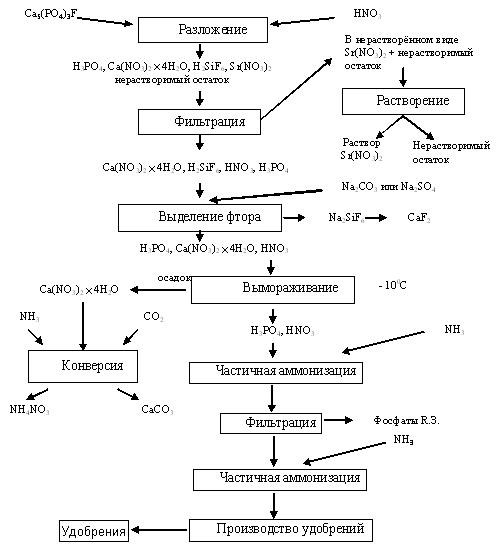
Рис. 10.2. Технологическая схема азотнокислотной переработки апатита
10.2. Комплексная переработка калийного сырья
Природным источником калия служат руды, главными минералами которых являются сильвинит, карналлит, нефелин и некоторые другие.
Мировые запасы калийного сырья оцениваются в 131,4 млрд. т (в пересчете на К2О). Наша страна обладает крупнейшими в мире запасами калийных солей, около 50 млрд. т. Из них самое значительное Верхнекамское месторождение. Большие запасы калийных солей сосредоточены также в Белоруссии (около Минска), Прикарпатье и некоторых других районах. Все они, как правило, являются комплексным сырьем. Так, средний состав сильвинитовых руд в России, мас %.: 24-33 KCl, 6I-7I NаСl, 0,2-0,3 MgCl2, 1,3-1,7 СаSО4. Содержание нерастворимого остатка (н. о. – глина, сульфат, карбонат кальция и т. д.) в калийных рудах может составлять от десятых долей до десяти и более процентов. Сильвинитовая руда Верхнекамского месторождения содержит до 2,5 % н. о., а Старобинского (Белоруссия) – до 10-12 % н. о.
Таким образом, состав калийных руд при организации комплексной переработки сырья предопределяет необходимость рационального и наиболее полного использования, по крайней мере, четырех основных компонентов: калия, натрия, магния, хлора.
Основным целевым продуктом калийной промышленности является хлорид калия, который может служить, как в качестве самостоятельного удобрения, так и сырьем для получения калиевых солей: сульфата, карбоната, нитрата и др. Кроме того, соли калия входят в состав некоторых сложных удобрений, как, например, нитроаммофоски, аммофоски (NPK удобрения), содержащих три питательных элемента: фосфор, азот и калий.
В нашей стране добыча сильвинитовых руд осуществляется шахтным методом, а их переработка в хлорид калия – галургическим и флотационным методами. Принципиальная схема галургического метода представлена на рис.10.3. Метод основан на различной растворимости хлоридов калия и натрия в воде в зависимости от температуры. Выход KCl по этой технологии составляет 85,9%.
Флотационный метод основан на различной смачиваемости кристаллов хлорида калия и натрия в присутствии флотореагентов, увеличивающих селективность их разделения. Выбор технологической схемы зависит от состава руды и от наличия в ней нерастворимого остатка. Выход KCl при флотационном методе составляет 84,5%.
Выделение сильвинита связано с образованием значительных по объему галитовых (NaCl) отходов и жидких глинисто-солевых шламов, складируемых в солеотвалах и шламонакопителях. При получении 1 т KCI в отвал поступает 2,5-3,0 т галитовых отходов (влажностью до 10-12%) и 0,3 т нерастворимого остатка, в виде шламосолевой пульпы с отношением ж : т, равном 1,7 : 2,5.
К настоящему времени в солеотвалах накоплено более 130 млн. т галитовых отходов, а в шламонакопителях – до 20 млн. т глинисто-солевых шламов. Общая площадь земель, занятых ими, превышает 500 га.

Рис.10.3. Принципиальная схема получения хлорида калия галургическим методом

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 |



