Уменьшение количества складируемых галитовых отходов может быть осуществлено в результате реализации следующих мероприятий:
- широкого использования галита в различных отраслях народного хозяйства в качестве вторичных минеральных сырьевых ресурсов;
- в химической промышленности (производство едкого натра и хлора);
- в энергетике;
- в дорожном и коммунальном хозяйстве, в производстве кормовой и пищевой поваренной соли и других;
- утилизации всех шламовых отходов, например, в промышленности строительных материалов, для производства глинисто-солевых порошков, применяемых при бурении, в качестве удобряющих добавок к торфяным и песчаным почвам и др.
Наиболее перспективными и экономически целесообразными направлениями использования галитовых отходов являются производства технического хлорида натрия с последующим получением едкого натра и хлора в химической промышленности и поваренной соли в пищевой. В первую очередь можно перерабатывать на поваренную соль (пищевую или техническую) галлургические галитовые отходы, так как получаемые по флотационной схеме обогащения галитовые отходы являются менее пригодными к утилизации из-за дорогостоящего процесса очистки их от аминов, применяемых при флотации. В связи с этим, предусматриваются их возврат и закладка в выработанное шахтное пространство.
10.3. Пути совершенствования производств важнейших химических продуктов
Производство серной кислоты. Ни одна отрасль промышленности практически не может обойтись без серной кислоты. Особенно широко она применяется в химической промышленности.
Серную кислоту получают различной концентрации и качества. В нашей стране установлен стандарт на серную кислоту и олеум (раствор серного ангидрида в серной кислоте). Выпускаемые промышленностью контактная серная кислота и олеум содержат соответственно 92,5-94% H2SO4 и 18,5-20% SO3 (в серной кислоте).
Для производства серной кислоты используется довольно широкий ассортимент сырья. Так, наряду с серным колчеданом применяют серу, отходящие серосодержащие газы цветной металлургии, сероводород, отработанную серную кислоту и др.
Серный колчедан может содержать примеси соединений меди, цинка, свинца, мышьяка, никеля, кобальта, селена, висмута, теллура, кадмия, фтора, а также золото и серебро. Содержание селена составляет до 220 г/т, золота до 4 г/т, серебра до 40 г/т, мышьяка до 0.4%, фтора до 0.2%.
Наиболее ценным сырьем дня получения серной кислоты является элементарная сера. При ее сжигании образуется концентрированный газ, содержащий незначительные количества примесей мышьяка. При обжиге серы не остается огарка, поэтому схема переработки этого вида сырья на серную кислоту упрощается и является более экономичной. В настоящее время до 50% всей элементарной серы, получаемой в мире, расходуется на производство серной кислоты.
Серную кислоту получают из сернистого ангидрида (SO2) путем окисления его кислородом и последующего присоединения воды по реакции:
SO2 + 1/2O2 + Н2О ![]() Н2SO4
Н2SO4
В обычных условиях окисление сернистого ангидрида протекает очень медленно, поэтому в промышленности для ускорения процесса эту реакцию проводят на катализаторах или в качестве передатчика кислорода применяют оксид азота. В зависимости от этого различают контактный и нитрозный (башенный) способы производства серной кислоты. Удельный вес серной кислоты, получаемой нитрозным способом, в общем объеме её производства составляет менее 5% и продолжает уменьшаться.
Сущность контактного способа состоит в том, что сернистый ангидрид окисляется до серного в присутствии катализатора при высокой температуре (440-550оС). Процесс окисления сернистого ангидрида на катализаторе протекает с выделением тепла:
2SO2 + О2 ![]() 2SO3 + Q
2SO3 + Q
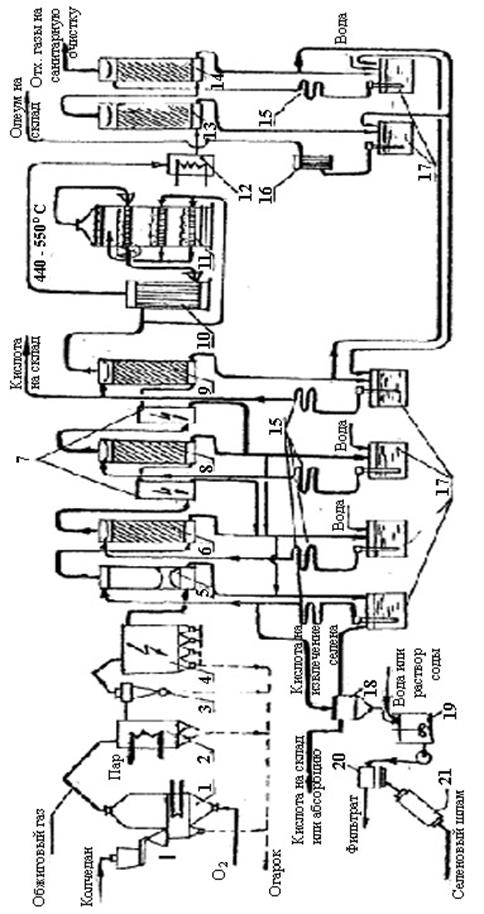
Наиболее полно производство контактной серной кислоты отражает технологическая схема, в которой исходным сырьем служит колчедан (классическая схема) (рис.10.4). Эта схема включает четыре основные стадии:
- получение сернистого ангидрида;
- очистку газа, содержащего сернистый ангидрид, от примесей;
- окисление сернистого ангидрида до серного на катализаторе;
- абсорбцию серного ангидрида водой.
Основными направлениями создания экологически обоснованного (малоотходного и безотходного) производства серной кислоты являются:
- максимально возможное улавливание SO2 и, следовательно, минимально возможное загрязнение им атмосферы;
- использование всех компонентов сырья (селена, меди, драгоценных металлов, железа и т. д.).
В колчеданах, применяемых для производства серной кислоты, содержится 0,002-0,02% селена, соединения которого находят все более широкое применение в различных областях народного хозяйства: в производстве выпрямителей переменного тока, фотоэлементов, стекольной промышленности, телевидении. Отходы переработки колчедана – основной источник получения селена в нашей стране.
Степень извлечения селена из колчедана в производстве серной кислоты контактным способом колеблется в широких пределах (от 30 до 60%) и зависит от устройства и режима работы печей, режима работы очистного оборудования и прочего.
Для достижения высокой степени окисления и уменьшения содержания сернистого ангидрида в отходящих газах без значительного увеличения количества контактной массы применяют так называемое двойное контактирование или контактирование с промежуточной абсорбцией. Сущность двойного контактирования состоит в том, что процесс окисления SO2 на катализаторе проходит в два этапа, причём на первом степень превращения составляет около 90%. Затем из газа выделяют серный ангидрид, направляя газ в дополнительный, промежуточный абсорбер. В результате в газе увеличивается соотношение О2:SO2, что позволяет на втором этапе увеличить степень превращения оставшегося сернистого ангидрида до 95-97%. Общая степень превращения достигает 99,5-99,7%, а содержание SO2 в отходящих газах составляет около 0,03%, в то время как при одинарном контактировании – десятые доли процента: в среднем 0,2% SO2 (5 г/м3) и около 0,007% SO3 (0,3 г/м3).
В настоящее время ведутся работы по усовершенствованию схемы производства контактной серной кислоты путем нового оформления отдельных стадий этого процесса и применения более мощных аппаратов, обеспечивающих высокую производительность систем, частичной или полной замены воздуха кислородом и повышения давления реакционных газов.
При обжиге серного колчедана отходы пиритных огарков составляют 70% от массы колчедана. На 1 т производимой кислоты выход огарка составляет около 0,55 т. Пиритные огарки состоят, главным образом, из железа (40-63%) с небольшими примесями серы (1-2%), меди (0,33-0,47%), цинка (0,42-1,35%), свинца (0,32-0,58%), драгоценных (10-20 г/т) и других металлов.
Утилизация пиритных огарков возможна по нескольким направлениям:
- для извлечения цветных металлов и производства чугуна и стали;
- в цементной промышленности;
- в сельском хозяйстве и т. д.
Однако в настоящее время пиритные огарки используют главным образом в цементной промышленности в качестве минерализующей добавки к портландцементной шихте.

Небольшие количества огарка и пыли сухих электрофильтров используют для получения минеральных пигментов: железного сурика, охры. Пиритные огарки используются также в сельском хозяйстве в качестве удобрений, содержащих медь, и для получения некоторых инсектицидов.
Производство аммиака. Соединения азота имеют исключительно большое значение для всего народного хозяйства. В связи с этим азотная промышленность по темпам развития опережает другие отрасли химической промышленности. Основным промежуточным продуктом для получения огромного числа различных азотсодержащих соединений является аммиак, а синтез его из водорода и азота – единственным крупномасштабным методом производства этого важнейшего продукта.
Производство аммиака состоит из трех основных технологических стадий:
- получение исходной азотоводородной смеси (синтез-газа);
- очистка синтез-газа от примесей;
- каталитический синтез аммиака.
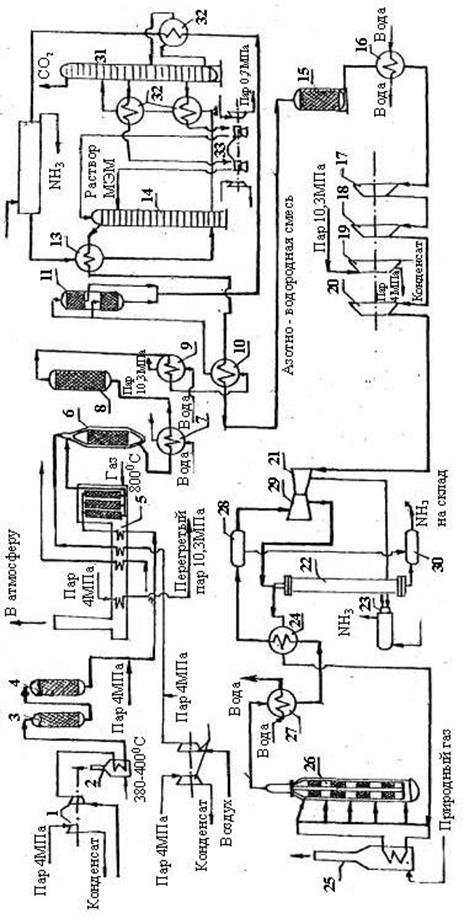
Основные процессы объединены в единый энерготехнологический комплекс. Принцип энерготехнологической схемы состоит в тесной взаимосвязи между химическими и энергетическими процессами, между аппаратурой технологических и энергетических стадий, что позволяет достичь, возможно более полной утилизации низкопотенциального и высокопотенциального тепла, вести технологические процессы с высокой скоростью. Ниже приведена технологическая схема производства аммиака с этаноламиновой очисткой газа от СО2 (рис.10.5).
Дальнейшее развитие технологии синтеза аммиака направлено, в первую очередь, на снижение расхода сырья и энергии, уменьшение капиталовложений при строительстве новых производств, повышение надежности работы оборудования и приборов, оптимизацию технологического процесса с широким использованием вычислительной техники и управляющих систем и исключение вредного воздействия на окружающую среду. В связи с развитием атомной энергетики возможно использование тепла атомных реакторов для получения водорода и для производства аммиака в целом.
В производстве аммиака основным сырьем является природный газ. Для получения водорода планируется используется реакция:
С + Н2О ![]() СО + Н2
СО + Н2
Одним из путей совершенствования схемы синтеза аммиака является выделение метана и аргона из циркуляционного газа.
В последнее время ведутся исследования совмещенных технологических схем производства аммиака и метанола, аммиака и опресненной воды, аммиака и карбамида.


|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 |



