На сегодня доля энергозатрат в стоимости аммиака, включая амортизационные отчисления, составляет около 70%. Поэтому разработка схем, обеспечивающих более высокий, чем существующий КПД использования энергии, имеет большое значение. В конечном итоге развитие производства аммиака идет в направлении более рационального использования сырья и энергии с минимально возможным влиянием производства на окружающую среду, т. е. в направлении создания безотходного или чистого производства.
Производство азотной кислоты. Азотная кислота – один из важнейших продуктов химической промышленности. По объему производства в мире (свыше 50 млн. т в год) азотная кислота находится на втором месте после серной кислоты. В нашей стране около 40% азотной кислоты расходуется на производство сложных минеральных удобрений и нитратных солей.
Промышленность выпускает азотную кислоту следующих видов: 46-57% (мас. %) НNО3, концентрированную (98,9% НNО3) и реактивную (54-68% HNО3).
В настоящее время наиболее широко применяется многотоннажное производство азотной кислоты из аммиака. Процесс окисления происходит с поглощением тепла на платиновом катализаторе по реакции:
4NH3 + 5O2 ![]() 4NO + 6H2O – Q
4NO + 6H2O – Q
Атмосферный воздух, применяемый для производства азотной кислоты, забирается на территории завода или вблизи него. С целью избежания отравления катализатора воздух очищают от газообразных примесей и пыли в скруббере, орошаемом водой, не содержащей хлора.
Технологическая схема производства азотной кислоты под показана на рис. 10.6.
Хвостовые нитрозные газы подвергаются высокотемпературной каталитической очистке на двухслойном катализаторе. Для каталитического разложения оксидов азота в первом слое применяется палладированный оксид алюминия. В качестве газа-восстановителя используется природный газ.
Повсеместное введение очистки отходящих газов путем восстановления оксидов азота на катализаторе позволило ликвидировать печально знаменитые «лисьи хвосты» и сделать производство азотной кислоты практически малоотходным. На очереди стоит задача создания экологически обоснованного безотходного производства азотной кислоты.
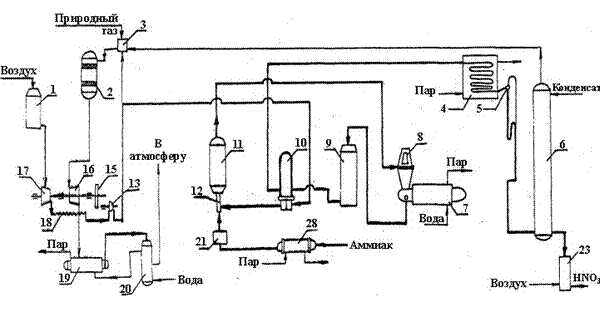 |
Рис 10.6. Технологическая схема производства азотной кислоты:
1 – фильтр для очистки воздуха; 2 – реактор для восстановления оксидов азота; 3 – камера подготовки газов (топка); 4 – конденсатор; 5 – сепаратор; 6 – абсорбционная колонна; 7 – котёл-утилизатор; 8 – контактный аппарат; 9 – окислитель нитрозных газов; 10 – подогреватель воздуха; 11 – фильтр тонкой очистки аммиачно-воздушной смеси; 12 – смеситель аммиака и воздуха; 13 – турбокомпрессор – вторая ступень; 15 – редуктор; 16 – газовая турбина; 17 – турбокомпрессор – первая ступень; 18 – холодильник; 19 – котёл-утилизатор; 20 – экономайзер; 21 – фильтр для аммиака; 22 – подогреватель для аммиака; 23 – продувочная колонна.
Каустическая сода. Основными потребителями каустической соды (NaOH) являются целлюлозно-бумажная промышленность, производства искусственных волокон, глинозема, различных химических соединений, мыла и др.
Каустическую соду в основном получают электрохимическим способом – электролизом раствора (рассола) NaCl. Одновременно получают анодный продукт – элементарный хлор. В современном производстве едкого натра и хлора применяются два основных способа электролиза: с жидким ртутным катодом и диафрагмой (мембраной).
При производстве NaOH в электролизерах с ртутным катодом получают концентрированный раствор каустической соды высокой степени чистоты, что является одним из основных преимуществ этого метода. Недостатком способа является загрязнение окружающей среды высокотоксичными соединениями ртути. В настоящее время в мировой практике соотношение методов получения NaOH с ртутным катодом и диафрагменным методом составляет 1:1. Однако доля диафрагменного метода непрерывно увеличивается.
Получение NaOH с использованием ртутного катода основано на образовании амальгамы натрия в электролизере под действием постоянного электрического тока на раствор поваренной соли:
2 NaCI + 2nНg ![]() Сl2 + 2NаНgn.
Сl2 + 2NаНgn.
Образовавшаяся амальгама в специальном аппарате разлагается водой с образованием NaOH и H2, а регенерированная ртуть возвращается в электролизер:
2 NаНgn + 2H2O ![]() 2 NaОН + H2 + 2nНg.
2 NaОН + H2 + 2nНg.
В результате электролиза раствора NaCl получают три товарных продукта: каустическую соду, хлор и водород.
Технологическими отходами производств NaOH с ртутным катодом являются: ртутьсодержащие отходы (шламы), образующиеся при очистке хлора и каустической соды, сточные воды, выхлопные (вентиляционные) газы, шламы СаСОз и Мg(ОН)2, образующиеся в результате очистки рассола от ионов Са2+ и Mg2+. Особую опасность для людей и окружающей среды представляют ртутьсодержащие отходы.
Диафрагменный метод получения каустической соды более перспективен, поскольку исключает применение ртути. Принципиальная технологическая схема получения каустической соды и хлора диафрагменным методом с повторным использованием сточных вод представлена на рис. 10.7.
Щелочь, получаемую при электролизе в виде растворов, подвергают концентрированию в выпарных аппаратах. При выпаривании электролитических щелоков происходит выделение твердой поваренной соли вследствие ее малой растворимости в концентрированных растворах едкого натра. В виде так называемого обратного рассола она возвращается на электролиз. По этой бессточной диафрагменной схеме в нашей стране работает производство каустической соды мощностью 150 тыс. т в год.
Другой компонент хлорида натрия – хлор выделяется при электролизе в элементарном виде. Он находит широкое применение в современной химической промышленности и некоторых других областях народного хозяйства. Производство хлора в мире превышает 11 млн. т в год.
 |
Рис. 10.7 Схема повторного использования сточных вод в производстве хлора и каустической соды диафрагменным методом:
I – оборотный барометрический цикл; I I – установка очистки сточных вод; 1 – приготовление рассола; 2 – очистка рассола; 3 – электролиз; 4 – выпарка электрощёлоков под давлением (41) и в вакууме (42); 5 – отделение соли от каустической соды; 6 – барометрическая конденсация; 7 – градирня; 8 – осветление сточных вод; 9 – обезвоживание суспензий; 10 – фильтрация сточных вод.
Кальцинированная сода. Сода находит широкое применение в народном хозяйстве. В настоящее время мировое производство соды составляет около 20 млн. т в год. Около 30% соды используется в самой химической промышленности, где она применяется в производстве фторидов, фосфорных удобрений, синтетических моющих средств, стеклопластиков и пенопластов и др.
Кальцинированную соду (Na2CO3) преимущественно получают аммиачным методом (способ Сольве) из NaCl. В качестве сырья для производства Na2CO3 используют также нефелин, чилийскую селитру (NaNO3) и NaOH.
Во всем мире аммиачным способом производят 85% соды, модифицированным аммиачным – 3%, из NaNO3 и NaOH – 0.1%; природной соды добывается 8-12%. Принципиальная технологическая схема получения кальцинированной соды аммиачным методом представлена на рис. 10.8.
Сущность процесса состоит в следующем: очищенный от примесей аммонизированный раствор поваренной соли подвергается карбонизации, образующийся бикарбонат натрия выпадает в осадок:
NaCl + NH3 + CO2 + H2O ![]() NaHCO3
NaHCO3 ![]() + NH4Cl.
+ NH4Cl.
Кристаллы NaHCO3 отфильтровываются от маточника и подвергаются кальцинации (прокалке) с целью получения готового продукта:
2NaHCO3 ![]() Na2CO3 + CO2 + H2O.
Na2CO3 + CO2 + H2O.
Для регенерации аммиака маточник, содержащий (г/л):
180-200 NH4Cl, 70-80 NaCl и небольшую часть непрореагировавшего NH4HCO3, обрабатывают известковым молоком:
2NH4Cl + Ca(OH) 2 ![]() 2NH3
2NH3![]() + 2H2O + CaCl2 .
+ 2H2O + CaCl2 .
Выделяющийся аммиак отгоняют с паром и возвращают в цикл.
При регенерации аммиака на каждую тонну соды образуется 10-12 м3 так называемой «дистиллерной жидкости». Она представляет собой суспензию нерастворимых продуктов (СаСО3 , CaSO4 , Са (ОН)2, песка и др.) в растворе хлоридов кальция и натрия.
Средний состав дистиллерной жидкости (г/л): 85-95 CaCl2, 45-50 NaCl, 6-15 CaCO3 , 3-5 CaSO4 , 3-10 Mg(OH)2 , 2-4 CaO, 1-3 Fe2O3 + Al2O3 , 1-4 SiO2. На одну тонну Na2CO3 в отвал выбрасывается 1 т СаСl2, 0,5 т NaCl и 200-300 кг твердых нерастворимых примесей. Для захоронения эту жидкость перекачивают в шламонакопители, так называемые «белые моря».
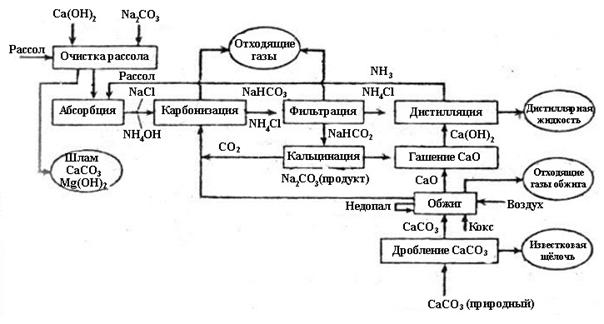 |
Рис 10.8. Принципиальная схема получения кальцинированной соды аммиачным методом
Кроме дистиллерной жидкости отходами производства кальцинированной соды являются шламы очистки рассола, состоящие из CaCO3 и Мg(ОН)2, отходящие газы карбонизации, содержащие NH3 , и отходящие газы обжиговоизвестковых печей.
Особую сложность вызывает содержание «белых морей» в связи с высокой растворимостью хлористых солей. Из дистиллерной жидкости можно извлекать СаСl2 и NaCl. При этом хлористый натрий можно использовать как техническую соль или вернуть в производство соды. Организация сбыта CaCl2 более сложная проблема, так как отсутствуют крупные потребители этого продукта. Кроме того, на выпаривание воды из дистиллерной жидкости необходимо затратить много энергии. Хлорид кальция может быть использован в химической промышленности в качестве осушителя жидкостей и газов, для посыпки улиц и дорог зимой (вместо NaCl), для мелиорации солончаковых почв, как добавка в шихту для получения цемента и в бетон.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 |



