1) заранее определить количество узлов ![]() квадратурной формулы, исходя из величины
квадратурной формулы, исходя из величины ![]() и оценки погрешности соответствующей квадратурной формулы. Для этого потребуется вычислить
и оценки погрешности соответствующей квадратурной формулы. Для этого потребуется вычислить ![]() или
или ![]() и ее
и ее ![]() . Затем вычислить приближенное значение
. Затем вычислить приближенное значение ![]() как собственный интеграл от
как собственный интеграл от ![]() до некоторого
до некоторого ![]() , используя найденное
, используя найденное ![]() . После этого увеличиваем
. После этого увеличиваем ![]() и вычисляем
и вычисляем ![]() от
от ![]() до нового
до нового ![]() с тем же
с тем же ![]() . Вычисления прекращаем, если
. Вычисления прекращаем, если ![]() , в противном случае снова увеличиваем
, в противном случае снова увеличиваем ![]() и т. д.
и т. д.
2) заранее определить достаточно большой верхний предел интегрирования ![]() . Это можно сделать, например, следующим образом: поставить требование
. Это можно сделать, например, следующим образом: поставить требование 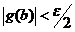 . Затем вычислить
. Затем вычислить ![]() как собственный интеграл на отрезке
как собственный интеграл на отрезке ![]() по аналогии с вычислением
по аналогии с вычислением ![]() , для контроля точности увеличивая
, для контроля точности увеличивая ![]() .
.
Все вышесказанное относится, в первую очередь, к Excel, где целесообразно будет воспользоваться процедурами VBA. Что касается пакета Mathematica, там не надо слишком заботиться об ![]() , b b и т. д., ибо функция Integrate уже включает в себя вычисление интеграла по квадратурной формуле с некоторой точностью. В [2] имеется программа системы Mathematica, не содержащая циклов. Ее необходимо уточнить (оформить цикл).
, b b и т. д., ибо функция Integrate уже включает в себя вычисление интеграла по квадратурной формуле с некоторой точностью. В [2] имеется программа системы Mathematica, не содержащая циклов. Ее необходимо уточнить (оформить цикл).
Глава IV
Решение обыкновенных дифференциальных уравнений и
систем обыкновенных дифференциальных уравнений.
§ 1. Некоторые сведения о дифференциальных уравнениях химических процессов (уравнениях кинетики, кинетических уравнениях).
Основной закон химической кинетики: скорость реакции в каждый момент времени пропорциональна произведению концентраций реагирующих веществ, возведенных в соответствующие степени.
Пусть стехиометрическое уравнение реакции записано в виде
![]() (1)
(1)
где ![]() –
– 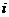 -тое исходное вещество,
-тое исходное вещество, ![]() –
– ![]() -тый продукт,
-тый продукт, ![]() – коэффициенты. В случае одностадийной реакции кинетическое уравнение имеет вид
– коэффициенты. В случае одностадийной реакции кинетическое уравнение имеет вид
![]() (2)
(2)
![]() – константа скорости,
– константа скорости, ![]() – порядок реакции,
– порядок реакции, ![]() – скорость реакции.
– скорость реакции.
Если рассматриваемая реакция обратимая, то ее кинетическое уравнение принимает вид
![]() (3)
(3)
Простейшие примеры.
1) Радиоактивный распад.
Скорость распада радиоактивного вещества пропорциональна его количеству – реакция первого порядка. Пусть ![]() – число атомов радиоактивного вещества,
– число атомов радиоактивного вещества, ![]() – время,
– время, ![]() – константа распада. Тогда
– константа распада. Тогда
![]() (4)
(4)
Задача: найти время, за которое концентрация уменьшится вдвое.
Решение. Задача Коши для уравнения (4) с начальным условием ![]() имеет решение
имеет решение ![]() . Отсюда искомое время
. Отсюда искомое время ![]() удовлетворяет соотношению
удовлетворяет соотношению ![]() , откуда следует, что
, откуда следует, что ![]() .
.
2) Коагуляция – процесс осаждения коллоида.
Ее можно рассматривать как реакцию второго порядка
![]() (5)
(5)
где ![]() – концентрация золя,
– концентрация золя, ![]() – константа, характеризующая вероятность столкновения частиц.
– константа, характеризующая вероятность столкновения частиц.
3) Определение порядка реакции в случае, когда в ней принимает участие одно вещество.
Кинетическое уравнение
![]() (5)
(5)
где ![]() – концентрация вещества
– концентрация вещества ![]() ,
, ![]() – время,
– время, ![]() – константа скорости реакции,
– константа скорости реакции, ![]() – неизвестный порядок реакции.
– неизвестный порядок реакции.
Задача: Пусть дано уравнение (6) и начальное условие 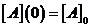 . Найти
. Найти ![]() .
.
Решение. Введем переменную ![]() :
: 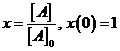 . Тогда (6) примет вид
. Тогда (6) примет вид
![]() или
или ![]() (7)
(7)
где 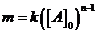 ,
, 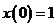 ,
, 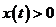 .
.
В результате интегрирования получим
![]() (8)
(8)
Выделим два момента времени ![]() и
и ![]() , найдем
, найдем ![]() и
и ![]() . Подставим в (8):
. Подставим в (8): 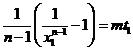 ;
; 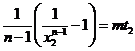 откуда следует, что
откуда следует, что 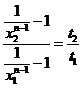 . Выберем
. Выберем ![]() и
и ![]() так, чтобы выполнялось
так, чтобы выполнялось ![]() . Тогда
. Тогда 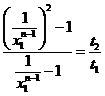 , откуда
, откуда 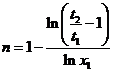 .
.
В дальнейшем будем рассматривать химические реакции, протекающие в замкнутой системе, для которых концентрации исходных веществ и продуктов реакции связаны соотношениями 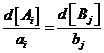 . Обозначим исходные концентрации через
. Обозначим исходные концентрации через ![]() и
и ![]() и проинтегрируем данное соотношение. Получим
и проинтегрируем данное соотношение. Получим 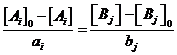 . Последнее соотношение можно обозначить через переменную
. Последнее соотношение можно обозначить через переменную ![]() :
:
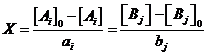 (9)
(9)
§ 2. Математические модели некоторых химических процессов.
Необратимые реакции первого порядка.
Задача 1. Некоторое вещество ![]() , концентрация которого в момент
, концентрация которого в момент ![]() равна
равна ![]() , подвергается превращению в процессе необратимой реакции первого порядка при постоянных условиях. Требуется получить уравнение кинетической линии и найти константу скорости реакции.
, подвергается превращению в процессе необратимой реакции первого порядка при постоянных условиях. Требуется получить уравнение кинетической линии и найти константу скорости реакции.
Решение. ![]() . Кинетическое уравнение:
. Кинетическое уравнение: 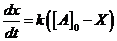 ,
, 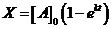 ,
, 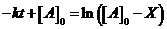 ,
, 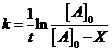 .
.
Для нахождения ![]() выбираем экспериментальные точки
выбираем экспериментальные точки ![]() , находят по формуле
, находят по формуле ![]() , в качестве
, в качестве ![]() берут среднее арифметическое значение.
берут среднее арифметическое значение.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |




