Обратимые реакции первого порядка.
Рассмотрим одностадийную обратимую реакцию первого порядка:
![]() .
.
Выражение для скорости превращения вещества ![]() будет иметь вид
будет иметь вид ![]() . Вспомним (9):
. Вспомним (9): ![]() . Получим кинетическое уравнение
. Получим кинетическое уравнение ![]() или
или ![]() , где
, где ![]() .
.
Задача 2. Некоторое вещество ![]() , концентрация которого в момент
, концентрация которого в момент ![]() равна
равна ![]() , участвует в обратимой реакции, где оба процесса являются реакциями первого порядка. Требуется получить уравнение кинематической кривой и найти
, участвует в обратимой реакции, где оба процесса являются реакциями первого порядка. Требуется получить уравнение кинематической кривой и найти ![]() .
.
Решение. ![]() , где
, где ![]() .
. ![]() отсюда следует, что
отсюда следует, что ![]() . Начальное условие:
. Начальное условие: ![]() откуда следует, что
откуда следует, что ![]() ;
; ![]() ;
; 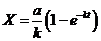 .
.
Найдем выражение для концентраций исходного вещества и продукта:
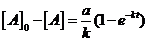 . Отсюда
. Отсюда 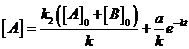 ;
; 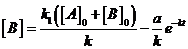 .
.
Устремим ![]() :
:
![]() ;
; ![]() .
.
Выразим ![]() :
:
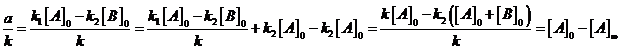
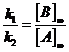 . Найдем
. Найдем ![]() : выражение для
: выражение для ![]() запишем в виде
запишем в виде ![]() . Отсюда
. Отсюда ![]() , отсюда
, отсюда 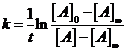 . Получим
. Получим ![]() ;
; ![]() , где
, где 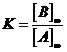 .
.
Обратимые реакции разных порядков.
Пример. ![]() . Будем исходить из допущения, что разложение
. Будем исходить из допущения, что разложение ![]() – реакция второго порядка, обратимая реакция – первого порядка.
– реакция второго порядка, обратимая реакция – первого порядка.
![]() ,
, ![]()
![]() . С другой стороны
. С другой стороны ![]() . Исключив
. Исключив ![]() , получим
, получим
![]() . Устремим
. Устремим ![]() :
: ![]() . Вычитаем одно из другого:
. Вычитаем одно из другого: 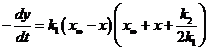 . Обозначим
. Обозначим ![]() ,
, ![]() . Тогда
. Тогда ![]() . Учитывая, что
. Учитывая, что ![]() , приводим уравнение к виду
, приводим уравнение к виду ![]() .
.
Последовательные реакции.
Имеется процесс, протекающий по схеме: 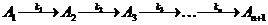 ,
, ![]() – константа скоростей реакций.
– константа скоростей реакций.
![]() – скорость накопления вещества
– скорость накопления вещества ![]() .
. ![]() . Обозначим
. Обозначим ![]() ,
, ![]() . Тогда получим кинетические уравнения процесса:
. Тогда получим кинетические уравнения процесса:
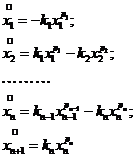 , где
, где ![]() – порядки реакций
– порядки реакций
Математической моделью рассматриваемого процесса является система обыкновенных дифференциальных уравнений.
Задача 3. Известно, что двухстадийная последовательная реакция протекает следующим образом: первая стадия – реакция второго порядка; вторая стадия – реакция первого порядка. Установить функциональную зависимость концентраций исходного вещества и продукта реакции от времени 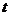 , если известны константы
, если известны константы ![]() ,
, ![]() и начальные условия: концентрация исходного вещества равна 1, концентрация продукта равна 0.
и начальные условия: концентрация исходного вещества равна 1, концентрация продукта равна 0.
Решение. Обозначим концентрацию исходного вещества через ![]() , продукта – через
, продукта – через ![]() . Тогда получим
. Тогда получим ![]()
![]()
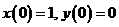 . Из первого уравнения с учетом начальных условий
. Из первого уравнения с учетом начальных условий ![]() . Тогда для
. Тогда для ![]() имеем уравнение
имеем уравнение ![]() . В явном виде оно не решается (смотреть [1]).
. В явном виде оно не решается (смотреть [1]).
Построение кинетических кривых для двухстадийной реакции.
Имеется двухстадийная необратимая реакция, каждая стадия представляет собой реакцию первого порядка ![]() . Процесс описывается следующей системой:
. Процесс описывается следующей системой:
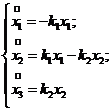 где
где ![]() ,
, ![]() .
.
Задача 4. Построить кинетические кривые для каждого из веществ, участвующих в процессе. Найти max концентрации промежуточного вещества.
Решение. Из первого уравнения системы находим 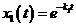 ; получаем
; получаем 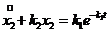 откуда
откуда 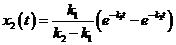 при
при ![]() и
и 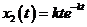 при
при 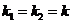 .
.
Точкой max ![]() в первом случае является
в первом случае является ![]() , во втором –
, во втором – ![]() . Точка перегиба в любом случае
. Точка перегиба в любом случае ![]()
![]() .
.
Для построения кинетической кривой вещества ![]() учтем, что
учтем, что 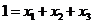 . Получим:
. Получим: ![]() возрастает,
возрастает, 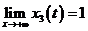 . Точка перегиба
. Точка перегиба ![]() совпадает с точкой max
совпадает с точкой max ![]() .
.
Последовательность двух обратимых реакций первого порядка.
![]() ,
, ![]() – концентрации
– концентрации ![]() .
.
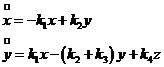
Кроме того, ![]() , т. е.
, т. е. ![]() .
. ![]() . Получаем систему
. Получаем систему
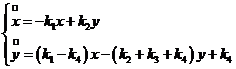
Затем ![]() , и т. д.
, и т. д.
Последовательно-параллельные реакции первого порядка.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |




