Второй этап относиться к периоду 40-50 годов ХХ века и связан с развитием методов измерения каталитической активности в безградиентных условиях проточно-циркуляционного метода. Использование методов значительно повысило достоверность каталитических экспериментов и сделало возможным прямое измерение скорости каталитической реакции и ввести понятие об удельной каталитической активности (УКА) . Особо подчеркивалось, что изменение скорости химической реакции в гетерогенном катализе вызывается промежуточным поверхностным химическим взаимодействием реагирующих веществ с катализатором. При этом основными факторами, определяющими УКА, являются химический состав и химическое строение катализатора, а повышение общей активности объема катализатора существенно зависит от увеличения работающей поверхности.
Генезис катализаторов
Области применения гетерогенного катализа за последнее время настолько расширились, что его можно считать основным способом проведения технических газовых реакций. Соответственно этому возрастает удельный вес работ по изысканию активных катализаторов для ускорения определенных химических реакций.
Ведущая роль в этих исследованиях придается химической индивидуальности вещества, и именно в этом направлении систематизировался экспериментальный материал, что особенно ярко бросается в глаза при рассмотрении патентной литературы.
Совершенно очевидна, однако, недостаточность характеристики катализаторов только по их составу. Наряду с химической индивидуальностью каталитическая активность определяется также совокупностью большого числа факторов, не зависящих от состава, но меняющихся в зависимости от способов приготовления катализатора. Оптимальные условия получения активных образцов ограничиваются определенными интервалами концентраций, температур предварительной обработки и др. По мере усложнения состава катализаторов влияние условий приготовления проявляется все более резко, и допустимый интервал их колебаний сводится к строгой рецептуре, уже небольшие отклонения от которой приводят к резкому ухудшению полученного катализатора.
При отыскании факторов, меняющих каталитическую активность при постоянном составе, в первую очередь обращает на себя внимание развитие поверхности. Действительно, активность контактной массы, выражаемая константой скорости реакции или другой аналогичной величиной, относится обычно к единице веса или объема катализатора. Поэтому, считая реакцию протекающей на поверхности гетерогенного катализатора, мы должны предположить наличие следующей зависимости:
К = сF = с1 ![]() (1)
(1)
где F — поверхность единицы веса или объема катализатора; D — средний поперечник частицы катализатора.
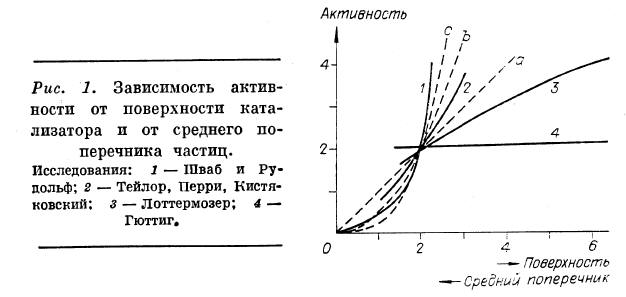
Катализатор представляет собой обычно весьма сложные агрегаты отдельных кристаллов, и остается открытым вопрос о том, поперечник каких частиц, первичных или вторичных, оказывает решающее влияние на каталитическую активность. Помимо этого, применимость уравнения (1) ограничивается предположением о неоднородности поверхности катализатора и протекании реакции лишь на особых активных местах (Тэйлор). Некоторыми авторами эти активные места принимаются идентичными ребрам отдельных кристаллов (Шваб и Питч), что приводит к замене уравнения (1) выражением
K=c![]() (2)
(2)
другими - углам кристаллов (Странский), что соответствует обратной пропорциональности активности третьей степени поперечника:
K=c![]() (3)
(3)
Существуют также предположения о протекании реакции внутри катализатора (Шмидт), чему должна соответствовать независимость каталитической активности от развития поверхности, во всяком случае начиная с определенной крупности частиц. Экспериментальные исследования этого вопроса чрезвычайно бедны количественным материалом и не лишены противоречий. Основная причина встречающихся расхождений заключается в отсутствии надежной методики измерения поверхности. При различных способах - микроскопическом исследовании, рентгенографическом,. адсорбцци, скорости растворения и др.— измеряются, вероятно, различные величины. Результаты исследований представлены на рис. 1, где кривым а, b, с соответствуют уравнения (1), (2) и (3).
Наиболее актуальной задачей генезиса является поэтому борьба с рекристаллизацией, изыскание способов консервирования активной нарушенной решетки. При изготовлении технических контактных масс это достигалось двумя способами:
1) применением носителей, 2) введением добавок. Первый способ основывается на замедлении рекристаллизации благодаря взаимодействию активного вещества с носителем. Второй метод заключается в уменьшении скорости роста кристаллов путем создания межкристаллитных прослоек из добавок, распределенных вначале равномерно внутри вещества и отбрасываемых в процессе кристаллизации катализатора к периферии кристаллитов. Этот способ позволяет повысить температуру начала кристаллизации до предела устойчивости прослойки. Наиболее ярким примером применения этого метода изготовления активных контактных масс являются железные катализаторы для синтеза аммиака с добавками трудно восстанавливаемых окислов. Как показали Миташ и Кейнеке, роль этих добавок сводится к повышению устойчивости. Не содержащие добавок катализаторы обладают вначале такой же активностью, как и активированные, однако они очень быстро снижают свою активность вследствие рекристаллизации. Аналогичную роль приписывает Натта окиси алюминия и хрома по отношению к цинковым катализаторам при синтезе метанола.
Первоначальный комплекс, образующий при последующей обработке скелет, содержащий активный компонент, должен удовлетворять следующим требованиям: 1) хорошему развитию поверхности на единицу веса и объема, 2) термической стойкости, 3) широкой возможности вариаций состава.
Вопросы для самоконтроля:
1.Что представляют собой растворы?
2.Предельно разбавленные растворы?
3.Как определяют коэффициент активности?
Рекомендуемая литература:
1 Основная литература
1 Промышленный катализ. Под ред проф . М.: Калвис. 2005. – 136с.
2 Крекинг нефтяных фракций на цеолитсодержащих катализаторах. Под. ред. . М., Химия, 2002
3 Технология переработки нефти и газа. Крекинг нефтяного сырья и переработка углеводородных газов (ч. 2). М., Химия, 2010
4 , , Технология переработки нефти, газа и ТГИ.–С.-П.: Недра, 2009.– 832 с. (Глава 2– Основы химмотологии моторных топлив и смазочных масел, с. 43–104).
5 Горючее, смазочные материалы: Энциклопедический толковый словарь-справочник/ Под ред. .–М.: Техинформ, 2007.–736 с.
6 Нефть и нефтепродукты: Энциклопедия международных стандартов.–М.: Протектор, 2006.–1040 с.
7 Экология переработки углеводородных систем.–М.: Химия, 2002.–608 с.
2 Дополнительная литература
1 , Технология переработки нефти.–Ч. 2. Деструктивные процессы.–М.: Колос, 2007.–334 с.
2 Технология переработки природных энергоносителей.–М.: Химия Колос.2005 – 456 с.
3 , . Руководство к лабораторным занятиям. Л: Химия, 2000.-240с
Лекция 5. Основные этапы и методы приготовления катализаторов
План:
1. Способы приготовления катализаторов
2. Этапы приготовления катализаторов
Синтез всех высокодисперсных систем, в том числе и большинство твердых катализаторов, может быть осуществлен двумя способами: конденсацией или диспергированием. Под конденсацией понимают образование гетерогенной дисперсной системы из гомогенной в результате ассоциации молекул, атомов или ионов в агрегаты. Методом конденсации дисперсные твердые тела могут быть получены как из жидкой, так и из газовой формы. Диспергирование – дробление или измельчение макроскопических фаз до микроскопических размеров, достигаемых в некоторых случаях размеров коллоидных частиц. Диспергирование может осуществляться механическим воздействием на твердое тело, в результате фазовых превращений, а также за счет удаления части непористого материала путем химического или термического воздействия на него. Приготовление катализаторов от начальной стадии подготовки исходных веществ до операции получения товарного продукта определенной формы и размера представляет собой многоэтапный и многостадийный процесс. Процесс приготовления всех катализаторов можно условно разделить на три основных этапа:
1. Выбор и подготовка исходных веществ.
2. Получение активного компонента заданного состава
3. Переработка катализаторной массы в товарный продукт (изделие)
Первый этап включает в себя выбор по определенным критериям исходных веществ; приготовление растворов и золей для метода осаждения или нанесения; измельчение солей, оксидов, гидроксидов для метода механического смешения
Переработка катализаторной массы в товарный продукт заключается в придании катализатору определенной формы и размера, для чего используются следующие основные методы формования:
1) формование порошков и паст методом экструзии;
2) жидкофазное или газофазное формование;
3) формование порошков методом таблетирования;
4) формование порошков методом окатывания.
Рассмотрим второй этап приготовления катализаторов, т. е. получение активного компонента различными методами. Деление на методы основано по названию ключевой стадии, входящий в данный метод и в значительной степени определяющей основные характеристики и свойства получаемого катализатора.
І. В качестве более эффективного способа приготовления катализаторов рекомендуется метод совместного осаждения. Этот метод в результате одновременного осаждения катализатора и носителя приводит к образованию тонкодисперсного катализатора высокой активности. Хотя для приготовления катализатора выгоднее пользоваться другими методами, полагают, что метод совместного осаждения во всех без исключения случаях обеспечивает получение наиболее активной формы катализатора.
Методы осаждения из растворов (или соосаждение для многокомпонентных систем) включают стадии гелеобразования или получения осадков с последующими стадиями старения (кристаллизации), промывки, фильтрации, сушки и термообработки. Формование осажденных катализаторов в зависимости от физико-химических свойств осадков может осуществляться сразу же после стадии осаждения методами жидкостного или газофазного формования, после стадии фильтрации методом экструзии или после стадии прокаливания методом таблетирования. Методы осаждения из растворов следует рассматривать как частный случай конденсационных методов получения дисперсных материалов в виде порошков и суспензий. Осаждение позволяет достаточно надежно регулировать химический и фазовый состав, дисперсность и морфологию промежуточных продуктов, из которых при последующих соответствующих термообработках получают готовые каталитические системы. Данный метод достаточно универсален. С его помощью готовят как однокомпонентные, так и многокомпонентные каталитические системы различного химического состава, в том числе принадлежащие к классу нанесенных катализаторов. К недостаткам можно отнести использование агрессивных реагентов (кислот и оснований), а также большое количество сточных вод и вредных выбросов, которые необходимо утилизировать.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |


