МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РЕСПУБЛИКИ КАЗАХСТАН имени ШАКАРИМА г. СЕМЕЙ | ||
Документ СМК 3 уровня | УМКД | УМКД 042-18-10.1.17 /03-2014 |
УМКД Учебно-методические материалы «Технология переработки углеводородного сырья» | Редакция №1 от 01.01.2001г |
УЧЕБНО-МЕТОДИЧЕСКИЙ КОМПЛЕКС
ДИСЦИПЛИНЫ
«ТЕХНОЛОГИЯ ПЕРЕРАБОТКИ УГЛЕВОДОРОДНОГО СЫРЬЯ»
для специальности
5В072100 – «Химическая технология органических веществ»
УЧЕБНО-МЕТОДИЧЕСКИЕ МАТЕРИАЛЫ
Семей
2014
Содержание
1 Глоссарий
2 Лекции
3 Практические и лабораторные занятия
4 Самостоятельная работа обучающегося
1 ГЛОССАРИЙ
Раздел глоссарий создается при необходимости (не обязательный)
2 ЛЕКЦИИ
Структура лекционного занятия:
Микромодуль1. Введение и основные понятия катализа
Лекция 1. Введение. История катализа. Определение катализа и катализатора. 1ч
План:
1. История катализа
2. Явление катализа и понятие катализатора.
Слово «катализ», вероятно, впервые введено в 16 веке химиком А. Либавиусом в его учебнике «Алхимия» и имело значение «разложение» или «разрушение». В 1835 г. этот термин узаконен И. Берцелиусом для реакций, протекающих в присутствии посторонних соединений, которые сами как будто в реакции не участвуют. Точнее Берцелиус писал о каталитической силе, приводящей к разложению тел. Примерно в то же время Митчерлих ввел термин «контактное действие».
На самом деле даже “небиологический”, т. е. неферментативный катализ был известен задолго до Либавиуса и тем более Берцелиуса.
Первый известный нам пример небиологического каталитического процесса - синтез диэтилового эфира из спирта при участии серной кислоты (VIII в., Джабир ибн Хайам).
C2H5OH + HO-C2H5 > H2O + C2H5-O-C2H5
Вторично эта реакция была открыта в 1540 г. Валерием Кордусом и получила технологическое оформление в работах С. Фробениуса.
В XVII и XVIII вв. во время создания научных основ химии было открыто несколько каталитических реакций с участием небиологических катализаторов. Так, в 1666 г. А. Лефебр и Н. Лемери разработали камерный способ синтеза серной кислоты базируясь на предыдущих разработках. Это XVII век. И только в конце следующего, XVIII века, механизм синтеза серной кислоты изучен М. Клеманом и Х. Дезормом. Они доказали, что в реакции участвуют не только реагенты (SO2 и O2), но и оксиды азота:
NO2 + SO2 + H2O > NO + H2SO4
NO + 1/2O2 > NO2
Ката?лиз (греч. ????????? восходит к ????????? — разрушение) — избирательное ускорение одного из возможных термодинамически разрешенных направлений химической реакции под действием катализатора(ов), который многократно вступает в промежуточное химическое взаимодействие с участниками реакции и восстанавливает свой химический состав после каждого цикла промежуточных химических взаимодействий.
Термин «катализ» был введён в 1835 году шведским учёным Йёнсом Якобом Берцелиусом.
Явление катализа распространено в природе (большинство процессов, происходящих в живых организмах, являются каталитическими) и широко используется в технике (в нефтепереработке и нефтехимии, в производстве серной кислоты, аммиака, азотной кислоты и др.). Большая часть всех промышленных реакций — каталитические.
Случай, когда катализатором является один из продуктов реакции или ее исходных веществ, называют автокатализом.
Катализатор изменяет механизм реакции на энергетически более выгодный, то есть снижает энергию активации. Катализатор образует с молекулой одного из реагентов промежуточное соединение, в котором ослаблены химические связи. Это облегчает его реакцию со вторым реагентом. Важно отметить, что катализаторы ускоряют обратимые реакции как в прямом, так и в обратном направлениях. Поэтому они не смещают химическое равновесие.
По влиянию на скорость реакции катализ многие источники делят на положительный (скорость реакции растет) и отрицательный (скорость реакции падает). В последнем случае происходит процесс ингибирования, который нельзя считать 'отрицательным катализом', поскольку ингибитор в ходе реакции расходуется.
Катализ бывает гомогенным и гетерогенным (контактным). В гомогенном катализе катализатор состоит в той же фазе, что и реактивы реакции, в то время, как гетерогенные катализаторы отличаются фазой.
Гомогенный катализ
Примером гомогенного катализа является разложение пероксида водорода в присутствии ионов йода. Реакция протекает в две стадии:
H2О2 + I > H2О + IO
H2О2 + IO > H2О + О2 + I
При гомогенном катализе действие катализатора связано с тем, что он вступает во взаимодействие с реагирующими веществами с образованием промежуточных соединений, это приводит к снижению энергии активации.
Гетерогенный катализ
При гетерогенном катализе ускорение процесса обычно происходит на поверхности твердого тела — катализатора, поэтому активность катализатора зависит от величины и свойств его поверхности. На практике катализатор обычно наносят на твердый пористый носитель.
Механизм гетерогенного катализа сложнее, чем у гомогенного. Механизм гетерогенного катализа включает пять стадий, причем все они обратимы.
Диффузия реагирующих веществ к поверхности твердого вещества Физическая адсорбция на активных центрах поверхности твердого вещества реагирующих молекул и затем хемосорбция их Химическая реакция между реагирующими молекулами Десорбция продуктов с поверхности катализатора Диффузия продукта с поверхности катализатора в общий потокПримером гетерогенного катализа является окисление SO2 в SO3 на катализаторе V2O5 при производстве серной кислоты (контактный метод).
Течение реакции именно на поверхности катализатора можно продемонстрировать на опыте, в котором пластинку из платины нагревают в пламени газовой горелки, затем пламя тушат и пускают на пластинку струю газа из горелки, при этом пластинка снова раскаляется докрасна — окисление метана происходит на поверхности металла.
Вопросы для самоконтроля:
1.Что представляет собой серебро?
2. Что представляет собой золото?
Рекомендуемая литература:
1 Основная литература
1 Промышленный катализ. Под ред проф . М.: Калвис. 2005. – 136с.
2 Крекинг нефтяных фракций на цеолитсодержащих катализаторах. Под. ред. . М., Химия, 2002
3 Технология переработки нефти и газа. Крекинг нефтяного сырья и переработка углеводородных газов (ч. 2). М., Химия, 2010
4 , , Технология переработки нефти, газа и ТГИ.–С.-П.: Недра, 2009.– 832 с. (Глава 2– Основы химмотологии моторных топлив и смазочных масел, с. 43–104).
5 Горючее, смазочные материалы: Энциклопедический толковый словарь-справочник/ Под ред. .–М.: Техинформ, 2007.–736 с.
6 Нефть и нефтепродукты: Энциклопедия международных стандартов.–М.: Протектор, 2006.–1040 с.
7 Экология переработки углеводородных систем.–М.: Химия, 2002.–608 с.
2 Дополнительная литература
1 , Технология переработки нефти.–Ч. 2. Деструктивные процессы.–М.: Колос, 2007.–334 с.
2 Технология переработки природных энергоносителей.–М.: Химия Колос.2005 – 456 с.
3 , . Руководство к лабораторным занятиям. Л: Химия, 2000.-240с
Лекция 2. Типы каталитических систем. Понятие о каталитической активности (1ч)
План:
1. Сущность каталитического действия
2. Активный центр катализатора
3. Классификации катализаторов
4. Каталитическая активность катализатора
Если энергия активации высока, то лишь небольшая доля сталкивающихся молекул имеет энергию, достаточную для того, чтобы произошла реакция, а если она низка, то реагирует большая часть молекул, и поэтому константа скорости будет большой. Из этого следует, что если каким-либо образом можно снизить энергию активации, то реакция должна протекать с более высокой скоростью.
Катализатор - это вещество, которое заставляет реакцию протекать быстрее, снижая энергию активации лимитирующей стадии. Некоторая мера эффективности катализаторов может быть получена при рассмотрении изменений энергии активации различных реакций, которые обусловлены наличием катализаторов. При разложении перекиси водорода в отсутствие катализатора энергия активации равна 76 кДж/моль, и при комнатной температуре разложение протекает очень медленно. Если добавить небольшое количество иодида, происходит та же самая реакция, но с энергией активации 57 кДж/моль, и, таким образом, при комнатной температуре (когда RT = 2,5 кДж/моль) константа скорости лимитирующей стадии увеличивается в
Катализ обусловлен промежуточным химическим взаимодействием реагирующих веществ с катализатором, в результате которого открывается новый реакционный путь. Ускорение процессов с помощью катализаторов достигается за счет того, что появляются новые механизмы, при которых медленные стадии заменяются более быстрыми.
Реакция превращения веществ А и В в вещество АВ с участием катализатора К осуществляется по следующей схеме:
A + K > AK
АК + В > АВ + К
А + В > АВ.
Независимо от механизма действия роль катализатора с точки зрения энергетики реакции сводится, как показано на рис., к снижению энергии активации (Еакат < Еа ), за счет чего увеличивается константа скорости реакции.
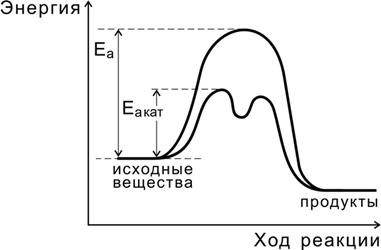
Независимо от механизма действия роль катализатора с точки зрения энергетики реакции сводится, как показано на рис., к снижению энергии активации (Еакат < Еа ), за счет чего увеличивается константа скорости реакции.
Активный центр катализатора
Активный центр катализатора – это атом или группа атомов (ионов) катализатора, при взаимодействии которых с молекулами (ионами, радикалами) реагентов или интермедиатов происходит ускорение химических реакций.
Согласно представлениям об активных центрах, в каталитическом процессе участвует не весь катализатор, а только небольшая его часть. Именно активные центры катализатора участвуют в образовании с исходными реагентами специфической связи, которая приводит к появлению промежуточного соединения, за счёт чего определённые реакции протекают быстрее.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 |


