1) в результате превращения избыточной энергии в тепло (в молекулярное движение), либо в тепло и свет с большей длиной волны (флуоресценция) в том случае, когда лучистая энергия поглощается отдельной молекулой хлорофилла в растворе;
2) в результате передачи энергии (но не электрона) непосредственно соседней молекуле хлорофилла при помощи процесса, называемого резонансной передачей энергии; или
3) путем передачи электрона одной из ближайших молекул (акцептору электрона) и возвращения в первоначальное состояние в результате принятия электрона от какой-то другой молекулы (донора электрона,). Последние два механизма играют ключевую роль в фотосинтезе.
РАССМОТРИМ ДАЛЕЕ ОСОБЕННОСТИ ФОТОСИНТЕЗА У БАКТЕРИЙ И РАСТЕНИЙ
Транспорт возбужденных ?-электронов, обеспечивающий аккумулирование (конвертирование) солнечной энергии в макроэргических связях АТФ, свойствен как хлорофиллсодержащим бактериям, так и зеленым растениям. Хлорофилл обладает уникальной способностью быть как донором, так и акцептором электронов в зависимости от действия на него солнечного света. В исходном состоянии (когда на него не действует свет) хлорофилл служит донором электронов. Поглотив фотон в видимой области солнечного излучения, этот пигмент теряет электрон, окисляется и приобретает акцепторные свойства. Принимая электрон от сопряженных с ним веществ, он
снова испытывает восстановление и становится готовым отдать электроны, если на него вновь подействует свет. Такая цикличность в работе хлорофилла позволяет называть его «электронным насосом», приводимым в действие и регулируемым солнечной энергией.
Это свойство хлорофилла открыто в 1948 г. академиком . Его открытие вошло в науку под названием реакции обратимого фотохимического восстановления хлорофилла (реакции Красновского).
Фотосинтез у хлорофилл у бактерий
Хлорофилл у содержащих бактерий хлорофилл сосредоточен в плазмолемме. Там же присутствуют и другие вещества, участвующие в переносе электронов, которые возбуждаются солнечной энергией в молекуле хлорофилла и покидают ее. Мембрана обеспечивает тесное взаимодействие всех компонентов фотосинтетического комплекса. Благодаря его упорядоченной мембранной организации промежутки между соседними
компонентами этого комплекса имеют порядок 1 нм, что обеспечивает миграцию возбужденных ?-электронов между молекулами по резонансному механизму.
Фотон видимого света, поглощаясь молекулой хлорофилла, возбуждает в ней электрон, который переносится на феофитин, а с него –на убихинон и далее –на цитохром с. Убихинон сосредоточен на внутренней стороне плазмолеммы, а цитохром с –на наружной. Расстояние между ними более 2,5 нм. Чтобы передать электрон цитохрому с, убихинон должен пересечь плазмолемму. Для этого он превращается в убихинол, присоединив вместе
с парой электронов два протона, которые мембрана черпает из цитоплазмы. Убихинол перемещается от внутренней стороны плазмолеммы к наружной и, отдавая там электроны цитохрому с, окисляется с отдачей 2Н+ и выделением их в окружающую среду. Поглощение одного фотона обеспечивает перенос одного Н+-иона через плазматическую мембрану хлорофиллсодержащей бактерии. Содержание Н+ в цитоплазме выше, чем в окружающей среде. Следовательно, система электронного транспорта в фотосинтетическом комплексе плазмолеммы хлорофиллсодержащей бактерии обеспечивает то же, что и бактериородопсин в плазматической мембране галобактерии, –трансмембранный перенос Н+-ионов в соответствии с их концентрационным градиентом.
Пассивный транспорт протонов приводит к эффекту обращения протонной помпы, сосредоточенной также в плазмолемме. В результате Н+-зависимая АТФаза (Н-АТФаза), являющаяся главным компонентом протонного насоса, катализирует не гидролиз АТФ, а его синтез из АДФ и ортофосфата, т. е. выполняет роль АТФсинтазы. За счет АТФ осуществляются все процессы жизнедеятельности хлорофиллсодержащей бактерии, включая поддержание ионных градиентов на ее плазматической мембране.
Такие микроорганизмы не способны синтезировать углеводы за счет работы фотосинтетического комплекса, поскольку возбужденные электроны, отдав фитину, убихинолу и цитохрому избыточную энергию, возвращаются с цитохрома на молекулу хлорофилла.
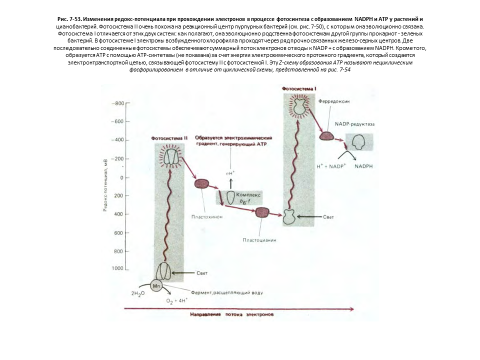
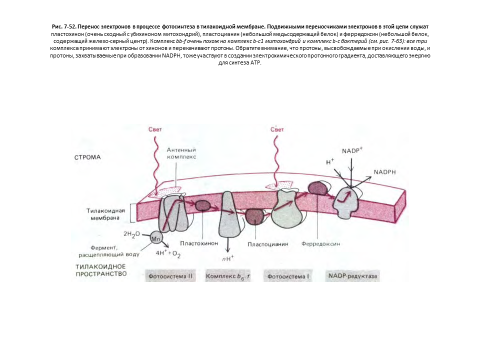
Итак, процесс фотосинтеза представляет собой сложную совокупность реакций по пространственной и временной организации – от 10-15 секунд (в фемтосекундном интервале времени протекают процессы поглощения света) до 104 секунд (образование продуктов фотосинтеза) [7-8].
Понятие «первичные процессы фотосинтеза» включает фотофизические и фотохимические стадии фотосинтеза – процессы поглощения света, миграции энергии, разделения зарядов и формирование электрохимического потенциала в реакционных центрах. Работы последних лет показали очень высокую эффективность первичных процессов фотосинтеза благодаря специфике их структурной организации [3].
Фотосистема содержит реакционный центр и антенный комплекс [32]
Фотосистемами называют состоящие из множества белков комплексы, которые катализируют преобразование энергии света через энергию возбужденных молекул хлорофилла в биологически полезные формы. Фотосистема содержит два тесно связанных компонента: фотохимический реакционный центр и антенный комплекс (рис. 7-48).
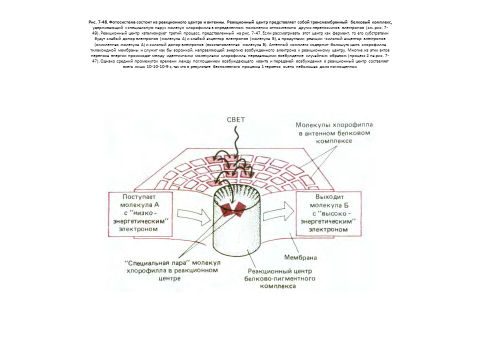
Антенный комплекс необходим для улавливания света. В хлоропластах он представляет собой скопление нескольких сотен молекул хлорофилла, связанных между собой белками, которые прочно удерживают эти молекулы в тилакоидной мембране.
В зависимости от вида растения в каждом комплексе находятся также дополнительные пигменты - каротиноиды, которые способны улавливать свет с другими длинами волн. При возбуждении молекулы хлорофилла в антенном комплексе энергия быстро передается от одной молекулы к другой путем резонансного переноса до тех пор, пока не достигнет двух особых молекул хлорофилла в фотохимическом реакционном центре. Таким образом, каждый антенный комплекс действует как «воронка» собирающая энергию и направляющая ее к специальным участкам, где она может быть использована наиболее эффективно (рис. 7-48).
Фотохимический реакционный центр это трансмембранный белково-пигментный комплекс, составляющий самое «сердце» фотосинтеза. Полагают, что этот комплекс впервые появился у примитивных фотосинтезирующих бактерий более 3 млрд. лет назад. Особая пара молекул хлорофилла в реакционном центре действует как надежная ловушка для энергии возбуждения благодаря тому, что реакционно-способные электроны этих молекул прямо передаются в цепь акцепторов, расположенных в непосредственной близости к хлорофиллу в том же самом белковом комплексе (рис. 7-49).
Электрон от хлорофилла, находящегося в возбужденном состоянии, в реакционном центре передается к близлежащим молекулам, где электрон может находиться в гораздо более стабильном состоянии. Тем самым электрон становится доступным для последующих фотохимических реакций, протекание которых требует времени. Суммарный результат этих медленных реакций заключается в том, что электрон от донора (такого, как вода) переходит в возбужденное состояние в составе сильного донора (такого, как хинон).
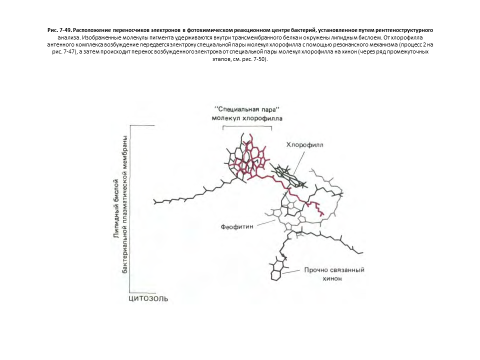
Представление о фотосинтетической единице (ФСЕ) – одно из фундаментальных положений современного фотосинтеза. В его основе лежат две идеи:
о групповом функционировании пигментов (была сформулирована по итогам работ Р. Эмерсона 1943 г., установившего, что в выделении одной молекулы О2 участвует комплекс, содержащий 300 молекул хлорофилла [125]) о функциональной гетерогенности пигментов. В опытах (1930 г.) с определением ассимиляционного числа (СО2/Хл) показано, что не все молекулы хлорофилла фотохимически активны: 99% всех пигментов находятся в антенных комплексах и выполняют функцию сборщиков энергии, и только ~ 1% пигментов, локализованных в реакционных центрах, непосредственно участвуя в процессах преобразования энергии [13].Идея коллективного функционирования пигментов, отраженная в представлении о фотосинтетической единице (ФСЕ), предполагает необходимость их энергетического взаимодействия [9 - 10]. В основе процессов энергетического взаимодействия пигментов антенного комплекса и реакционного центра и взаимодействие молекул хлорофилла а в димере реакционного центра лежит механизм «экситонного взаимодействия», поскольку обмен энергией между молекулами пигментов идет по индуктивно-резонансному механизму Фёрстера [11], в основе которого лежит экситонный перенос энергии.
В антенном (светособирающем) комплексе пигменты четко организованы и ориентированы друг относительно друга [12]. Кроме того, благодаря взаимодействию пигментов с различными аминокислотными группами белков в антенном комплексе присутствует большой набор различных спектральных форм, поэтому пигменты имеют широкий и сильно перекрывающийся спектр поглощения [13]. В результате сильного перекрывания спектров поглощения пигментов в антенне быстро устанавливается равновесие энергии, между пигментами внутри антенны (в течение долей пикосекунд) и между антенной и реакционным центром. При участии серии форм пигментов с различными спектральными характеристиками энергия направленно мигрирует к наиболее длинноволновым пигментам реакционного центра, где происходит захват энергии возбуждения и преобразование её в форму энергии разделенных зарядов [1]. Эффективное экситонное сопряжение между пигментами обеспечивает очень высокую скорость переноса энергии. Так, для переноса возбуждения между молекулами хлорофилла в антенне требуется 300-400 фс, от антенны к реакционному центру – 50-100 пс, тогда как время между поглощением фотона и разделением заряда в реакционном центре – около 100 пс [10 – 11]. Собственно реакция разделения зарядов в РЦ происходит за 3-4 пс.
1.1.2 Реакционный центр ФС2
Реакционный центр был впервые выделен в 1971 г. Л. Верноном [14]. В изучение его структурной организации особый вклад внесли исследования [15], в которых методом дифференциальной спектрофотометрии был выделен пигмент Р680, и лаборатории , в которых методом импульсной спектроскопии был найден первичный акцептор электрона реакционного центра ФС2 – феофетин [16, 17]. Современная модель комплекса ФС2, содержащего реакционный центр, представлена на рис.1.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



