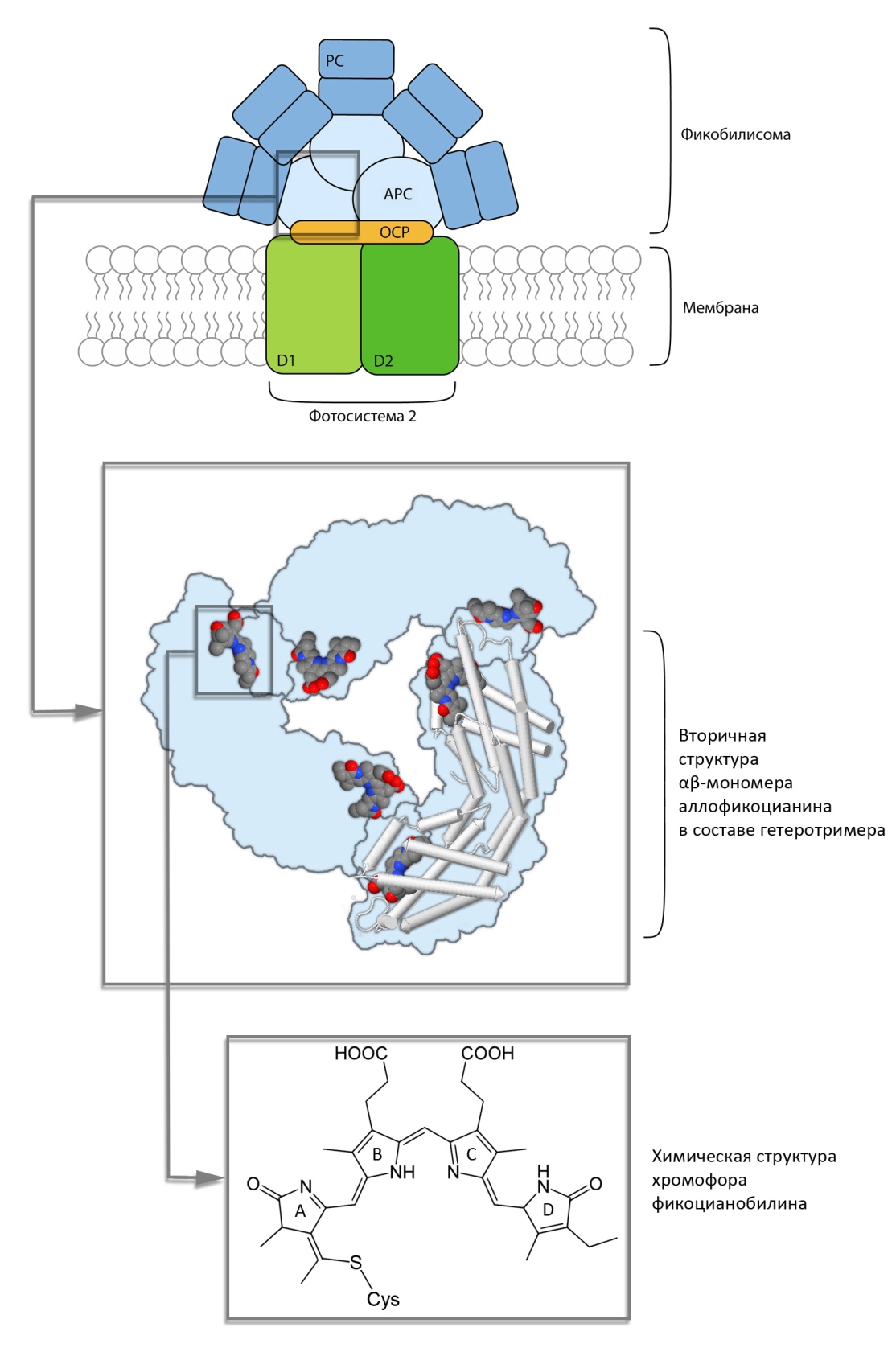
Рис. 3. Сверху: строение фотосинтетических мембран цианобактерии Synechocystis sp. PCC6803. PC – фикоцианин, APC – аллофикоцианин, D1, D2, – белки комплекса ФС2, OCP – orange carotenoid protein. В центре: схематическое представление структуры тримеров аллофикоцианина по данным рентгеноструктурного анализа [25]. Показано расположение хромофоров и элементы вторичной структуры. Снизу: химическое строение хромофора - фикоцианобилина. Пиррольные кольца пронумерованы от A до D.
Согласно рентгеноструктурным данным, ? - и ?-полипептидные субъединицы содержат по две шпильки и восемь ?-спиральных участков, за счет шести из которых формируется общая глобиновая структура этих белков. Хромофорные группы располагаются в промежутках - карманах между ?-спиралями. Оставшиеся две ?-спирали и две шпильки каждой субъединицы образуют взаимодействующие домены, за счет которых происходит образование (??)1-мономеров [33]. Далее мономеры, которые имеют пространственную форму дуг, образуют ?-?-гидрофобный контакт между ?-субъединицей одного мономера и ?-полипептидом следующего, замыкаясь в кольцеобразный тример. Все тримеры, независимо от типа фикобилипротеинов, имеют форму плоских дисков диаметром 11,5 и толщиной 3 нм с отверстием треугольной формы, находящимся в центре диска и также равным по размерам 3 нм [23, 32].
Особое место среди фикобилипротеинов занимают аллофикоцианины (АФЦ), поскольку их структура и фотофизические свойства обеспечивают эффективный захват энергии возбуждения коротковолновых форм фикобилипротеинов [31, 34]. В то же время, АФЦ взаимодействуют с оранжевым-каротин протеином (ОСР) [35, 36] и передают энергию возбуждения терминальными эмиттерам и хлорофиллом реакционных центров [34] (см. рис. 2).
В ряде работ авторы отмечают сложную структуру спектров поглощения тримеров аллофикоцианина, а также зависимость форм спектров от температуры [37, 38, 39]. Основной максимум в спектре поглощения (650 нм) связывают с образованием тримеров и взаимодействием хромофоров находящихся в соседних (??)1-мономерах. При повышении температуры от 25 до 60 °С взаимодействие между хромофорами нарушается, при этом в спектрах поглощения увеличивается вклад компоненты с максимумом 610 нм, что соответствует поглощению мономеров [40].
Таким образом, фотофизические свойства аллофикоцианина являются результатом сложных взаимодействий хромофоров и белков. Поскольку аллофикоцианин, как и другие фикобилипротеины, относится к классу водорастворимых белков, важнейшим фактором, влияющим на свойства аллофикоцианина, является взаимодействие с растворителем.
ФОТОСИНТЕТИЧЕСКИЙ АППАРАТ У РАСТЕНИЙ
Напомним, что фотосинтез у хлорофиллсодержащих бактерий ограничен образованием АТФ за счет реализации протонного градиента на плазматической мембране. Дальнейшая эволюция жизни связана с появлением у зеленых растений способности использовать фотосинтез для созидания углеводов и других высокомолекулярных органических веществ.
Клетки зеленых растений (автотрофов) обеспечивают за счет фотосинтеза питательными веществами, а значит, и свободной энергией как самих себя, так и гетеротрофов. Для синтеза углеводов электроны, возбужденные светом в хлорофилле, должны не только регулировать трансмембранный перенос Н+-ионов, но и переноситься на другие вещества, вплоть до СО2, а не возвращаться в молекулы, которым они прежде принадлежали. Поэтому цепь переноса электронов, замкнутая у хлорофиллсодержащих бактерий, становится разомкнутой у зеленых растений.
Фотосинтез у зеленых растений
Энергия фотонов преобразуется в энергию химических связей синтезируемых органических веществ. Скорость фотосинтеза измеряется количеством кислорода, выделенного за единицу времени. Она зависит от интенсивности поглощенного света. Максимальная скорость фотосинтеза при постоянном сильном освещении достигает одной молекулы О2 (на одну молекулу хлорофилла) за 50 с. Источником всего атмосферного кислорода служит вода, участвующая в реакциях фотосинтеза.
При восстановлении углекислого газа до углевода осуществляется перенос 4 атомов водорода с Н2О на СО2. Изменение свободной энергии в реакциях фотосинтеза при образовании одной молекулы О2 составляет около 500 кДж·моль-1, на что затрачивается 8 квантов света с суммарной энергией примерно 1470 кДж·моль-1. Следовательно, коэффициент использования солнечной энергии при фотосинтезе достигает 34%. Примерно к такому же КПД можно прийти путем другого расчета –при сопоставлении энергии,
заключенной в 8 фотонах, с энергией, затрачиваемой на синтез углеводов.
Свободная энергия, затрачиваемая на транспорт электронов против разности потенциалов при переносе атомов водорода с Н2О на СО2 черпается из фотохимических процессов, в которых участвует хлорофилл. Каждая молекула хлорофилла тесно связана с донором (Д) и акцептором (А) электронов. Поэтому при облучении светом происходят следующие превращения:
Акцептор принимает электрон от возбужденного хлорофилла и превращается в А-. Место этого электрона в хлорофилле занимает другой, принимаемый им от донора. Электрон не может перейти с донора на акцептор непосредственно, так как они пространственно разобщены и не взаимодействуют между собой. Последнее обеспечивается тем, что донор и акцептор являются компонентами биологической мембраны и фиксированы в ее определенных точках. Не взаимодействуя между собой, А - и Д+, образовавшиеся под действием света при участии хлорофилла, могут участвовать в других окислительно-восстановительных реакциях с теми мембранными компонентами, которые тесно контактируют с ними. Вне биомембраны фотосинтез не осуществляется.
Как отмечалось ранее, местом фотосинтеза в зеленых растениях являются мембранные системы хлоропластов. В этом специализированном органоиде, кроме двойной наружной мембраны, содержится сложно организованная сеть внутренних мембран, образующих многослойные структуры, упакованные в пачки (граны). Внутренние мембраны ограничивают замкнутые объемы в виде уплощенных пузырьков –тилакоидов. В каждом хлоропласте примерно 1000 тилакоидов, а в одной клетке –от 50 до 200 хлоропластов. В мембранах тилакоидов протекают светозависимые фотосинтетические реакции, так как там сосредоточены хромофоры –молекулы, поглощающие световую энергию. К ним относятся хлорофилл а, хлорофилл b, каротиноиды и другие пигменты. Хлорофилл поглощает свет наиболее интенсивно в синей и красной, но отражает в зеленой и желтой областях. Этим определяется зеленый цвет растений. На один хлоропласт приходится примерно 109 молекул хлорофилла.
Две разновидности хлорофилла (а и b), имея незначительные различия в химическом строении, существенно отличаются по физическим свойствам и биологической активности.
О коренных отличиях в механизмах переноса энергии свидетельствует наличие флуоресценции у хлорофилла а (с квантовым выходом около 0,2) при ее отсутствии у хлорофилла b. Последний сам по себе непосредственно не участвует в фотосинтетических превращениях, но он входит в состав светособирающей пигментной матрицы, помогающей улавливать солнечную энергию. После фотовозбуждения хлорофилл b быстро передает свою избыточную энергию хлорофиллу а, который при этом возбуждается и принимает непосредственное участие в фотосинтезе. Хлорофилл а может возбуждаться светом и без посредника, но участие хлорофилла b повышает коэффициент использования солнечной энергии.
Как уже мы отмечали, он повышается также благодаря присутствию в светособирающем комплексе других пигментов (каротиноидов и фикобилинов). Сопоставив спектры поглощения хлорофилла и каротиноидов, нетрудно убедиться, что хлорофилл поглощает энергию ограниченного участка солнечного спектра. Однако фотосинтез идет под действием почти всей видимой области электромагнитного спектра, поскольку зеленый свет хорошо поглощают каротиноиды, входящие в светособирающую матрицу. Кроме того, каротиноиды защищают хлорофилл от фотоокисления при избыточном освещении.
Перенос энергии от различных пигментов комплекса на хлорофилл а осуществляется по резонансному механизму. В конце концов, энергия фотовозбуждения достигает реакционного центра, в котором сосредоточено несколько молекул хлорофилла а, ориентированных определенным образом в тилакоидной мембране.
Это первая стадия фотохимического процесса. Совокупность реакционного центра и светособирающей матрицы называется фотосинтетической единицей. Каждая из них включает приблизительно 300 молекул хлорофилла.
Фотосинтетическая единица входит в состав фотосистемы(ФС), компонентами которой являются также интегральные белки тилакоидной мембраны. Мембранные протеины фиксируют многие молекулы хлорофилла на одной полипептидной цепи, создавая тем самым необходимую ориентировку пигмента. Комплекс «хлорофилл а –мембранный белок» служит главным узлом фотосистемы.
Функциональным элементом тилакоидной мембраны считается квантосома, в состав которой входят две фотосистемы, не одинаковые по свойствам. В каждой ФС есть собственная фотосинтетическая единица, причем относительное содержание хлорофилла а в ФС I много выше, чем в ФС II. Обе фотосистемы поглощают свет с длинами волн короче 680 нм, но только ФС I способна возбуждаться и более длинноволновым светом, причем ее максимум поглощения приходится на 700 нм. Поэтому хлорофилл а, входящий в разные фотосистемы, имеет различное наименование: в ФС I его называют пигментом Р700, а в ФС II –пигментом Р680. Различия определяются не особенностями молекулярной структуры пигментов (она одинакова), а специфическим мембранным окружением хлорофилла а в ФС I и ФС II (вероятно, составом мембранных белков, фиксирующих молекулы пигмента). В целом молекулярная масса квантосомы достигает 2·106 дальтон. Между молекулами хлорофилла, принадлежащими разным ФС в одной квантосоме, расположены молекулы других веществ, входящих в ее состав и выполняющих функцию переноса электронов. Поэтому говорят, что ФС I и ФС II разобщены в пространстве тилакоидной мембраны, но сопряжены между собой системой переноса электронов, которые переносятся с ФС II на ФС I, и обратный переход невозможен.
В темноте молекула хлорофилла а пребывает на нижнем синглетном уровне. Световая энергия по резонансному механизму переводит его электроны на более высокий энергетический уровень. Полосы поглощения хлорофилла соответствуют переходам So>S1* (в красной области спектра) и So>S2* (в синей области). Раствор хлорофилла a in vitro флуоресцирует за счет обратного перехода электронов с S1* на S0 (заметим, что обратный переход с S2* на S1 –безызлучательный). С уровня S2* возможен также безызлучательный переход на метастабильный триплетный уровень Т. Находясь на нем, электроны хлорофилла могут перейти под действием света на уровень Т*, что означает возбужденное триплетное состояние хлорофилла. Именно такой переход присущ хлорофиллу in vivo, когда он встроен в тилакоидную мембрану. С уровня Т электроны могут возвратиться и на уровень S0, что сопровождается фотолюминесценцией. Поэтому хлорофилл а люминесцирует не только в пробирке, но и в хлоропластах. Однако его квантовый выход in vivo только 0,03-0,06, тогда как in vitro –0,2. Из сопоставления этих чисел ясно, что львиная доля энергии, выделяющейся при электронных переходах в облученной молекуле хлорофилла а, находящейся в тилакоидной мембране, идет на фотосинтез.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



