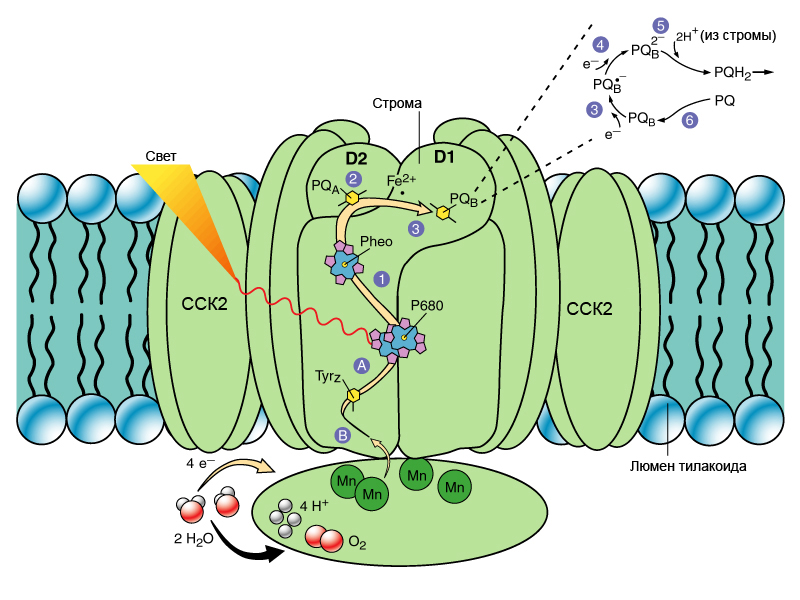
Рис. 1. Структурно-функциональная организация комплекса второй фотосистемы. Показаны белки ядерного комплекса ФС2 D1 и D2, светособирающий комплекс 2 (ССК2), кислород-выделяющий комплекс, основные кофакторы переноса электрона, а также стадии восстановления Qb по [126].
Реакционный центр организован на двух мембранных белках – D1 и D2 [18]. По аминокислотной последовательности они подобны L- и M-субъединицам реакционного центра пурпурных бактерий [19]. Комплекс ФС2 водорослей и высших растений включает около 20 полипептидов, большая часть которых представлена интегральными белками, и только 5 полипептидов располагаются на поверхности мембраны, обращенной к люмену, формируя периферийный домен комплекса.
Структурно и функционально в комплексе ФС2 можно выделить ядро, ряд низкомолекулярных интегральных белков, примыкающих к ядру, функциональная роль которых остается до сих пор не вполне ясной, и белки кислород-выделяющего комплекса (КВК). Реакционный центр ФС2 включает 6 молекул хлорофилла а: две молекулы образуют димер с максимумом поглощения 680 нм (P680), две дополнительные мономерные молекулы располагаются между Р680 и феофетином (на рисунке не показаны); еще две молекулы мономерного хлорофилла с максимумами поглощения 672 и 678 нм (ХлZ и ХлD – сопровождающие пигменты) связаны с внутренней антенной ФС2 – СР43 и СР47, через которую энергия возбуждения поступает в реакционный центр [12, 18]. В состав РЦ входят также две молекулы феофитина, из которых только одна непосредственно участвует в фотохимических реакциях, являясь акцептором электрона [17]. Кроме того, реакционный центр ФС2 содержит две молекулы хинона: Qa в комплексе с железом (Qa?Fe2+) и Qb, а также две молекулы ?-каротина и цитохром b559. Донором электронов для восстановления окисленного Р680 служит тирозин Z (TyrZ), сопряженный с (Mn)4-комплексом фотоокисления воды [20].
Редокс-агенты, участвующие в транспорте электронов ФС2, располагаются в центральной части – ядре – комплекса ФС2 и связаны с интегральными белками D1 и D2. Белки D1 (38 кДа) иD2 (39 кДа) имеют высокую степень гомологии друг с другом по первичной структуре и сходное расположение в мембране. Белки образуют по 5 трансмембранных ?-спиралей, аминокислотные остатки которых и связывают компоненты реакционного центра ФС2, а также редокс-кофакторы вторичного транспорта электронов [19]. Димер Р680 сопрягает белки D1 и D2. Кроме того, к каждому из белков присоединяет еще по 2 молекулы хлорофилла а (дополнительный и сопровождающий хлорофилл), молекулу феофетина а (Фео), ?-каротин и пластохинон (Qa связан с белком D2, а Qb – с белком D1). Между Qa и Qb находится ион двухвалентного железа, в координировании которого участвуют оба белка [3]. Люменальный домен полипептида D1 присоединяет 4 иона марганца и формирует Mn-кластер, осуществляющий окисление воды. По данным рентгеноструктурного анализа, пигмент реакционного центра Р680 располагается в области ФС2, обращенной к люменальному пространству тилакоида [19].
Кроме белков D1 и D2 в состав ядра входят белки СР47 и СР43, которые, связывают около 30 молекул хлорофилла а и составляют внутреннюю (фокусирующую) антенну комплекса [12], а также цитохром b559, включающий ?-и ?-субъединицы, участвующие в циклическом транспорте электронов в ФС2 и белок I [13].
Для эффективного поглощения энергии квантов света молекулы хлорофилла a связаны с молекулами мембранных белков. Передача энергии осуществляется от коротковолновых форм пигментов к длинноволновым, поэтому антенный комплекс является «воронкой», обеспечивающей эффективную передачу энергии, поглощенной молекулой пигмента, на специальные молекулы хлорофилла в РЦ ФС2.
Попавший на РЦ ФСII экситон переводит в возбужденное состояние первичный донор электрона ![]()
![]() (в дальнейшем –
(в дальнейшем –![]()
![]() ), после чего происходит разделение зарядов между
), после чего происходит разделение зарядов между ![]()
![]() и промежуточным акцептором
и промежуточным акцептором ![]()
![]() (феофитином) и передача электрона последовательно на
(феофитином) и передача электрона последовательно на ![]()
![]() и
и ![]()
![]() - стабильные первичный и вторичный акцепторы (молекулы пластохинона). Рассмотренные первичные процессы фотосинтеза можно описать следующей цепочкой ПРЕДСТАВЛЕННОЙ НА РИСУНКЕ [68]:
- стабильные первичный и вторичный акцепторы (молекулы пластохинона). Рассмотренные первичные процессы фотосинтеза можно описать следующей цепочкой ПРЕДСТАВЛЕННОЙ НА РИСУНКЕ [68]:
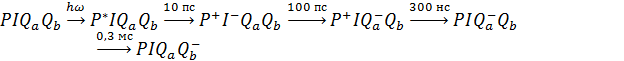
Фотосинтетический аппарат цианобактерий
Фотосинтетический аппарат цианобактерий представлен двумя взаимодействующими между собой фотосистемами (ФС1 и ФС2). Светосбор осуществляется мембранными пигмент-белковыми комплексами, содержащими реакционные центры (РЦ) и коровую хлорофильную антенну [21]. У цианобактерий дополнительными светосборщиками являются фикобилисомы (ФБС) – мультибелковые комплексы, расположенные на поверхности тилакоидной мембраны и примыкающие к ФС I и ФС II [22]. ФБС состоят из содержащих хромофоры фикобилипротеинов и неокрашенных линкерных полипептидов [23]. Молекулы всех фикобилипротеинов состоят из ? - и ?-полипептидных субъединиц, каждая из которых ковалентно связана с фикобилиновым хромофором, представляющим собой линейный тетрапиррол [24]. Для цианобактерии Synechocystis sp. PCC6803 (далее Synechocystis 6803) характерны ФБС полудисковидной формы, основными фикобилипротеиновыми компонентами которой служат С-фикоцианин и аллофикоцианин [25]. Ядро ФБС, примыкающее к стромальной поверхности тилакоидной мембраны, расположено в центре полудиска и представлено в виде трех цилиндров, состоящих из состыкованных друг с другом тримеров аллофикоцианина. Связь ФБС с фотосинтетической мембраной обеспечивается линкерным полипептидом LCM, который состоит из нескольких доменов и участвует также в сборке ядра ФБС [26]. От ядра в радиальном направлении отходят шесть боковых цилиндров, каждый из которых состоит из гексамеров фикоцианина. Энергия света, поглощенного фикобилинами, передается на хлорофилл РЦ ФС1 и ФС2, что позволяет увеличить эффективность фотосинтеза за счет использования света в спектральной области, где поглощение хлорофилла не эффективно [27].
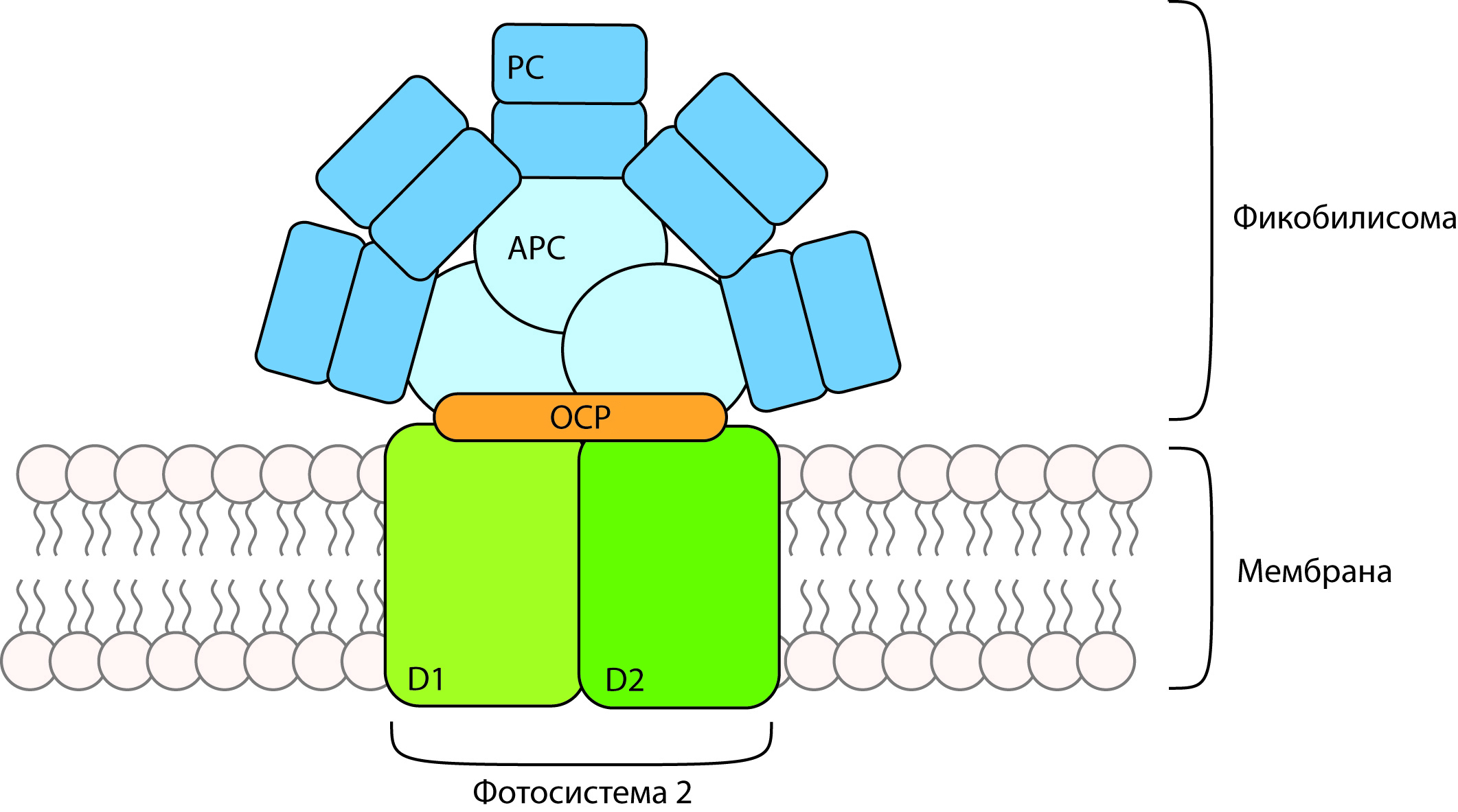
Рис. 2. Фотосинтетическая мембрана Synechocystis sp. PCC6803. PC – фикоцианин, APC – аллофикоцианин, D1, D2, – белки комплекса ФС2, OCP – orange carotenoid protein.
Полностью секвенированный геном и способность к фотогетеротрофному росту делают одноклеточную цианобактерию Synechocystis 6803 удобным объектом для исследования первичных процессов фотосинтеза и, в частности, функций антенных пигмент-белковых комплексов ФБС [28]. Сконструированы мутанты Synechocystis 6803, лишенные одного или нескольких компонентов ФБС [29]. В фикобилисомах мутанта CK, в результате делеции четырех генов, отсутствуют ? - и ?-субъединицы фикоцианина и два линкерных полипептида. У мутанта PAL в результате введения дополнительных делеций в гены, кодирующие субъединицы аллофикоцианина, полностью утрачена фикобилипротеиновая антенна, что подтверждено данными иммунологического анализа и флуоресцентной спектроскопии. Мутантные штаммы сохраняют способность к фотоавтотрофному росту [29, 30].
Фикобилипротеины
Фикобилипротеины (ФБП) выполняют роль светосборщиков в антенных комплексах цианобактерий и красных водорослей - фикобилисомах, поглощая свет и эффективно передавая энергию электронного возбуждения на хлорофилл по фёрстеровскому индуктивно-резонансному механизму. Использование фикобилипротеинов позволяет цианобактериям на порядок увеличить эффективность светосбора реакционными центрами [31]. Интенсивная окраска, высокая концентрация в клетке, водорастворимость, высокий квантовый выход флуоресценции, а также относительная простота выделения сделали их излюбленными объектами белковой химии [23].
Молекулы всех фикобилипротеинов состоят из ? - и ?-полипептидных субъединиц в соотношении 1:1 с молекулярными массами 16 и 18 кДа, соответственно. Фикобилипротеины относятся к кислым белкам с изоточкой в области 4.25 – 4.85 ед. рН. Между двумя субъединицами отсутствуют дисульфидные сшивки, поскольку остатки цистеинов связяны с хромофорными группами фикобилинов [26].
Цистеиновые остатки, образующие тиоэфирные связи с хромофорами фикобилинов, занимают строго фиксированное положение в первичной структуре. Обязательными в связывании хромофоров с апопротеином являются Cys?-84 и Cys?-84 остатки [24]. Дополнительные хромофорные группы включаются в первичную структуру около С-конца ? - или ?-полипептидных субъединиц, на уровне 150-х аминокислотных остатков, и на уровне 50-х остатков, ближе к N-концу. Число хромофоров в (??)1-мономере соответствует разделению фикобилипротеинов на классы, так, например, (??)1-мономер аллофикоцианина содержит два хромофора [26, 32].
Фикобилины относятся к незамкнутым или линейным тетрапирролам, в основе химического строения которых лежат четыре пиррольных кольца, соединенных тремя моноуглеродными мостиками, обозначаемыми как ?-, ? - и ?-мостики.
Для фикобилипротеинов характерна выраженная способность к агрегации. В неденатурирующих условиях в растворах не удается получить отделенные друг от друга ? - и ?-полипептиды фикобилипротеинов, неизменно образующих уже в крайне низкой концентрации, близкой к 10-7 М, (??)1-мономеры, или, точнее говоря, (??)-гетеродимеры. Поверхность (??)1-мономеров гидрофобна, что обеспечивает их высокую стабильность в буферных растворах низкой ионной силы. Самопроизвольная агрегация не обрывается на мономерах и при содержании белка, равном 10-6 М, в растворах преобладают (??)3-тримеры и (??)6-гексамеры фикобилипротеинов [23, 26].

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



