![]()
(6.12)
где V1 - объем 0,1M раствора NaOH, израсходованного на титрование, мл; 0,0071 - масса P2O5, соответствующая 1 мл 0,1 M раствора NaOH,
г/дм3;
мл;
V2 - общий объем раствора, полученный при извлечении P2O5 водой,
А - объем анализируемого раствора, взятого на титрование, мл.
m - масса навески удобрения, г;
ОБРАБОТКА РЕЗУЛЬТАТОВ РАБОТЫ
Одним из основных показателей процесса получения простого суперфосфата является коэффициент разложения сырья. Коэффициент разложения фосфата определяют по формуле:
![]()
где P2O5 усв.- содержание усвояемой формы P2O5 в суперфосфате,
P2O5 общ. - содержание общей формы P2O5 в суперфосфате.
Под выходом понимают массу простого суперфосфата, получаемую на единицу массы фосфата (фосфоритной муки или апатитового концентрата):
![]()
где Gсуп.- масса простого суперфосфата, г
Gф - масса фосфата, г
Состав и характеристика полученного суперфосфата приведены в таблице 1.
Таблица 1
P2O5общ. % | P2O5своб. % | P2O5усв. % | P2O5водораст. % | Коэффициент разложения, % |
КОНТРОЛЬНЫЕ ВОПРОСЫ:
Как получают простой суперфосфат? Что такое степень разложения фосфата и от чего она зависит? Как влияют температура и концентрация применяемой серной кислоты на степень разложения фосфатов? Из каких веществ состоит жидкая фаза суперфосфата в зависимости от вида сырья. Какие вещества представляют твердую фазу готового продукта. Чем отличается сернокислотное разложение апатита и фосфорита Каратау. Как рассчитывается норма серной кислоты при получении простого суперфосфата из апатита и фосфорита Каратау. Каково содержание усвояемой формы P2O5 в готовом продукте, полученном из апатита и фосфорита Каратау. В каких формах существуют P2O5 в продукте. Какие существуют методы улучшения физико-химических свойств суперфосфата, полученного из фосфорита Каратау. ЗАДАНИЕ: Рассчитать нормы и количество кислоты, приготовить удобрение при заданных условиях, определить все формы P2O5 рассчитать показатели процесса.ЛАБОРАТОРНАЯ РАБОТА № 3
Тема: «ПОЛУЧЕНИЕ и АНАЛИЗ ДВОЙНОГО СУПЕРФОСФАТА»
ЦЕЛЬ: практическое изучение процесса получения двойного суперфосфата, приобретение навыков проведения технологического процесса в лабораторных условиях и анализ его качественных технологических показателей.
КРАТКИЕ ТЕОРЕТИЧЕСКИЕ СВЕДЕНИЯ
Сырьем для получения двойного суперфосфата являются природные фосфаты и фосфорная кислота.
Основная реакция, протекающая при получении двойного суперфосфата:
Ca5F(PO4)3 + 7H3PO4 + 5H2O = 5Ca(H2PO4)2H2O + HF (1)
Доломиты, входящие в состав фосфоритов, разлагаются фосфорной кислотой по реакции:
Cа, Мg(CO3)2 + 4H3PO4 + H2O = Ca(H2PO4)2H2O + Mg(H2PO4)2H2O + 2CO2 (2)
Оксиды железа и алюминия, содержащиеся в природных фосфоритах, также разлагаются фосфорной кислотой и образуются
средние фосфаты:
Аl2O3 + 2H3PO4 + H2O = 2AlPO42H2O (3)
Fe2O3 + 2H3PO4 + H2O = 2FePO42H2O (4)
Фтористый водород, образующийся при разложении фторапатита, реагирует с диоксидом кремния и силикатами с образованием четырехфтористого кремния и кремнефтористой кислоты:
4HF + SiO2 = SiF4 + 2H2O (5)
SiF4 + 2HF = H2SiF6 (6)
Температура разложения фосфоритного сырья в пределах 40….700С не оказывает заметного влияния на скорость разложения фосфата. Но при более высокой температуре ускоряется процесс схватывания и затвердения двойного суперфосфата, а также выделение фторсодержащих газов. Рабочая температура 80…1000С. Норма фосфорной кислоты для разложения
фосфорита 100%, а для разложения апатитового концентрата 105% от стехиометрического расхода. Длительность разложения в смесителе составляет 4…6 минут, в суперфосфатной камере 1,5 часа, на складе …10 суток.
РАСЧЕТ РАСХОДА ФОСФОРНОЙ КИСЛОТЫ
Расход фосфорной кислоты рассчитывают на заданное преподавателем количество фосфатного сырья определенного состава.
Стехиометрический расход фосфорной кислоты, необходимой для разложения 100г апатитового концентрата (в г) рассчитывают по уравнению реакции (1).
Из уравнения следует, что на 1,5 моль Р2О5 в кальцийфторапатите расходуется 7 моль Н3РО4, отсюда:
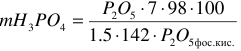 (7)
(7)
Где: Р2О5 апат – концентрация Р2О5 в сырье
98 и 142 – молярные массы Р2О5 и Н3РО4
Р2О5 фос к. т. – концентрация фосфорной кислоты, проценты.
Стехиометрический расход фосфорной кислоты для разложения 100 г фосфорита рассчитывают с учетом содержания в нем САО, MgO, Al2O3, Fe2O3 и Р2O5
Расчет ведут по реакциям (3, 4, 7, 8, 9)
Ca3(PO4)2 + 4H3PO4 + 3H2O = 3Ca(H2PO4)2 H2O (8)
СаО + 2H3PO4 = Ca(H2PO4)2 H2O (9)
2H3PO4 + MgO = Mg (H2PO4)2 +H2O (10)
Пример расчета
Рассчитать расход фосфорной кислоты концентрации 73% H3PO4 при норме 100% фосфоритной муки, содержащей 39,8% САО, 2,5% MgO, 1,5% AI2O3, 1,0% Fe2O3 , 24,5% Р2O5 .
Предварительно рассчитывают массу Ca3(PO4)2, MgO, Al2O3, Fe2O3
и СаО, не связанного в Ca3(PO4)2 , содержащегося в 100 г фосфоритной муки.
Масса Ca3(PO4)2:
где: 310 и 142 – молярная масса Ca3(PO4)2 и Р2O5
24,5 – масса Р2O5, содержащаяся в 100 г фосфоритной муки. Масса СaО, связанного в виде Ca3(PO4)2,
![]()
где: 56 – молярная масса СаО
Масса СаО, не связанного в виде Ca3(PO4)2,
39,8 - 28,99 = 10,81 г
где 39,8 – масса СаО в 100 г фосфоритной муки, г
Масса MgO - 2,5г, Масса Fe2O3 - 1,0 г Масса AI2O3 – 1,5 г
Расход фосфорной кислоты концентрации 100%:

Расход раствора фосфорной кислоты концентрации 73% в граммах.
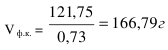
Объем фосфорной кислоты концентрации 73% в мл.
![]()
Где 1,557 г/см3 - плотность фосфорной кислоты концентрации 73%.
Второй вариант расчета. Для опыта необходимо рассчитать расход
фосфорной кислоты. Ее обычно определяют как количество фосфорной кислоты
в г Р2O5 (H3PO4), затрачиваемой на разложение 100г фосфатного сырья
по формуле (при разложении фосфорита Каратау):
HP2O5 = 2,54X1 + 3,55X2 + 1,39X3 + 0,89X4 - X, г
где X1, X2, X3, X4 и X - содержание СаО, MgO, AI2O3, Fe2O3 и Р2O5 в сырье, проценты.
Расход фосфорной кислоты в пересчете на Н3PO4 заданной
концентрации составит:

ОБОРУДОВАНИЕ:
Сушильный шкаф
Химическая посуда
Аналитические и технические весы
Фотоколориметр
ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ И ОБРАБОТКА ПОЛУЧЕННЫХ РЕЗУЛЬТАТОВ
В предварительно взвешенную термостойкую чашку, наливают рассчитанное количество фосфорной кислоты. Нагревают до 80-90oC. Затем при постоянном перемешивании в течение 1-2мин высыпают навеску фосфата. По окончании введения фосфата продолжают перемешивание еще 3-5мин. После этого продукт помещают в сушильный шкаф на 60-90мин., где поддерживают температуру 105-110oC (камерное созревание). Затем продукт охлаждают до комнатной температуры и взвешивают на технических весах.
Далее двойной суперфосфат подвергают анализу на содержание Р2O5 общей, усвояемой, водорастворимой и свободной.
Одновременно надо определить влажность двойного суперфосфата.
Если анализ проводят не сразу по получении, то взвешивают его повторно, перед отбором проб на анализ.
МЕТОДИКА ПРОВЕДЕНИЯ АНАЛИЗОВ
Определение общей Р2O5
Приблизительно 1-2г двойного суперфосфата взвешивают на аналитических весах с точностью до 0,0002г, переносят в термостойкий стакан емкостью 250мл и добавляют 50мл раствора соляной кислоты концентрацией 20%НСI, накрывают часовым стеклом и кипятят на медленном огне 30мин., добавляя воду по мере упаривания раствора до объема примерно 50мл. После охлаждения раствор вместе с осадком переносят в мерную колбу емкостью 250мл, доводят дистиллированной водой до метки, перемешивают и фильтруют, отбрасывая первые порции фильтрата. Отбирают пипеткой 1мл фильтрата и переносят в мерную колбу на 100мл, доливают водой до 50мл, прибавляют 25мл реактива на фосфаты (раствор Г) и доводят водой до метки. Через 10...15мин измеряют оптическую плотность относительно раствора сравнения.
Раствор сравнения готовят одновременно с пробой, в мерную колбу на 100мл берут 25 мл раствора Г и доводят дистиллированной водой до метки. Раствор сравнения используется для определения всех форм Р2O5 и готовят один раз.
Содержание P2O5 в массовых процентах вычисляют по формуле:
![]() (11)
(11)
где V1 - масса Р2O5, найденная по калибровочному графику, мг; m - масса анализируемого вещества, г;
W - объем мерной колбы, мл;
V2 - объем анализируемого раствора, отобранный на анализ, мл.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



