Определение усвояемой P2O5
Приблизительно 1...2г двойного суперфосфата взвешивают на аналитических весах с точностью до 0,0002г помещают в мерную колбу емкостью 500мл через сухую воронку, смывая навеску раствором трилона Б (конц.0,2моль/дм3), предварительно нагретого в стакане до температуры 93±3oС, в количестве 150мл, затем колбу закрывают пробкой и взбалтывают на аппарате для встряхивания 20...30мин. Объем раствора доводят до метки дистиллированной водой, перемешивают, фильтруют через фильтр “белая лента “, отбрасывая первые порции фильтрата.
Отбирают пипеткой 1мл фильтрата и переносят в мерную колбу на 100мл. К раствору добавляют 2мл раствора соляной кислоты (20%), 5...10мл воды, кипятят 10мин, охлаждают и разбавляют водой до 30мл. Затем прибавляют 25мл раствора на фосфаты, доливают водой до метки, перемешивают и через 10...15мин измеряют оптическую плотность, относительно раствора сравнения.
Содержание P2O5 в массовых процентах вычисляют по вышеприведенной формуле (11).
Определение воднорастворимой и свободной форм P2O5
4-5 г двойного суперфосфата взвешивают на аналитических весах с точностью до 0,0002г, помещают в мерную колбу емкостью 500мл. Пробу заливают 400 мл воды и сразу же перемешивают, чтобы избежать образования комков. Колбу закрывают пробкой, устанавливают на аппарат для встряхивания. По истечении 30 мин содержимое колбы доводят до метки, фильтруют через сухой фильтр “белая лента” в сухую посуду, первые порции фильтрата отбрасывают.
Отбирают 1 мл фильтрата и переносят в мерную колбу на 100мл. К раствору добавляют 2 мл раствора соляной кислоты (20% HСl) и 15-20 мл воды, кипятят 10 мин. Охлаждают и разбавляют водой до 50 мл, затем прибавляют 25 мл раствора Г, доливают водой до метки, перемешивают и далее анализируют и рассчитывают как при определении общей формы P2O5 (5.3.1.).
Для определения содержания свободной формы P2O5 50 мл фильтрата, полученного извлечением P2O5 водой, пипеткой переносят в коническую колбу, разбавляют водой до 100...150 мл и титруют 0,1M раствором NaOH в присутствии 3...5 капель метилового оранжевого до перехода окраски из розового в желтый цвет. Содержание P2O5 свободной вычисляют по формуле:
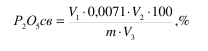 (12)
(12)
где V1 - объем 0,1M раствора NaOH, израсходованного на титрование, мл; 0,0071 - масса P2O5 , соответствующая 1 мл 0,1 M раствора NaOH,
г/дм3;
мл;
V2 - общий объем раствора, полученный при извлечении P2O5 водой, А - объем анализируемого раствора, взятого на титрование, мл.
m - масса навески удобрения, г.
ОБРАБОТКА РЕЗУЛЬТАТОВ РАБОТЫ
Одним из основных показателей процесса получения двойного суперфосфата является степень разложения сырья. Степень разложения природного фосфата определяют по форме:
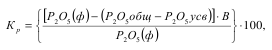 (13)
(13)
где P2O5(ф) - содержание P2O5 в фосфорите, %
P2O5 общ - содержание общейP2O5 в удобрении, %
P2O5 усв - содержание усвояемой P2O5 в удобрении,
% B - выход двойного суперфосфата.
Под выходом принимают массу двойного суперфосфата, получаемую из единицы массы фосфата:
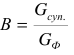 (14)
(14)
где Gсупер - масса двойного суперфосфата, г
Gфосф - масса фосфорита, г
Результаты опытов по получению двойного суперфосфата заносят в таблицу 1.
Таблица 1 Показатели качества двойного суперфосфата
Содержание P2O5 ,% | Выход | Кр,% | ||
в исходном продукте, фосфорите | общ | усв | водор | своб |
КОНТРОЛЬНЫЕ ВОПРОСЫ:
Свойства двойного суперфосфата как удобрения. Виды сырья и их влияние на качество продукта. Факторы, влияющие на степень разложения и состав продукта. Выборы метода получения двойного суперфосфата и их сравнительная характеристика. Обоснование выбора технологических параметров. Методы улавливания фторсодержащих соединений. Пути совершенствования технологии двойного суперфосфата.
ЗАДАНИЕ: Рассчитать расход кислоты для получения заданного количества удобрения. Приготовить двойной суперфосфат. Провести химический анализ и обработать результаты.
ЛАБОРАТОРНАЯ РАБОТА № 4
Тема: «ПОЛУЧЕНИЕ И АНАЛИЗ ПРЕЦИПИТАТА»
ЦЕЛЬ РАБОТЫ: Познакомиться с производством и условиями получения преципитата. Получить на лабораторной установке преципитат нейтрализацией фосфорной кислоты известковым молоком. Выполнить анализ готового продукта на определение общего и цитратнорастворимого Р2O5.
ОБЩИЕ ПОЛОЖЕНИЯ
Преципитат – это фосфорное удобрение, называемое в промышленности и в сельском хозяйстве дикальцийфосфатом CaHPO4·2H2O (дигидрат гидроортофосфата кальция). Содержит в цитратнорастворимой форме Р2O5 (до 41,27 % Р2O5). Цитратнора - створимая форма легко усваивается растениями.
Представляет собой кристаллический порошок белого или кремового цвета. Практически негигроскопичен, не слёживается, обладает хорошей рассеиваемостью. Благодаря хорошим физическим свойствам и высокой агрохимической активности может использоваться на большинстве почв. Применяется также для получения смешанных удобрений.
Несмотря на то, что дикальцийфосфат и является эффективным удобрением, для этой цели его специально не производят, так как фосфорную кислоту выгоднее перерабатывать в двойной суперфосфат, в котором часть Р2O5 извлекается из фосфорита, и поэтому стоимость Р2O5 в двойном суперфосфате значительно меньше, чем в дикальцийфосфате.
Удобрительный преципитат получают при утилизации слабых фосфорнокислотных растворов, например являющихся отходом производства желатина на костеперерабатывающих заводах.
Преципитат получают осаждением (преципитированием) Фосфорнокислотных растворов известковым молоком или водной суспензией измельченного известняка с последующим отфильт - ровыванием, сушкой и измельчением.
Преципитирование – это процесс нейтрализации фосфорной кислоты известью, известняком, в результате чего происходит осаждение преципитата.
При введении в раствор фосфорной кислоты извести (из - весткового молока) или суспензии известняка (мела) они вначале полностью растворяются, образуя монокальцийфосфат (дигидроортофосфат кальция):
Са(ОН)2 + 2Н3РO4 = Са(Н2РO4)2 + 2Н2О;
СаСО3 + 2Н3РO4 = Са(Н2РO4)2 + СO2↑ + Н2О.
Монокальцийфосфат (суперфосфат) по мере нейтрализации фосфорной кислоты, в слабокислой среде инконгруэнтно разлагается с выделением осадка дикальцийфосфата. Кроме того, монокальцийфосфат реагирует с новыми порциями извести или известняка, также образуя дикальцийфосфат:
Са(ОН)2 + Са(H2PO4)2 + 2H2O = 2[СаНРO4·2Н2O];
СаСО3 + Са(Н2РO4)2 + 3Н2O = 2[СаНРO4·2H2O] + CO2↑.
Избыток извести сверх стехиометрического отношения СаО:Р2O5 в дикальцийфосфате и увеличение рН раствора свыше 6,3 приводят к образованию трикальцийфосфата (ортокальцийфосфата):
2СаНРO4 + Са(ОН)2 = Са3(РO4)2 + 2Н2O.
Поэтому преципитирование ведут в строго определенных условиях при рН раствора не больше 6,3. Избыток известняка не вызывает разложения дикальцийфосфата.
Примеси, содержащиеся в экстракционной фосфорной ки - слоте, также реагируют с известью или известняком.
По мере нейтрализации растворов фосфорной кислоты происходит разложение этих примесей:
(Fe, А1)2(SO4)3 + 2Н3РO4 + 4H2O + 3Ca(OH)2
= 2(Fe, A1)PO4·2Н2O + 3CaSO4·2H2O;
H2SO4 + Ca(OH)2 = CaSO4·2Н2О;
H2SiF6 + 3Ca(OH)2 = 3CaF2 + SiO2 + 4H2O;
2HC1 + Ca(OH)2 = CaCl2 + 2H2O.
Примеси уменьшают содержание усвояемого Р2O5 в продукте, илистые осадки фосфатов алюминия и железа, фторида кальция и кремниевой кислоты ухудшают структуру осадка и затрудняют отфильтровывание преципитата.
Примеси также увеличивают расход СаО, необходимый для взаимодействия с кислотой. Теоретический расход СаО на единицу Р2O5 составляет 56:71 = 0,79. Практический, в зависимости от состава фосфорной кислоты, расход СаО на единицу Р2O5 составляет 0,8–0,9 массовых частей.
Поэтому при определении расхода нейтрализующих веществ на преципитирование необходимо учитывать наличие примесей в фосфорной кислоте.
Для получения двухводной соли, лучше усваиваемой растениями, осаждение известняком ведут при температуре 50–60 0С. При использовании для осаждения известкового молока температура должна быть не выше 40 0С во избежание образования трикальцийфосфата.
ПРИБОРЫ И РЕАКТИВЫ
Оборудование: установка для получения преципитата; уста - новка для получения раствора Петермана; фарфоровый стакан на 2 дм3; стеклянный стакан на 250 см3 и на 1 дм3; аналитические и технохимические весы; набор ареометров; мерные цилиндры на 25, 50, 100, 250, 500 см3 и на 1 дм3; мерная колба на 250, 500 см3 и на 1 дм3; коническая колба на 250 см3; пипетки на 10, 25 и 50 см3; фарфоровая чашка; электроплитка; сушильный шкаф; муфельная печь; капельная воронка; часовое стекло; стеклянная палочка; стеклянный бюкс; фильтровальная бумага; фильтр «синяя лента»;
фарфоровая ступка с пестиком; фарфоровый тигель; водяная баня; термометр.
Реактивы: H3PO4 (конц.); HNO3 (конц.); CaCO3 (крист.); CaO (крист.); вода дистиллированная; HCl (20 %-й раствор); цитрат аммония (50 %-й раствор); раствор NaOH (0,1н.); раствор аммиака (2,5; 10 и 25 %-й); раствор H2SO4 (0,1н.); магнезиальная смесь, щелочная; раствор Петермана; лимонная кислота (х. ч.); хлорид аммония (х. ч.); MgCl2·6Н2О (х. ч.).
Индикаторы: фенолфталеин, метиловый красный.
Примечание.
Цитрат аммония (50 %-й раствор) готовят следующим образом. 500 г лимонной кислоты растворяют в 600 см3 25 %-го раствора аммиака. Раствор должен быть нейтральным по метиловому красному, в противном случае его нейтрализуют прибавлением лимонной кислоты или аммиака. Раствор разбавляют водой до 1 дм3, перемешивают и фильтруют.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



