Магнезиальная смесь, щелочная готовится следующим образом. 70 г хлорида аммония и 55 г хлорида магния растворяют в 200–250 см3 воды. К раствору добавляют 250 см3 10 %-го раствора аммиака, разбавляют водой до 1 дм3, перемешивают и оставляют на сутки, после чего фильтруют.
Раствор Петермана. Готовый раствор должен содержать 42 г аммиачного азота и 173 г гидрата лимонной кислоты в 1. Предварительно готовят ≈ 10 %-й раствор аммиака, концентрацию которого проверяют следующим образом.
Пипеткой отбирают 10 см3 10 %-го раствора аммиака и переносят в мерную колбу на 500 см3, в которую налито 400–450 см3 дистиллированной воды. Раствор в колбе доводят дистиллированной водой до метки и тщательно перемешивают. Из колбы отбирают пипеткой 2–3 пробы по 25 см3, переносят их в конические колбы на 250 см3, в которые налито 30 см3 дистиллированной воды, и титруют 0,1 н. раствором серной кислоты в присутствии метилового красного.
Содержание азота (х, г/дм3) в растворе вычисляют по формуле:

где а – объём 0,1н. раствора серной кислоты, израсходованного на титрование, см3.
Так как при приготовлении раствора Петермана расчет ведут на гидрат лимонной кислоты, то коммерческий реактив должен быть предварительно проверен. 100–150 г лимонной кислоты тщательно измельчают в ступке и отбирают в сухой бюкс среднюю пробу. 1 г лимонной кислоты растворяют в дистиллированной воде в мерной колбе на 250 см3, раствор доводят дистиллированной водой до метки и тщательно перемешивают. Две пробы пипеткой на 25 см3 переносят в конические колбы на 250 см3, нагревают до 60–70 0С и в присутствии фенолфталеина титруют 0,1 н. раствором гидроксида натрия до появления розовой окраски.
Содержание гидрата лимонной кислоты (y, г/дм3) вычисляют по формуле:
![]()
где b – объём 0,1н. раствора гидроксида натрия, израсходованного на титрование, см3.
Количество 10 %-го раствора аммиака (m) и лимонной кислоты (n), необходимые для приготовления N литров раствора Петермана вычисляют по соотношениям:
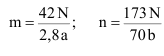
Вычисленное количество лимонной кислоты помещают в стакан и растворяют в горячей воде, используя по 200–250 см3 горячей воды на каждые 173 г лимонной кислоты. Одновременно в бутыль 1 (рис. 1) с меткой, указывающей объём раствора Петермана, наливают вычисленный объём раствора аммиака. Оба раствора охлаждают до 10–15 0С. К охлажденному раствору аммиака через воронку 2 приливают небольшими порциями растворы лимонной кислоты. Во время приливания лимонной ки - слоты раствор в бутыли охлаждают до 10–15 0С. После внесения всей лимонной кислоты воронку промывают водой, вынимают её из бутыли и бутыль закрывают пробкой. Раствор в бутыли осторожно перемешивают и после охлаждения доводят водой до метки, вновь перемешивают и оставляют на 2 дня.
Если раствор Петермана применяют вместо 50 %-го раствора цитрата аммония, то он должен быть предварительно про фильтрован.
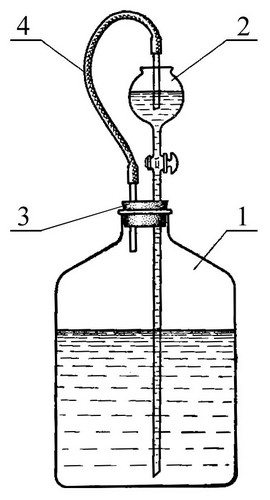
Рис. 1. Бутыль для приготовления раствора Петермана:
1 – бутыль; 2 – воронка с краном; 3 – резиновая пробка ; 4 – трубка для отвода паров аммиака в воронку
ВЫПОЛНЕНИЕ РАБОТЫ
ПОЛУЧЕНИЕ ПРЕЦИПИТАТА
Получение преципитата в лабораторных условиях сводится к нейтрализации фосфорной кислоты известковым молоком или известняком с определением основных технологических показа - телей процесса – коэффициентов осаждения, т. е. общего перехода Р2O5 из раствора в осадок и преципитирования, т. е. степени перехода Р2O5 в преципитат, а также количества преципитата.
Порядок выполнения работы
До начала выполнения опыта рассчитывают необходимое количество известкового молока (известняка) для переработки заданного количества фосфорной кислоты.
Расчет проводят по следующим уравнениям реакций:
CaO + H2O = Ca(OH)2; Н3РO4 + Са(ОН)2 = СаНРO4·2Н2O;
Н3РO4 + СаCО3 = СаНРO4·2Н2O + CO2↑.
Для расчёта используют следующие данные:
Масса Н3РO4 – 100 г. Концентрация Н3РO4 – 85 %. Плотность 85 %-й Н3РO4 – 1,690 г/см3. Концентрация раствора Са(ОН)2 – 92,65 г/дм3. Плотность раствора Са(ОН)2 – 1,054 г/см3. Избыток Са(ОН)2 – 1,5.Приготовление известкового молока.
В фарфоровый стакан на 2 дм3, снабженный мешалкой, вливают сначала небольшое количество воды ≈ 150–200 см3 и при вращающейся мешалке всыпают 7–15 г извести СаО. Каждые 5 мин возобновляют загрузку воды и извести с таким расчетом, чтобы вся операция была закончена в течение 30–40 минут.
Общее количество приготовленного известкового молока должно быть несколько больше рассчитанного количества.
Пробу известкового молока анализируют на содержание СаО титрованием пробы кислотой или ареометрически. Количество известкового молока, необходимое для проведения опыта, определяют в зависимости от концентрации и отмеряют в мерный цилиндр на 1.
Получение преципитата.
Получение преципитата осуществляется на установке, схема которой представлена на рис. 2.
В фарфоровый стакан 1, снабженный термометром 2 и ис - пользуемый в качестве реактора для получения преципитата, вносят мерным цилиндром на 100 см3 рассчитанное количество Н3РO4 (в зависимости от концентрации). Включают мешалку 3, после чего начинают вводить в реактор известковое молоко. Подачу известкового молока осуществляют при помощи капельной воронки 4, куда время от времени наливают суспензию из стакана с мешалкой, со скоростью 10–15 см3/мин. Преципитирование проводят в течение 1–1,5 ч.
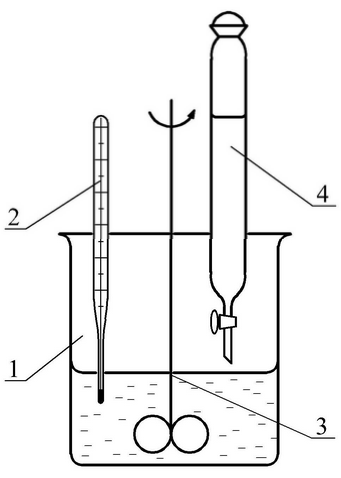
Рис. 2. Схема установки для получения преципитата:
1 – фарфоровый стакан; 2 – термометр; 3 – мешалка; 4 – капель - ная воронка
Медленное приливание известкового молока необходимо для предотвращения образования ортофосфата кальция и резкого повышения температуры, а также для получения более крупнокристаллического осадка преципитата. Процесс преципитирования проводят при температуре 40 0С.
После введения всего необходимого количества известкового молока продолжают перемешивание пульпы еще в течение 30 минут. По истечении указанного времени пульпу переносят на воронку Бюхнера и отфильтровывают раствор от осадка под небольшим разрежением.
Осадок промывают несколько раз водой, взвешивают во влажном состоянии, после чего его высушивают в сушильном шкафу при температуре не выше 100 0С. Определяют содержание влаги в преципитате и практический выход продукта.
Затем готовый продукт подвергают анализу.
Измеряют также объем полученного фильтрата и анализируют его на содержание Р2O5 раствора. Это необходимо для установления количества Р2O5, остающегося в жидкой фазе преципитата и характеристики степени промывки осадка. Данные также используют для установления технологических показателей процесса получения преципитата.
Получение преципитата из известняка
При преципитировании фосфорной кислоты при помощи известняка, применяется более концентрированная суспензия ≈ 150–250 г/дм3, чем известковое молоко. Известняковую пульпу следует приливать в реакционный стакан медленно – из расчета проведения опыта в течение 4–4,5 ч. Известняк применяется с содержанием СаСО3 ≈ 95 %. Фосфорную кислоту берут с концентрацией 10–15 %, а в некоторых опытах возможно применение кислоты с содержанием 5–10 % P2O5 или 40–50 % Р2О5.
При применении кислоты, содержащей значительное количество фтора (≥ 1%), рекомендуется процесс проводить в две стадии. Вначале около 70 % Р2О5 кислоты осаждают известняком, а затем остальное количество – известковым молоком. В этих условиях исключается возможность образования к концу процесса тонкодисперсного осадка.
Обработка результатов
Полученные данные используют для вычисления технологических показателей процесса: коэффициента осаждения P2O5 из раствора и коэффициента преципитирования.
Коэффициент осаждения Р2O5 из раствора ![]() характери
характери
зует степень перехода P2O5 из раствора в осадок. Его рассчитывают по разности между содержанием P2O5 в исходной кислоте и жидкой фазе преципитатной пульпы (%):
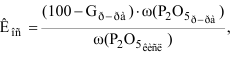
 Коэффициент преципитирования Кпрец. характеризует степень перехода Р2O5 из фосфорной кислоты в преципитат, рассчитывают его по формуле:
Коэффициент преципитирования Кпрец. характеризует степень перехода Р2O5 из фосфорной кислоты в преципитат, рассчитывают его по формуле:
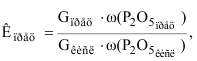

Если осадок не промыт или промыт недостаточно, коэффициент преципитирования несколько больше коэффициента осаждения Р2O5 вследствие того, что в жидкой фазе преципитата содержится часть не осажденной Р2О5.
АНАЛИЗ ГОТОВОГО ПРОДУКТА
В данной работе рассмотрено определение содержания общего и цитратнорастворимого P2O5 и Р2О5 раствора в фильтрате.
Определение общего и цитратнорастворимого P2O5 в преципитате.
Для определения P2O5 применяют весовой или ионитный метод (с объёмным окончанием анализа).
Весовой метод. Весь фосфор, входящий в состав преципитата, переводят в раствор при помощи соляной кислоты. Из раствора ион РО4 осаждают в виде MgNH4PO4·6H2O. Осадок прокаливают до пирофосфата магния Mg2Р2О7 и взвешивают.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



