Газовая коррозия – это разновидность химической коррозии металлов. Она исходит в условиях, исключающих наличие влаги на поверхности металла и возникновение электрохимической коррозии. Поэтому в большинстве случаев считают, что газовая коррозия исходит при повышенной температуре, когда вода находится в газовой фазе, или при обычной температуре, но в сухой атмосфере.
В промышленности газовая коррозия встречается часто, например, коррозия деталей нагревательных печей, коррозия металлов при термообработке и др. На скорость газовой коррозии влияют различные факторы, но прежде всего температура и состав газовой среды. Повышение температуры заметно ускоряет газовую коррозию. Эта зависимость приближённо описывается уравнением Аррениуса:
![]() ,
,
где К – скорость реакции; А и В – константы; Т – абсолютная температура, К. Дополнительное влияние оказывают вторичные реакции, вид и свойства продуктов коррозии и др.
3.3.2 Коррозия в газовой среде при высоких температурах
Коррозионное разрушение поверхностного слоя металлов и сплавов при эксплуатации машин и оборудования при высоких температурах в газовых средах наносит большой ущерб. Потери металла неизбежны как при холодной пластической обработке, так и при термической обработке. Газовая коррозия поражает не только поверхность металла, но может проникнуть и вглубь (например, обезуглероживание, сульфидная и водородная коррозия).
Устойчивость сталей и сплавов против коррозии в газовых средах при высоких температурах зависит от следующих факторов:
- природы металла или состава сплава;
- состава газовой среды;
- температуры, давления и продолжительности нагревания;
- скорости нагревания и охлаждения;
- непрерывности или периодичности режима;
- наличия механических напряжений.
Для предотвращения коррозии сталей и сплавов при высоких температурах применяются следующие методы:
а) введение в сплавы специальных легирующих элементов – Cr, Ni, Al, Si;
б) химико-термическая обработка деталей путём диффузионного насыщения поверхности изделий элементами Cr, Al, Si, Be;
в) покрытие поверхности изделий другими, более окалиноустойчивыми материалами – эмалирование путём порошкового напыления более устойчивыми окисями.
3.3.3 Отдельные виды газовой коррозии
Наиболее часто на практике встречаются следующие виды газовой коррозии:
1) окисление;
2) коррозия в атмосфере азота;
3) коррозия в атмосфере, содержащей водород;
4) карбонильная коррозия;
5) ванадиевая коррозия;
6) коррозия, вызываемая сернистыми соединениями;
7) коррозия газообразным хлором и хлористым водородом.
Ниже рассмотрим основные виды коррозии, имеющие существенное значение для практики.
1 Окисление
При взаимодействии кислорода с металлами и сплавами последние окисляются с переходом через ряд фаз, определяющих скорость окисления. Эти фазы можно классифицировать следующим образом (рис. 3.4):
а) образование зародышей кристаллов на границе металл-окисел;
б) образование окисной плёнки на границе газ-металл в результате химической реакции на поверхности;
в) диффузия ионов металла и кислорода через окисную плёнку;
г) образование промежуточных слоёв в процессе роста окисной плёнки из-за неравномерной диффузии кислорода и ионов металла через неё;
д) изменение состава металла в поверхностных слоях вследствие избирательного окисления и диффузии в слоях окисной плёнки, причём поверхностный слой металла обедняется одними легирующими элементами и обогащается другими.
Металлы при высоких температурах могут окислятся кислородом, парами воды, оксидом углерода (CO2), оксидом серы (SO2) и др.
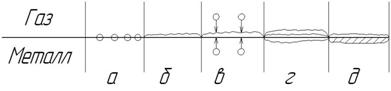
Рисунок 3.4 – Схема развития процесса окисления металлических поверхностей
Помимо окисления при температуре выше 700°С кислород, пары воды, оксид углерода и другие кислородосодержащие вещества могут обезуглероживать сталь и чугун, ухудшая их механические свойства.
Окисление углерода происходит на поверхности стали: из прилегающего слоя он диффундирует на поверхность стали и окисляется. Снижение концентрации углерода в поверхностном слое стали приводит к изменению структуры сплава и ухудшает механические свойства, особенно предел усталости и предел прочности при растяжении.
При определённых условиях водяной пар обладает более сильным окислительным действием, чем воздух или двуокись углерода.
Газовая коррозия в перегретом паре идёт значительно быстрее, чем коррозия в воздушной среде при таких же температурах. Железо и низколегированные стали в перегретом паре при 500°С окисляются в два раза сильнее, чем в нагретом воздухе.
2 Коррозия в атмосфере азота
При нагревании в воздушной атмосфере большинство металлов и сплавов сильно окисляются, тогда как взаимодействие их с азотом протекает слабо. Исключение составляют сплавы, содержащие нитридообразующие элементы: хром, алюминий, титан, бериллий и др. Известно, что низколегированные хромом и алюминиевые стали при температуре 500°С образуют нитриды, обладающие высокой твёрдостью. Процесс образования нитридов на металлической поверхности называется азотированием и широко применяется в практике машиностроения.
Установлено, что добавление молибдена, ванадия и титана также благоприятно влияет на азотирование, а введение никеля затрудняют его.
При взаимодействии с азотом на поверхности металлов и сплавов протекает активная адсорбция; при этом скорость диффузии азота тем выше, чем больше сродство входящих в состав сплава элементов с азотом. Наибольшим сродством к азоту обладают титан и алюминий, значительно меньшим – хром, марганец, молибден, железо и кобальт.
Самым эффективным методом борьбы с газовой коррозией в атмосфере, содержащей азот, является повышение содержания никеля в сплаве. В последнее время в качестве защитных сред при термической обработке никелевых термоустойчивых сплавов используют азот или смесь водорода с азотом.
3 Коррозия в атмосфере, содержащей водород
Водород – одна из наиболее важных составных частей промышленных газов: водяного, светильного, генераторного. При его сжигании образуется водяной пар. Он легко диффундирует в металлы, изменяет их свойства и способствует протеканию некоторых реакций на поверхности и в толще металла.
Диффундирующий в металл водород взаимодействует с окислами, углеродом (или, точнее, с цементитом), серой, фосфором и рядом других элементов, образуя водяные пары, метан, сероводород и т. д. Эти продукты, например водяной пар или метан, приводят к нарушению структуры, понижают прочность металла, придают ему хрупкость и способствуют его разрушению. Такие процессы могут протекать в установках для синтеза аммиака, гидрирования углей при производстве бензина и в ряде других случаев, когда водород применяется при повышенной температуре и давлении. Наклёп или укрупнение зерен металла способствует повышению его хрупкости и преждевременному разрушению. Действие водорода сопровождается также обезуглероживанием металла. Влияние водорода усиливается при температуре выше 350°С и тогда мало зависит от содержания углерода в сплаве.
Вначале водород адсорбируется на металлической поверхности в молекулярном состоянии, а затем вследствие каталитических реакций диссоциирует на атомы. При температурах до 300°С в молекулярном состоянии водород практически не проникает в железо или сталь, но в атомарном состоянии он проникает в сталь даже при низких температурах, что наблюдается при её травлении в серной или соляной кислоте.
Количество водорода, диффундирующее в сталь, зависит от температуры травильных растворов. При этом возможно насыщение стали водородом. Установлено, что введённые в определённых количествах по отношению к углероду легирующие элементы (хром, ванадий, титан и др.), обеспечивающие образование карбидов, устраняют вредное влияние водорода.
Легированные стали в среде водорода ведут себя по-разному в зависимости от состава сплава: в одних из них воздействие водорода вызывает внутрикристаллический характер разрушения, у других – разрушения по границам зёрен. Отпуск образцов в вакууме в первом случае полностью восстанавливает их механические свойства, а во втором случае – нет.
У медных образцов под воздействием водорода снижаются механические свойства и этот процесс необратим. Медь следует отнести к неводородостойким металлам.
В табл. 3.1 приведены металлы и сплавы, стойкие к различным видам газовой коррозии.
Таблица 3.1 – Металлы и сплавы, стойкие к газовой коррозии
Вид коррозии | Металлы, сплавы |
Окисление | Cr, Ni, стали, содержащие Ti и Ni |
Наводораживание | Стали легированные Cr, V, Ti |
Карбонильная коррозия | Высоколегированные стали Cr, CrNi, бронзы |
Сернистая коррозия | Хромистые стали, алюминий |
Коррозия хлором и хлористым водородом | Никель и его сплавы, нержавеющие стали |
3.4 Методы защиты от газовой коррозии
1) Легирование.
Для защиты от газовой коррозии используют главным образом термостойкие сплавы. Чтобы уменьшить скорость окисления железа при 900°С в два раза, достаточно его легировать 3,5% А1, а в четыре раза – примерно 5,5% А1.
2) Другой метод борьбы с газовой коррозией состоит в использовании защитной атмосферы. Газовая среда не должна содержать окислителей в контакте со сталью и восстановителей в контакте с медью. В качестве защитной атмосферы при термообработке и сварке применяют инертные газы азот и аргон. Разогрев стали осуществляют в атмосфере, содержащей азот, водород и окись углерода. Сварка алюминиево-магниевых и титановых деталей должна производиться в атмосфере аргона.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 |


