Используются достаточно много известных элементарных процессов в газах, которые в определенном наборе и последовательности реализуются в той или иной технологии.
1.3.2 Процессы технических газов
Технологии применения газов связаны с изменением параметров их состояния (давления, температуры), перемещением газов, а также с разнообразными физическими и химическими процессами.
Технологии использования сжатых газов основываются на осуществлении физических и химических процессов с целью получения полезного продукта. Полезным продуктом может быть вещество (твердое, жидкое, газообразное), теплота (или холод).
Основные используемые физические процессы газов:
- сжатие (расширение);
- диффузия (разделение);
- фильтрация;
- осушка (увлажнение);
- сепарация;
- сжижение (газификация);
- растворение в жидких и твердых телах (дегазация);
- кристаллизация;
- ионизация;
- газовые разряды и др.
К химическим процессам относятся:
- химические реакции получения соединений;
- полимеризация;
- окисление (в т. ч. горение);
- газовая коррозия.
Процессы в газах бывают непрерывные и прерывные. В непрерывных процессах производится непрерывная подача компонентов и отвод продуктов. Характерным примером может
быть крупнотоннажные производства минеральных удобрений. В прерывных процессах загрузка и выгрузка веществ (для газов – закачка и отсос) производятся периодически. Это, например, производства с применением автоклавов.
Во всех этих случаях требуется транспортировка, перемещение требуемых масс газов. Для реализации же физических процессов и химических реакций необходимо создавать требуемые параметры газов, а именно: давление (от вакуума до очень высоких давлений) и температуры (отводом или подводом тепла).
Сжатие и перемещение газов – компримирование – осуществляется компрессорными машинами различного типа. Можно утверждать, что основа производственных процессов использующих газы – это компрессорные технологии. Конечно, кроме компрессорных машин применяются и другие газовые машины для преобразования энергии газов: газовые турбины, детандеры, а также устройства струйной техники: эжекторы, инжекторы и множество других аппаратов.
1.3.3 Общие сведения о технологиях использования газов
Прежде всего технологии с использованием газов необходимо разделить на два вида:
- технологии добычи (получения) газов;
- технологии использования газов.
Процессы получения газов бывают:
- добыча – извлечение газов из природных источников (природный газ, атмосфера);
- искусственное получение – синтез как результат химических реакций.
Технологии применения газов можно представить следующими основными группами:
- применение технических газов непосредственно потребителем (природный газ, кислород, азот, аргон, ацетилен
и др.) для технологических нужд заводов и других предприятий различных отраслей;
- использование газов как компонентов технологических процессов получения полезных продуктов (удобрений, пластмасс и т. п.).
Технологии добычи (получения) и использования технических газов требуют специальных технологических комплексов (завод, линия, цех, установка). Например, газоперерабатывающий завод, воздухоразделительная установка, цех производства аммиака и т. п.
В свою очередь, эти технологические комплексы оснащены самым разнообразным оборудованием необходимым для функционирования: компрессоры, сепараторы, реакторы, нагреватели, охладители, насосы, другие аппараты.
Процесс получения промежуточного или окончательного продукта производится по технологической цепочке от подвода компонентов сырья, энергетических ресурсов (пар, электроэнергия, вода) до отвода готового продукта. Комплекс оборудования для получения продукта называется технологической линией. Для получения сложных по технологии продуктов могут использоваться несколько линий (цехов), работающих в одном комплексе. Как правило, на таких линиях и заводах получают не один продукт, а несколько, с целью как можно более полного использования исходных компонентов и продуктов реакции.
Технологические процессы химических производств состоят из двух неразделимых составляющих: химическая технология и необходимое оборудование.
Химическая технология отвечает на вопросы:
─ какие нужны химические реагенты;
─ какие параметры реализации реакций;
─ какие массовые потоки компонентов;
─ какие необходимы катализаторы и ингибиторы и др.
К оборудованию предъявляются требования: какие необходимы машины, аппараты и другие технические устройства для реализации данной химической технологии. Отсюда следует и необходимость в раздельных службах на заводах – службы главного технолога и главного механика. Первая из них отвечает за соблюдением технологического регламента и выпуска качественной продукции, а вторая – за нормальное и надежное функционирование технологического оборудования.
1.3.4 Технологические схемы
Последовательное описание и графическое изображение процессов и соответствующих им машин и аппаратов называется технологической схемой производства. Схемы бывают двух типов: открытые и циклические (циркуляционные).
Схемы открытые применяются для производственных процессов, в которых происходит полное превращение вещества в полезный продукт за один проход через установку.
Циклическая схема предусматривает выделение продукта из реакционной смеси, которая затем многократно возвращается в технологический цикл вплоть до полного превращения в продукт.
Технологические схемы производств с использованием газов сложны и очень разнообразны. Не существует общих универсальных технологий, а значит, и схем. Можно выделить лишь основные составляющие, обязательные для всех технологических процессов с газами (рис. 1.2).
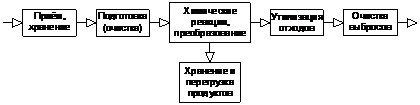
Рисунок 1.2 – Структурная схема газовых технологий
Схемы составляются на основе выбранного метода (или способа) производства продукта, в основе которого лежат физические превращения, химические реакции и механические процессы, протекающие при определенных условиях.
Графически схемы изображаются упрощенно, без излишней детализации, с использованием принятых условных обозначений, буквенных сокращений и надписей, цифровых позиций элементов.
После разработки схемы выполняется ее расчет – составление материального и энергетического балансов.
Материальный баланс означает, что масса веществ, поступивших на технологическую операцию – приход, равна массе всех веществ, получившихся в результате ее – расход:
![]() ,
,
где ![]() - суммарный расход сырья, кг;
- суммарный расход сырья, кг;
![]() - основной продукт, кг;
- основной продукт, кг;
![]() - побочный продукт (отходы), кг;
- побочный продукт (отходы), кг;
![]() - непроизводительные затраты сырья, кг.
- непроизводительные затраты сырья, кг.
Энергетический баланс для химикотехнологических процессов составляется в виде теплового баланса: приход тепла в данном цикле производства должен быть равен расходу его в этом же цикле (с учетом всех потерь).
Контрольные вопросы к теме 1
1 Перечислите основные применения газов в народном хозяйстве.
2 Приведите примеры применения газов в качестве энерго - и теплоносителя.
3 Приведите примеры применения газов в технологии машиностроения.
4 Изложите научные гипотезы о возникновении атмосферы и природных газов.
5 Основные, практически важные группы газов.
6 Перечислите основные, используемые на практике, процессы в газах. На какие группы делятся процессы?
7 Что такое непрерывные и прерывные технологические процессы с использованием газов? Приведите примеры.
8 Назовите виды технологий с использованием газов.
9 Назовите способы получения технических газов.
10 Какие две основные группы технологических процессов применения газов?
11 Что такое технологическая линия и ее компоненты?
12 Какой основной принцип построения технологических схем химических производств?
Список литературы
1. Общая химическая технология. Т.2. Важнейшие химические производства/ под редакцией . М.: Высшая школа,1984.-263с.
2. Основы процессов химической технологии. Л.:Химия,1967.-382с.
Тема 2 НЕКОТОРЫЕ СВЕДЕНИЯ ИЗ ТЕОРИИ ГАЗОВ
В данной главе приводятся сведения из термодинамики газов наиболее важные для расчетов технологических процессов с применением газов, рассматриваемых при изучении настоящего курса.
2.1 Свойства газов и газовых смесей
Газы. Это названия придумано голландским ученым Гельмонтом.
Газ – это такое агрегатное состояние вещества, в котором его частицы не связаны или слабо связаны между собой силами взаимодействия и движутся свободно, заполняя весь предоставленный им объем, и принимают его форму.
В отличие от жидких и твердых тел объем газов сильно зависит от давления и температуры.
Любое вещество можно перевести в газообразное состояние подбором надлежащей температуры и давления. На рис. 2.1 область газообразного состояния ограничена кривыми:
I – сублимация (отвердение); II – парообразование.
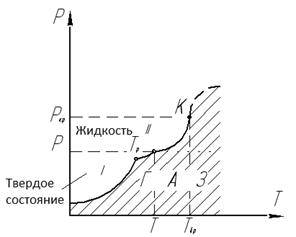
Рисунок 2.1 – Диаграмма фазовых переходов газов
При любом р<ркр существует температура Т, выше которой вещество становится газообразным. Точка Тр – тройная точка. На кривой I ниже точки Тр газ находится в равновесии с твердой фазой вещества (для воды – лед), а на кривой II (между точками Тр и К) – в равновесии с жидкой фазой (вода – пар). Газ в этих состояниях называется паром.
Пар – это название газообразного вещества в условиях, когда газовая фаза может находиться в равновесии с жидкой или твердой фазой того же вещества. Однако путем изменения температуры это равновесие может быть нарушено и тогда понятие пар теряет прежний смысл. Поэтому критерием в таких случаях служит критическая температура, т. е температура, выше которой вещество может находиться только в газообразном состоянии и никаким сжатием (без понижения температуры) сконденсировать его невозможно. Таким образом, газообразное вещество называют паром, если его температура ниже критической, и газом, если его температура выше критической.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 |


