Следует отметить, что газовые законы применимы только к парам, не находящимся в состоянии насыщения. Для насыщенных паров справедливы лишь закон Авогадро и закон Дальтона, которые не связаны с изменением параметров состояния.
При Т<Ткр газ можно сконденсировать, то есть перевести газ в жидкое состояние (или твердое). Например, вода замерзает при 0оС, а до этого (+5, +3, +1, +0,5оС) не замерзает. Также происходит и сжижение газов. Например, для О2 температура сжижения равна t=-182,98оС, а его отвердение происходит
при –218,7оС.
При Т>Ткр граница газообразной области условна, так как при этих температурах фазовые превращения не происходят.
2.1.1 Приведение к нормальным условиям
На практике для выполнения расчетов объемов и массовых потоков газов в различных устройствах и технологических линиях широко используют приведение объемов к нормальным условиям. Нормальными условиями для газов принято считать:
- температуру 0оС (273К);
- давление 760 мм рт. ст. или 101,325 кПа.
Такое приведение удобно и необходимо для сравнительных расчетов объемов газов при изменении параметров их состояния (давления, температуры). В отличие от жидкостей объем газа сильно изменяется при изменении параметров состояния.
Если состояние газа характеризуется параметрами p, V, T, то для приведения объема к нормальным условиям pн, Тн используется формула, получаемая из условия равенства массы (или массового расхода) m=mн
![]() ,
,
где Vн – объем, приведенный к нормальным условиям;
Тн, рн – нормальные параметры газа;
V – объем, измеренный при действительных параметрах
р и Т.
Пример. Воздушный компрессор сжимает воздух и транспортирует его к потребителю. Параметры атмосферы: tн=20оС, ра=1кгс/см2=0,0981 МПа; параметры у потребителя: tк=40оС, рк=8кгс/см2=0,7848 МПа. Расходомер на всасывании показывает производительность компрессора 100 м3/мин, а у потребителя – 10 м3/мин. Требуется определить величину утечек воздуха в пневмосети между компрессором и потребителем. Прямое сравнение производительностей 100 и 10 м3/мин не корректно, так как параметры воздуха существенно различны.
Выполним приведение производительностей к нормальным условиям на всасывании
![]()
и у потребителя
![]()
Величина утечки теперь может быть найдена как разность
Vут=Vн’-Vн”=90,2 – 67,5=22,7 нм3/мин.
Иногда удобно приводить производительность к условиям на всасывании или на нагнетании.
Чаще всего потери газа выражают не в объемных количествах, а в единицах массового расхода. Для нашего примера, с учетом зависимостей  и
и 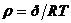 , получим массовый расход на всасывании:
, получим массовый расход на всасывании:
![]()
и у потребителя
![]()
Таким образом, утечка газа составляет
![]()
или 25% от расхода воздуха на всасывании. Заметим, что такая величина потерь воздуха в сети является недопустимой.
2.1.2 Концентрация газов
Если мы имеем смесь газов, то количество каждого из составляющих газов характеризуется его концентрацией. Концентрация выражается несколькими способами:
- весовым (Св)%; Св =Мi/Σ Мi= Мi/M;
- объемным (Со)%; Co= Vi/V;
- массой газа в единице объема (Св. о) г/м3.
Применяется также концентрация в частях по объему 1:V’, где V’ – объем смеси, в котором содержится 1 объем данного газа (например, концентрация углекислоты 1:2000).
Формулы для пересчета концентраций:
где μ – молекулярный вес газа;
р – давление газа, мм рт. ст.;
ро – нормальное давление газа (760 мм рт. ст.);
Vt – объем газа при температуре t.
В технике наиболее часто употребляется понятие объемной концентрации. Состав газовой смеси обычно задается объемными долями
![]() .
.
2.1.3 Масса и объем газа
Масса газа, заключенного в заданном объеме, равна m=ρV, где 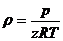 ;
;
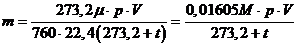 .
.
Объем, занимаемый данной массой газа при давлении р и температуре t равен
![]() ,
,
где μ – молекулярная масса газа;
р – давление газа, мм рт. ст.;
t – температура газа, оС;
G – масса газа, г;
V – объем, занимаемый газом, дм3.
На практике иногда пользуются понятием относительной массы.
Относительная масса газа d по отношению к другому газу при одинаковых давлениях и температурах равны ![]() .
.
Относительная масса газа по отношению к воздуху d=μ/29, по отношению к водороду d=μ/2 и т. д.
В задачах, связанных с изменением состояния в технологической линии, всегда используют массу, так как она неизменна (если не учитывать отборов и утечек). Например, если в технологической линии производится нагрев, охлаждение, дросселирование или газ совершает работу, конденсации, сжимания, закачка в емкость параметры газа рассчитываются из условия M = const (или m = const) в каждом состоянии или сечении. В разветвленных схемах выполняют расчет массовых потоков – основа химической технологии.
2.2 Идеальные газы
Понятие «идеальный газ» широко применяется в теории и расчетах состояния и движения газов. Для идеального газа постулируется ряд положений, существенно упрощающих теоретические выкладки. При этом получаемые результаты для определенного класса задач и условий достаточно близки к реальным данным. Важнейшими из таких положений являются изэнтропность (в приложении к механике газов это означает отсутствие трения газа о твердые границы, а также внутреннего трения между струйками и частицами газа) и совершенство газа, то есть подчинение свойств газа уравнению состояния идеальных газов в форме уравнения Клайперона – Менделеева
![]() ,
,
где р, V, T – давление, занимаемый объем и температура газа;
M и μ – масса и молекулярная масса газа;
R – универсальная газовая постоянная.
Чаще это уравнение применяется в виде для 1 кг газа:
рυ=RT,
где υ – относительный объем, м3/кг.
С учетом соотношения υ=1/ρ это уравнение приобретает вид
р=ρRT.
Значения газовой постоянной и молекулярного веса для некоторых газов приведены в таблице2.1.
Таблица 2.1 – Некоторые свойства газов
Газ | R, Дж/(кг∙К) | μ |
Воздух Углекислый газ CO2 Кислород Азот Гелий Водород Метан | 287,10 188,92 259,83 296,77 2077,04 4124,21 518,3 | 29 44 32 28 4 2 16 |
Газовая постоянная R является основной характеристикой газа и крайне важна для практических расчетов. Физический смысл газовой постоянной – работа расширения одного моля идеального газа при повышении его температуры на 1оК при постоянном давлении. В данном примере (рис. 2.2) – работа перемещения поршня на величину Н при подогреве одного моля газа на 1оК:
![]() ,
,
где m – масса поршня.
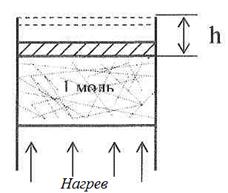
Рисунок 2.2 – К определению газовой постоянной
Величина μR называется универсальной газовой постоянной и для всех газов равна
![]() Дж/кмоль∙К.
Дж/кмоль∙К.
Зная молекулярный вес газа, можно легко определить его газовую постоянную.
Следствием совершенства идеального газа является его несжимаемость, то есть при постоянной температуре объем, занимаемый единицей массы газа, при р=υar остается неизменным. Этим свойством обладают жидкости, поэтому гидравлика, изучающая поведение и течение жидкостей, есть частный случай газодинамики, для которого допустимо считать газ несжимаемым. Строго говоря, при очень высоких давлениях объем жидкостей несколько уменьшается, но в большинстве случаев этим пренебрегают из-за малости.
В технических расчетах принимают газ идеальным при давлениях порядка нескольких атмосфер и практически важных температурах (-50 до 300оС).
2.3 Реальные газы
2.3.1 Определение параметров состояния реальных газов
Использование уравнения Клапейрона-Менделеева для идеального (совершенного газа) даёт хорошие результаты лишь для давлений, близких к атмосферному. С повышением давления газа погрешность от использования этого уравнения возрастает. В этом случае говорят о том, что газ становится несовершенным.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 |


