Метод вдувания в ванну применяется в электроплавильных печах для получения низкоуглеродистых сталей.
Обогащение кислородом дутья используется и при получении цветных металлов, и в ваграночной плавке.
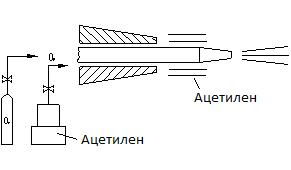
Рисунок 10.11 - Ацетиленовый резак
10.6.4 Кислородная резка
Кислородная резка является еще одним важным применением кислорода и называется еще и газорезкой. Это способ изменения формы и размеров металлических деталей путем сжигания металла в месте реза в струе кислорода. При этом температура воспламенения ниже температуры плавления.
В резаке (рис. 10.11) происходит подогрев кислорода посредством горящего ацетилена (или природного газа). Не режутся (или плохо режутся) стали с высоким содержанием углерода: чугун, высокохромистые, Al, Cu и их сплавы. В этом случае нужны флюсы.
Контрольные вопросы к теме 10
1 Назовите основные, практически важные свойства кислорода.
2 Как взаимодействует кислород с горючими веществами?
3 Назовите способы получения кислорода. В чем их суть?
4 Приведите принципиальную схему ректификационной установки получения кислорода. Назовите основные параметры.
5 Приведите схему холодильного цикла Капицы. Поясните его работу.
6 Изобразите рабочий процесс поршневого детандера. Каков его к. п.д.?
7 Приведите схему турбодетандера. Какие бывают типы турбодетандеров, их недостатки и преимущества?
8 Сравните поршневые и турбинные детандеры.
9 Назовите особенности конструкции кислородного турбокомпрессора.
10 Приведите схему и поясните устройство поршневого кислородного компрессора.
11 В чем хранят и как транспортируют кислород?
12 Расскажите основные сведения о применении кислорода в металлургии.
13 Объясните процесс и устройство для кислородной резки.
Список литературы
1. Глизманенко кислорода/ .– М.: Химия, 1972. – 752с.
2. Разумовский – элементарные формы и свойства/ . – М.: Химия, 1979.
Тема 11 ТЕХНОЛОГИЯ ПРОИЗВОДСТВА АММИАКА
11.1 Общие сведения об аммиаке
Аммиак, ![]() , - простейшее соединение азота с водородом. Бесцветный газ с очень резким характерным запахом (нашатырный спирт), легко растворяется в воде.
, - простейшее соединение азота с водородом. Бесцветный газ с очень резким характерным запахом (нашатырный спирт), легко растворяется в воде.
Уже в глубокой древности был известен хлористый аммоний (нашатырь – бессмертный огонь, персидское название). Получали в Ливии и Египте, сжигая в печах верблюжий навоз. Газ оседал в пористых полостях дымоходов, там его собирали и продавали в емкостях для лечебных и промышленных целей под названием «амоньянсос» - (греч. песчаная соль), затем его называли «аммониак», а в русской транскрипции – «аммиак».
В природе чистого аммиака не существует.
Аммиак образуется в организме человека как продукт белкового обмена и обезвреживается превращением его в мочевину и выводится из организма.
Аммиак играет важнейшую роль в жизни растений, потому и применяется как удобрение.
Вообще соединение азота играют неисключительную роль в деятельности человека (производство некоторых пластмасс, красителей, химических волокон, взрывчатых веществ и пороха, медикаментов и др.). Вследствие большой инертности азота долгое время не удавалось найти способы фиксации его в соединениях. Лишь в начале ХХ века были найдены три метода: электродуговой (соединение азота и кислорода при высокой температуре), цианамидный (реакция карбида кальция с азотом при 1000°С с образованием цианамида) и аммиачный метод – фиксация азота в соединении с водородом – получивший широкое промышленное применение в производстве минеральных удобрений.
11.2 Физические свойства аммиака
Аммиак при обычных условиях – это газ. Температура кипения 33,35°С, плавления 77,7°С. Удельный вес при нормальных условиях 0,771г/л или 0,771![]() , т. е. существенно легче воздуха. Параметры критического состояния:
, т. е. существенно легче воздуха. Параметры критического состояния: 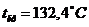 ;
; 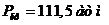 ,
, 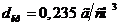 .
.
Твердый аммиак – кристаллы правильной формы.
Газообразный аммиак хорошо адсорбируется активированным углем.
С водой образуются непрочные соединения (аммиачная вода).
Сгорает в среде кислорода и воздуха с образованием азота и воды. Сухая смесь аммиака с воздухом способна взрываться, границы взрыва 16-20% аммиака при 18°С. С ростом температуры границы расширяются. Температура самовоспламенения 649°С.
Жидкий аммиак – хороший растворитель.
11.3 Получение аммиака
Как уже говорилось выше, в организме человека и животных аммиак образуется при нормальных условиях
(P=1 атм, t=36,6°С).
А вот промышленное получение аммиака далеко не такое простое. Аммиак получают методом термохимического синтеза (соединение азота и водорода), протекающего при очень высоких параметрах ![]() ,
, ![]() .
.
Процесс синтеза аммиака, с одной стороны, является примером наиболее совершенной химической технологии, а с другой стороны – наиболее сложный технически и аппаратурно.
Синтез аммиака предложен еще в начале прошлого века Габером. Суть его – в связывании азота и водорода реакцией, протекающей по схеме
![]()
Реакция обратима, протекает с уменьшением объема и выделением теплоты. Из этого следует, что более полно реакция проходит при высоких давлениях и низких температурах. При этом равновесный выход продукта (![]() ) невелик, поэтому процесс осуществляют по циклической схеме, которая предусматривает многократное возвращение в один и тот же аппарат реагирующих масс (
) невелик, поэтому процесс осуществляют по циклической схеме, которая предусматривает многократное возвращение в один и тот же аппарат реагирующих масс (![]() ) (рис. 11.1 а).
) (рис. 11.1 а).
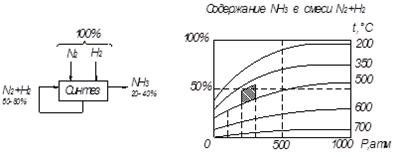
Рисунок 11.1 – Принципиальная схема циклической установки (а) и параметров синтеза аммиака (б)
На рис.11.1 б видно, что чем выше давление и ниже температура, тем больший выход продукта – аммиака.
Первый завод по производству синтетического аммиака построен в 1913 году.
Добиться 100% синтеза практически невозможно, т. к. нужны сверхмощные компрессоры, газоохладители и др. оборудование. В промышленных целях сегодня реакцию ведут при 400-500°С, давлениях 200-320 атм. При этом выход продукта составляет 20-40%. Уже много лет ведутся поиски путей – как снизить давление синтеза, т. к. очень сложное и дорогое оборудование, и прежде всего компрессорное оборудование.
Синтез аммиака идет только в присутствии катализатора. Катализатор должен быть активным в течении длительного периода времени, при температурах до 500°С, не быть чувствительным ко всяким примесям в азотоводородной смеси, иметь достаточную механическую прочность. Этим условиям удовлетворяет железный катализатор ![]() – магнетит с добавками.
– магнетит с добавками.
Часть азотоводородной смеси (60-80%), которая не прореагировала, т. е. не вступила в реакцию синтеза с получением аммиака, возвращается опять на вход в реактор, т. е. процесс носит циркуляционный характер.
На процесс образования аммиака существенное влияние оказывает время нахождения смеси газов в зоне контактирования в реакторе, чем медленнее процесс, тем больше выход аммиака.
Процесс получения аммиака состоит из 3 составляющих процессов: получение азота, получение водорода и собственно синтез аммиака.
Промышленная установка синтеза аммиака представлена на принципиальной схеме (рис.11.2).

Рисунок 11.2 – Технологическая схема синтеза аммиака:
1 – колонна синтеза; 2 – водяной конденсатор;
3 – сепаратор; 4 – циркуляционный компрессор;
5 – фильтр; 6 – конденсационная колона; 7 – испаритель;
8 – компрессор; 9 – сборник жидкого аммиака;
10 – компрессор свежего газа
В зависимости от принятого давления различают установки низкого (100 атм), среднего (200-550 атм) и высокого давления (600-1000 атм). На Украине ряд ПО «Азот» производят аммиак со средним давлением синтеза 320 атм.
Конечный продукт – аммиак – выделяют из его смеси с не прореагировавшим газом путем охлаждения до жидкого состояния в конденсационной колоне. Для этого устроен холодильный цикл, работающий на хладагенте – том же жидком аммиаке, не смешивающемся с продуктом.
Температура, до которой необходимо охладить газ для сжижения аммиака, зависит от давления в колоне:
- при 1000 атм – плюс 40°С;
- при 320 атм – минус 15°С;
- при 100 атм – минус 60°С.
Выбор рабочего давления – компромисс между производительностью по аммиаку и стоимостью оборудования и расхода энергии на сжатие газа (по компрессорному цеху).
11.4 Особенности конструкции компрессоров
11.4.1 Центробежные компрессорные установки
Для современных высокопроизводительных линий производства аммиака используются центробежные компрессорные установки.
На Украине производства аммиака функционируют на предприятиях «Азот» городов: Северодонецк, Черкассы, Днепродзержинск, «Стирол» г. Горловка и на Одесском припортовом заводе. Компрессорные установки поставки фирм Японии («Хитачи», «Мицубиси»), Франции («Крезолуар»), Казанского компрессорного завода. Эти установки однотипны как по параметрам технологического процесса, так и конструктивно. Последнее объясняется тем, что конструкции компрессоров базируются на лицензии фирмы «Дрессер» (США), купленной фирмами в 60-е годы ХХ в.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 |


