Легкое отравление – раздражение слизистой оболочки глаз и носа, чиханье, слезотечение, тошнота, головная боль, покраснение лица.
Тяжелое отравление – боль в глазах, удушье, кашель, головокружение, рвота, расстройство дыхания и сердечной деятельности. Может развиться отек легких. Нужно сделать искусственное дыхание и дать кислород.
Хронические отравления – воспаление слизистых оболочек верхних дыхательных путей, бронхов.
Допустима концентрация в воздухе промышленных помещений аммиака – ![]() .
.
Защита – спецодежда, очки, противогазы.
При отравлении аммиаком необходимо обильное питье, затем стакан растительного масла, молока или лимонного сока.
11.8 Применение аммиака
Выше мы рассмотрели крупнотонажное производство аммиака. Для чего же он нужен в таких количестьвах?
Прежде всего из аммиака производят азотную кислоту. Разбавленная азотная кислота (50-60%) используется для производства минеральных удобрений: аммиачной селитры, карбамида, а также кальцинированной соды, которая используется для производства едкого натра (каустик), мыла, стекла и в др. отраслях.
Концентрированная азотная кислота употребляется для производства взрывчатых веществ, красителей, нитролаков, некоторых пластмасс и др.
Рассмотрим производство карбамида – наиболее ценного азотного удобрения, легко усваиваемое растениями, содержащее 46% азота. Карбамид, кроме того, применяется и в промышленности для изготовления карбамидных смол, идущих на приготовление ценных пластмасс, древесностружечных плит, клеев, пропиток. Технологическая схема установки приведена на рис. 11.11. Сырьем для карбамида является аммиак и двуокись углерода, взаимодействующее по упрощенной реакции
![]() .
.
Процесс происходит медленно, не полностью. Время процесса уменьшается с повышением температуры. Для увеличения выхода продукта используют избыток аммиака и повышенное давление.
В промышленности синтез карбида ведут при
180-200 атм, 180-200°С. Выход карбамида составляет 60-70%.
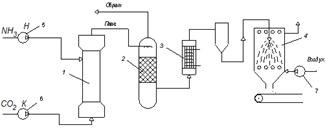
Рисунок 11.11 – Схема получения карбамида:
1 – колонна синтеза; 2 – дистилляционная колонна; 3 – выпарной аппарат; 4 – гранулятор; 5 – насос; – компрессор; 7 – воздуходувка
Контрольные вопросы к теме 11
1 Какие основные свойства аммиака и для чего он используется?
2 Какие особенности получения аммиака методом синтеза и его параметры?
3 Опишите суть циклического процесса получения аммиака в промышленных установках?
4 Какие газы и какие их превращения используются в установках синтеза аммиака?
5 Приведите принципиальную схему синтеза аммиака и перечислите основное оборудование?
6 Какие компрессоры применяются в установках синтеза? В чем их назначение?
7 Особенности конструкции компрессорной установки для сжатия азотоводородной смеси?
8 В чем основные конструктивные проблемы компрессоров азотоводородной смеси?
9 Как решается проблема концевых уплотнений компрессора синтез-газа?
10 Из-за чего возникает и как решается проблема разгрузки от осевых сил?
11 В чем специфика динамики ротора компрессоров высокого давления?
12 Особенности конструктивной схемы циркуляционных ступеней и компрессора для синтез-газа?
13 Как осуществляется хранение аммиака? Какое применяется оборудование (хранилища)?
14 Какие особенности транспортировки аммиака?
15 Опишите принципиальное устройство аммиакопривода.
16 Для получения каких продуктов применяется аммиак?
17 Изложите требования техники безопасности при работе с аммиаком.
Список литературы
1. и др. Основы химической технологии/ и др.– М., 1991.
2. Ведерников аммиака из природного газа/.– Киев: Техника, 1970.
Тема 12 ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ АЦЕТИЛЕНА
12.1 Основные свойства ацетилена
Молекулярный вес ацетилена 26,038; плотность (1 атм,
0 ºС) 1,17167 г/л = кг/м3, т. е. легче воздуха.
Газ при открытии назван «ацетиленом» в 1860 году французским физиком Бертло при обработке карбида калия К2С2 водой. Была установлена и формула газа С2Н2 – двуокись водорода. Ацетилен может быть в трех агрегатных состояниях: газ, жидкость, твердый.
При температуре -80,55ºС и давлении 961,5 мм рт. ст. твердый ацетилен плавится, его плотность ρж =1,27 г/мл, а далее, охлаждаясь, становится твердым (при нормальном давлении и температуре 189К) плотностью ρтв=0,729 г/см3. Ацетилен сжижается при давлении 46 атм, уже при 0ºС.
Ацетилен хорошо растворим в воде и водных растворах различных солей и щелочей. Особенно хорошо растворим в ацетоне: 1 объем ацетона растворяет 20 объемов ацетилена.
Ацетилен имеет специфический запах, общеядовитого действия.
Ацетилен горюч и взрывоопасен в смеси с кислородом, температура пламени достигает 3200ºС – наивысшая из всех известных горючих веществ. Используется для резки металлов.
Взрыв ацетилена происходит при его местном нагреве до параметров:
Р | 1 атм | 2 атм |
tºС | 635 | 510-540 |
Смесь ацетилена с воздухом или кислородом, содержащая от 2,5% до 80% ацетилена, взрывается от искры.
Пламя ацетилена очень яркое. Это используют для освещения в маячных фонарях, буях и др. Но главным является то, что ацетилен – исходное сырье для ряда важных органических синтезов.
Жидкий ацетилен при обычных температурах и, следовательно, при давлении 30-50 атм очень взрывоопасен. А при температуре -80ºС и давлении близком к атмосферному
(1,3 атм) взрыв не вызывает даже накаленная до красна проволока (спираль). Но если давление в баллоне с ацетиленом повысить более чем 2,7атм возникает взрыв. Порог взрыва можно существенно понизить растворением в жидком ацетилене ацетона, углеводородов.
Твердый ацетилен не взрывоопасен. Взрыв его можно вызвать только детонацией, например ударом.
12.2 Методы получения ацетилена
12.2.1 Производство ацетилена из карбида кальция
Карбид кальция образуется при взаимодействии негашеной извисти с коксом в электропечах при температуре 1800-2000ºС.
При контакте карбида кальция с водой происходит экзотермическая реакция с образованием ацетилена и выделением тепла:
СаС2 + 2Н2О = Са(ОН)2 + С2Н2 + Q (тепло),
Са(ОН)2 – гидрооксид кальция – не опасные отходы.
В небольших количествах ацетилен получают из карбида кальция в специальных аппаратах – ацетиленовых генераторах (рис. 12.1) двумя способами: «карбид в воду» и «вода на карбид». Второй способ экономичнее, он применяется в промышленном производстве. Первый способ проще и хорош для небольших местных потребностей при ремонтных и других работах.
Регулирование количества выделяющегося ацетилена производится изменением продолжительности соприкосновения карбида с водой, поднимая или опуская корзину.
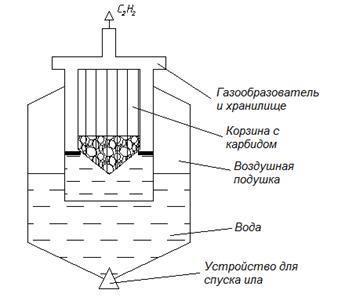
Рисунок 12.1 – Контактный ацетиленовый генератор
12.2.2 Производство ацетилена из углеводородов
Этот метод применяется для получения ацетилена в промышленных масштабах. Суть метода в термическом разложении углеводородов в специальных печах.
Реакция образования ацетилена из элементов
С (графит) + Н2 (газ) = С2Н2 (газ)
сильно эндотермична, т. е. требует большого количества тепла. Чтобы превратить углеводородное сырье, например метан в ацетилен, нужно нагревать его до 1000-1200ºС, причем очень быстро, а затем быстро охладить:
![]() 2СН4 = С2Н2 + 3Н2.
2СН4 = С2Н2 + 3Н2.
тепло
Быстро нужно делать потому, что эти соединения термодинамически не стабильны, распадаются быстро. На практике время реакции лежит в переделах 0,5–10 мс, а максимальная температура 1400ºС. А затем необходимо газ быстро охладить до 400ºС, чтобы предотвратить его обратное разложение – это т. н. «закалка».
Необходимые условия для такой реакции можно обеспечить в электрическом разряде, пропуская реагент через ядро разряда (электрокрекинг).
Промышленное распространение получил регенеративный (или окислительный) пиролиз. Суть его в быстром нагреве (за доли секунд) пиролизного газа при непосредственном контакте с сильно нагретой твердой поверхностью (1100-1300ºС). Затем газ необходимо быстро охладить до 400ºС. Для нагревания поверхности используют так же пиролизный газ или газ после выделения из него ацетилена в качестве топлива. Схема печи приведена на рис. 12.2.
Понижение давления уменьшает выход ацетилена и удорожает его стоимость. Выход ацетилена зависит от скорости охлаждения (до 400ºС - закалка), чем быстрее, тем лучше.
Давление в цикле поддерживается посредством поршневых или центробежных компрессоров специального исполнения. Такое требование обусловлено способностью ацетилена к возгоранию и взрыву. Это происходит при возникновении в какой-то части объема условий для разложения ацетилена, которое, начавшись в этой части, быстро распространяется на весь объем, всю систему.
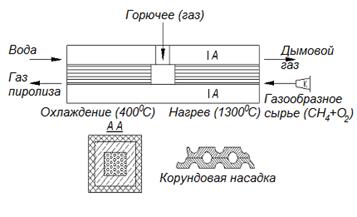
Рисунок 12.2 – Схема печи для экстракции ацетилена
12.3 Хранение и транспортировка ацетилена
Поскольку ацетилен взрыво - и пожароопасен в смеси с воздухом в широких пределах 2,5-80% (даже и до 100%), то обращение с ним должно быть очень осторожным.
Надо учитывать также, что возникновение внешнего очага пожара может инициировать взрыв ацетилена внутри установки. Поэтому в цеху необходимо исключить любой источник воспламенения, хорошо вентилировать помещение, исключить даже малейшее попадание воздуха в любую часть оборудования, а также утечки ацетилена изнутри.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 |


