2. Трофимова физики/ –М.: Высш. школа, 1985. – 432с.
3. Варгафтик по теплотехническим свойствам газов и жидкостей/ –М.: Наука,1972. – 720с.
4. Игнатенко методов определения термодинамических свойств многокомпонентных газовых смесей/ , // Компрессорное и энергетическое машиностроение.- 2006.- №3(5). С.82 –87.
5. Кучеренко газов/ - К.: Вища школа, 1981.- 96с.
6. Вуналович свойства воды и водяного пара/ - М.: Машгиз, 1985.-91с.
Тема 3 НЕКОТОРЫЕ ТЕХНИЧЕСКИ ВАЖНЫЕ СВОЙСТВА ГАЗОВ
3.1 Растворимость газов в жидкостях. Дегазация
Вода и другие жидкости, соприкасающиеся с каким-либо газом и смесью газов, содержат в растворённом виде некоторое количество этих газов, зависящее от рода газа, его парциального давления над поверхностью жидкости, температуры воды. Количество газа Gг, мг/л, растворённого в единице объёма жидкости, прямо пропорционально парциальному давлению газа:
![]() , мг/л,
, мг/л,
где ![]() - парциальное давление газа, кг/Па;
- парциальное давление газа, кг/Па;
![]() - коэффициент пропорциональности, мг/л∙Па.
- коэффициент пропорциональности, мг/л∙Па.
Парциальное давление растворённого газа рг, Па, равно разности полного давления над поверхностью жидкости и суммы парциальных давлений прочих растворённых газов и пара жидкости:
![]() .
.
Отсюда следует, что если при заданных условиях (p, t) парциальное давление пара жидкости неизменно, то растворимость газа в жидкости повышается с повышением полного давления над поверхностью жидкости. В качестве примеров на рис. 3.1 приведены кривые растворимости в виде углекислого газа и кислорода.
Для удаления газов, растворенных в жидкостях, применяют, как правило, термическую деаэрацию, значительно реже – химическое связывание газов различными реагентами, (например, кислород связывают стальными стружками).
При нагреве жидкости до температуры кипения (насыщения) концентрация газа стремится к нулю. Выделившийся из жидкости газ отводят вовне.
Аппараты, используемые для этих целей, называются деаэраторами или дегазаторами.
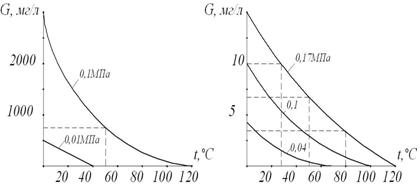
а б
Рисунок 3.1 – Растворимость в виде углекислого газа (а) и кислорода (б)
3.2 Поглощение газов и паров твёрдыми телами
Опыт показывает, что различные твёрдые тела поглощают значительное количество газа. Газ может проникать вглубь твёрдого тела подобно тому, как это происходит при растворении газа в жидкости. Такое глубинное удержание газа твёрдыми телами принято называть абсорбцией. Кроме того, газ может также удерживаться поверхностью твёрдого тела с образованием плёнки толщиной в один или несколько молекулярных слоёв. Тогда говорят о явлении адсорбции. Абсорбция и адсорбция газов или паров редко встречаются в чистом виде. В большинстве случаев поглощённый газ частично находится на поверхности, а частично диффундирует в толщу твёрдого тела. Поэтому, когда трудно установить характер механизма поглощения газа, употребляют более общий термин «сорбция», объединяющий оба понятия – адсорбцию и абсорбцию.
Твёрдые тела, поглощающие газы, иногда называют сорбентами, или, если это явление разделимо, адсорбентами (абсорбентами). Поглощаемый же газ или пар называется сорбатом (адсорбатом или абсорбатом).
Обратный процесс удаления газа из сорбента (например, путём нагревания в вакууме) называется десорбцией.
Механизм поглощения газа при адсорбции может быть разным, так как в различных системах твёрдое тело – газ адсорбция обусловлена различными силами. Различают физическую и химическую адсорбцию.
При физической адсорбции молекулы адсорбента сохраняют свою индивидуальность, а адсорбционные силы имеют ту же природу, что и межмолекулярное взаимодействие в газах, жидкостях и твёрдых телах. Адсорбированные молекулы газа принимают участие в тепловом (колебательном) движении атомов твёрдого тела и, следовательно, при достаточно большой амплитуде этого движения могут испаряться (десорбироваться) из поверхности твёрдого тела.
Какое количество газа может адсорбироваться на поверхности твёрдого тела? Опыт показывает, что для данного твёрдого тела адсорбция зависит от природы газа и его давления. Количественную связь массы μ адсорбированного газа от давления р (при постоянной температуре) получают из экспериментальных кривых – изотерм адсорбции. На рис. 3.2 показан типичный ход кривых адсорбции для двух температур: Т1 < Т2. На этих изотермах можно выделить три характерные области: область низких давлений - участок 0 а, область средних давлений - ab и область высоких давлений - bc. На отрезках кривых 0 а величина адсорбции пропорциональна давлению газа, а затем наступает состояние насыщения (участки ab). В этих условиях поверхность твёрдого тела покрывается мономолекулярным слоем, т. е. слоем, толщина которого не превышает размеров одной молекулы (атома) газа. При дальнейшем увеличении давления происходит наращивание первого слоя и адсорбированный газ может образовать плёнку, состоящую из нескольких молекулярных слоёв.
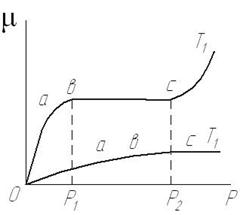
Рисунок 3.2 – Зависимость массы адсорбции от давления газа
Состояния, отмеченные на изотермах адсорбции, из-за теплового движения атомов твёрдого тела являются состояниями динамического равновесия, когда некоторые адсорбированные молекулы постоянно покидают поверхность тела (десорбируются), а другие приходят из объёма (адсорбируются). Как видно из рис. 3.2, для повышения адсорбционной способности твёрдого тела понижают его температуру, и, наоборот, если необходимо удалить адсорбированные газы (обезгазить данную поверхность), нагревают твёрдое тело. Это широко используют для получения и поддержания низких давлений.
Иногда взаимодействие между газом и твёрдым телом напоминает химическую реакцию. Тогда говорят о химической адсорбции. При этом действуют силы химической связи, которые отличаются по своей природе от сил межмолекулярного взаимодействия и часто их даже превосходят. Так, например, на плёнку кислорода, образовавшуюся на вольфрамовой нити накаливания, водород практически не оказывает никакого воздействия даже при температуре 1500°С. Это свидетельствует о том, что удерживаемый вольфрамовой нитью кислород действует совершенно не так, как в газообразном состоянии.
Отличие между химической и физической адсорбциями состоит также в том, что в то время, как эффективность физической адсорбции с понижением температуры возрастает, химическая адсорбция при недостаточно высоких температурах совсем не происходит и, наоборот, может очень быстро усиливаться с температурой. При нагревании тела газ, связанный механизмом химической адсорбции, из него либо совсем не удаляется, либо удаляется очень плохо. При этом химический состав десорбированного газа отличается от адсорбированного.
Явление химической адсорбции носит также название «хемосорбции», так как количество тепла, выделяющееся при этом процессе по порядку величины соответствует тепловым эффектам химической реакции.
При объёмном поглощении газов твёрдыми телами (абсорбции) количество поглощенного газа возрастает пропорционально объёму тела и зависит от его природы.
Абсорбция газа твёрдым телом, исключая хемосорбцию и физическую адсорбцию, идёт в направлении образования твёрдого раствора, т. е. проникновения молекул газа внутрь кристаллической решетки твёрдого тела.
Типичными абсорбентами газов являются металлы. В зависимости от условий они могут поглощать объёмы газов, в сотни раз превышающие их собственный объём. Так, например, титан поглощает до 1800 объёмов водорода при нормальных условиях (20° С и 760 мм рт. ст.), цирконий – 1500, палладий – 900, тантал – 750. Вследствие того что абсорбированные газы проникают внутрь металла, через некоторый промежуток времени газ начнёт проходить сквозь металл. Процесс диффузии газов через металлы зависит от природы металла и газа, толщины стенок и связан с давлением газа и температурой металла следующим уравнением:
![]() ,
,
где W – количество диффундируемого газа (объёмные единицы за единицу времени); a и b – константы для данной пары металл – газ; d – толщина стенок; р – давление у поверхности металла, в которую входит газ; Т – абсолютная температура.
На рис. 3.3 приведены кривые, иллюстрирующие скорость диффузии для различных металлов и газов. Следует отметить, что скорость диффузии водорода через палладий по сравнению с другими металлами наибольшая.
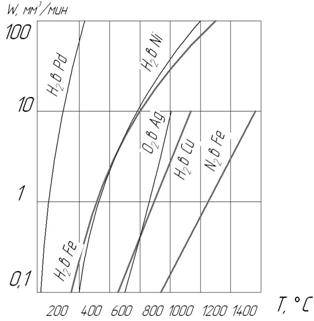
Рисунок 3.3 – Зависимость скорости диффузии
для различных металлов и газов
3.3 Газовая коррозия
3.3.1 Общие сведения
В технике аппаратура, изготовленная из металлов и сплавов, часто подвергается воздействию температуры и газов: кислорода воздуха, водорода, соединений, содержащих серу и углерод и др. Почти все металлы, приходя в соприкосновение с окружающей их газообразной или жидкой средой, более или менее быстро подвергаются разрушению с поверхности.
Всякий процесс химического разрушения металлов под воздействием окружающей среды называют коррозией.
Продукты коррозии могут образовывать на поверхности металла плотный защитный слой, затормаживающий её дальнейшее развитие, или же пористый слой, не защищающий поверхность от дальнейшего разрушающего воздействия среды. В этом случае процесс коррозии продолжается до полного разрушения материала или период времени, пока будет действовать агрессивная среда. При соприкосновении металлов с газами на поверхности металла образуются соответствующие соединения: оксиды, сернистые соединения, основные соли угольной кислоты, которые нередко покрывают поверхность плотным слоем, защищающим металл от дальнейшего воздействия тех же газов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 |


