Реальным газом называется газ, между молекулами которого имеется силовое взаимодействие. Основным отличием реального газа от идеального является его сжимаемость, т. е. зависимость объёма, занимаемого единицей массы газа, от изменения давления газа (температура полагается неизменной). Поскольку отношение массы газа к его объёму является плотностью газа 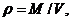 то из предыдущего положения следует, что для реальных газов имеет место зависимость плотности от давления.
то из предыдущего положения следует, что для реальных газов имеет место зависимость плотности от давления.
При увеличении давления в реальном газе возрастают силы межмолекулярного взаимодействия, становится заметным влияние собственного объёма молекул. Для расчётов параметров состояния таких газов используется уравнение Ван-дер-Ваальса
![]()
где ![]() поправка на взаимное притяжение молекул газа (внутреннее давление);
поправка на взаимное притяжение молекул газа (внутреннее давление); ![]() поправка на собственный объём молекул.
поправка на собственный объём молекул.
Вычисление параметров состояния газа по приведённому уравнению представляет определённые трудности из-за необходимости использования ряда коэффициентов. На практике проще, хотя и менее строго, плотность газа определяется через коэффициент сжимаемости, вводимый в уравнение состояния совершенного газа
![]()
откуда
![]()
Величина ![]() представляется в виде обобщенной функции приведенных параметров
представляется в виде обобщенной функции приведенных параметров
![]()
Здесь ![]() приведенная температура, т. е. отношение абсолютной температуры к критической абсолютной температуре
приведенная температура, т. е. отношение абсолютной температуры к критической абсолютной температуре
![]()
Аналогично приведенное давление есть отношение
![]()
Критическими называются параметры газа на линии перехода газа в жидкое состояние и наоборот. Эти параметры определяются экспериментально и находятся по справочной литературе. Они могут быть рассчитаны из уравнения
Ван-дер-Ваальса
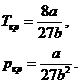
Для приближённых расчётов можно критическую температуру определять по формуле
![]()
где ![]() абсолютная температура кипения при нормальном давлении.
абсолютная температура кипения при нормальном давлении.
В критическом состоянии ![]() значение коэффициента сжимаемости для разных газов колеблется в пределах от
значение коэффициента сжимаемости для разных газов колеблется в пределах от![]() чаще всего он близок к
чаще всего он близок к ![]() Для его определения пользуются универсальной диаграммой (рис.2.3).
Для его определения пользуются универсальной диаграммой (рис.2.3).
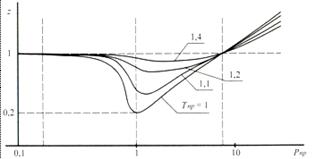
Рисунок 2.3 –Зависимость z от критических параметров газа
Отметим, что большинство технических газов могут приближённо считаться несжимаемыми лишь при малых абсолютных давлениях 
2.3.2 Термодинамические таблицы и диаграммы
На основе огромного фактического материала по экспериментальному определению свойств газов и смесей для практически важных технических газов были выполнены расчёты величин энтальпии и энтропии как функции состояния.
Энтальпия – термодинамическая функция, определяемая как сумма внутренней и объёмной энергий
![]()
или в дифференциалах ![]()
Энтальпия является потенциалом, т. е. её изменение зависит только от начального и конечного состояния и не зависит от пути.
Энтальпия характеризует состояние термодинамической системы. Изменение ее есть мера изменения работы в адиабатических процессах. Это изменение равно количеству теплоты, которое подводится или отводится от системы при ![]()
Энтальпия есть функция давления и температуры.
Энтропия является мерой необратимости рассеяния энергии в термодинамических процессах в системе. Энтропия также является потенциалом. Она не определима при нулевом давлении, поэтому в расчётах оперируют не её абсолютным значением, а изменением
![]()
Результаты расчётов собраны в справочные таблицы. Однако на практике более удобно и наглядно пользоваться составленными по этим справочным данным диаграммами состояния.
Такие диаграммы охватывают обычно и области жидкой фазы ниже пограничной кривой фазового перехода. По диаграммам легче определить изменение состояния газа при различных превращениях, а также теплоту и работу этих превращений. Диаграммы дают наглядность в движении термодинамических процессов, позволяют избежать ошибок и промахов в определении параметров процессов. Использование диаграмм даёт возможность проще и быстрее, чем при работе по формулам, определить необходимую величину. Кроме того, термодинамические расчёты по формулам не всегда возможны.
В практике используются несколько видов диаграмм в зависимости от задач. Состояние веществ определяют давление ![]() температура
температура ![]() и параметр влажности
и параметр влажности ![]() Зная эти параметры, легко определить другие: удельный объём, энтальпию
Зная эти параметры, легко определить другие: удельный объём, энтальпию ![]() энтропию
энтропию ![]() которые обычно отнесены к
которые обычно отнесены к ![]() массы газа.
массы газа.
Применяют следующие диаграммы: ![]() На каждой такой диаграмме остальные четыре параметра представлены линиями постоянных значений. Например, на диаграмме
На каждой такой диаграмме остальные четыре параметра представлены линиями постоянных значений. Например, на диаграмме ![]() нанесены линии: изохоры, изотермы, изобары.
нанесены линии: изохоры, изотермы, изобары.
При анализе и расчёте процессов сжатия и расширения газов наиболее часто применяются диаграммы ![]()
(рис. 2.4 и 2.5).
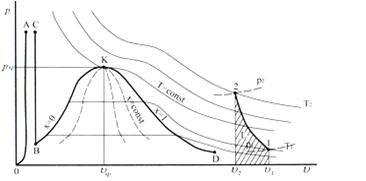
Рисунок 2.4 – Диаграмма ![]() (пример процесса сжатия):
(пример процесса сжатия):
ОА – объём твёрдой фазы в условиях плавления;
ВС – объём затвердевающей фазы (в равновесии с плавлением);
ВК – объём кипящей жидкости ![]() (в равновесии с паром);
(в равновесии с паром);
KD – объём пара ![]()
K – критическая точка ![]()
![]() линии постоянной влажности
линии постоянной влажности
Процесс сжатия показан линией 1-2. Отметим, что действительны лишь состояния 1 и 2, а остальные точки линии процесса условны.
В этой диаграмме удобно представляется внешняя работа сжатия ![]() равная
равная
![]()
которая показана заштрихованной площадью под линией сжатия.
Такая диаграмма удобна для расчётов компрессоров и детандеров объёмного типа.
На рис. 2.5 представлена диаграмма для водяного пара. На диаграмме в качестве примера показан процесс в паротурбинной установке: 0-1 – изобарное нагревание, теплота нагревания равна разности энтальпий (отрезок АВ); 1-2 – процесс дросселирования в вентиле при ![]() 2-3 – процесс расширения в турбине (отрезок ВС – работа расширения).
2-3 – процесс расширения в турбине (отрезок ВС – работа расширения).
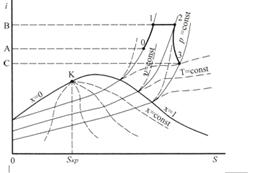
Рисунок 2.5 – Диаграмма ![]()
Эта диаграмма удобна для исследования процессов в паровых котлах, турбинах и нагревателях, а также в турбокомпрессорах.
Определение свойств реальных газов возможно также с применением таблиц [3] (для газов), [3] (для водяного пара) и др.
2.4 Смеси газов
Пусть мы имеем смесь нескольких газов, которые называются ![]() компонентами. Содержание каждого компонента в смеси характеризуется объемной долей
компонентами. Содержание каждого компонента в смеси характеризуется объемной долей ![]() или массовой долей
или массовой долей ![]() . Если при изменении состояния газовой смеси компоненты не подвергаются конденсации и не вступают в химическую реакцию друг с другом, то параметры смеси
. Если при изменении состояния газовой смеси компоненты не подвергаются конденсации и не вступают в химическую реакцию друг с другом, то параметры смеси ![]() связаны между собой уравнением состояния для идеального или реального газа. Чтобы воспользоваться этим уравнением, необходимо знать для смеси величину газовой постоянной
связаны между собой уравнением состояния для идеального или реального газа. Чтобы воспользоваться этим уравнением, необходимо знать для смеси величину газовой постоянной ![]() и коэффициента сжимаемости.
и коэффициента сжимаемости.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 |


