Календула - лекарственное растение. Из цветков календулы получают масляный экстракт, используемый в качестве пищевого красителя. Измельченные цветки календулы можно подвергнуть экстрагированию раствором этилового спирта. Таким образом можно получить отличное антисептическое и противовоспалительное средство.
Спиртовой раствор календулы можно упаривать, таким образом можно получить раствор различной концентрации и различной интенсивности окраски желтый раствор. Если растворитель полностью испарить получиться желеобразный оранжево-желтый пигмент, который можно использовать в пищевой промышленности для окраски кремов и карамелей.
Ход работы:
Взвешивают в стакане 20 г лепестков календулы и помещают его в конус из медной или латунной сетки или специальный нутч - фильтр (из прессованного стекла).
Собирают аппарат Сокслета (рис.1). Помещают анализируемое вещество в экстрактор. Присоединяют экстрактор к колбе и заливают в него этиловый спирт (или масло), пока он не начнет переливаться через сифонную трубку в колбу.
Добавляют еще треть взятого растворителя и колбу с экстрактором устанавливают в нагревательный аппарат (колбонагреватель). Затем подсоединяют шариковый холодильник. В собранном аппарате верхний край фильтра должен быть на 5 – 10мм выше сифонной трубки.
Нагревают аппарат так, чтобы растворитель стекал со скоростью не более 5 капель в 1 сек. Экстракцию продолжают до тех пор, пока растворитель в экстракторе не станет бесцветным. Затем установку отключают и охлаждают. Фильтр с цветками извлекают из экстрактора и помещают в сушильный шкаф и сушат 30 мин при t°105 -110°С. Затем охлаждаю в эксикаторе 30 мин и взвешивают.
Отгонка растворителя
После завершения экстрагирования установке дают остыть. Затем отсоединяют реакционную колбу, проводят следующий этап работы.
Собирают установку для отгонки растворителя (рис.7). Перед тем как собрать установку, реакционную колбу взвешивают. Затем проводят операцию отгонки растворителя. Для этого в реакционную колбу небольшими порциями переносят исследуемый раствор и нагревают, следя за температурой паров выходящих из реакционной колбы. Когда в реакционной колбе останется вязкая масса, отгонку прекращают. Установку отключают, дают остыть.
Остывшую установку разбирают и реакционную колбу взвешивают. Массу полученного вещества в % рассчитывают по формуле:
X = [(m-m1)/g]*100
где m-масса колбы до отгонки (г);
m1 - масса колбы после отгонки (г);
g - масса навески цветков календулы (г).

Рис.7 Установка для отгонки растворителя.
1 – реакционная колба, 2- термометр, 3- холодильник Либиха, 4 – аллонж, 5 - колба-приемник
Результат оценивается следующим образом:
- выход продукта 96- 99%- отлично выход продукта 93- 95%- хорошо выход продукта 92 и ниже - удовлетворительно, учитывая, что потери при этом составляют 7- 10%.
Обработка результатов
Выход продукта (Х) в процентах вычисляют по формуле
X = [(m-m1)/ m2]*100
где m - масса фильтра с цветками до экстракции (г);
m1 - масса фильтра пустого (г);
m2 - масса фильтра после экстракции (г).
За результат испытания принимают среднее арифметическое результатов двух параллельных определений.
2.4 Возгонка
Некоторые твердые вещества при нагревании способны испаряться до наступления температуры их плавления. Обратный переход паров в твердое состояние происходит сразу, минуя жидкую фазу. Такой процесс называется возгонкой или сублимацией.
Возгонка применяется для очистки веществ. Возгонка, даже однократная, как правило, приводит к получению вполне чистого продукта и заменяет несколько перекристаллизаций. Она может быть использована как для окончательной очистки продукта, так и для предварительного отделения летучего соединения от нелетучих примесей. От перекристаллизации возгонка отличается также более высоким выходом чистого продукта (98-99%).
С другой стороны, возгонка весьма длительный процесс, поэтому его обычно используют для очистки небольших количеств веществ. Область применения этого метода ограничена также тем, что способность многих твердых соединений сублимироваться очень мала. Поскольку скорость испарения пропорциональна общей площади поверхности испарения, подвергаемое возгонке вещество необходимо как можно тоньше измельчать. Не следует также допускать плавления вещества при возгонке, так как это ведет к падению скорости процесса вследствие резкого уменьшения поверхности вещества.
Применение вакуума, как и при перегонке, снижает температуру, при которой вещества начинают возгоняться. Под вакуумом удается сублимировать многие труднолетучие соединения.
При выборе приборов для возгонки следует отдавать предпочтение конструкциям, в которых расстояние между возгоняемым веществом и поверхностью конденсации минимально. С уменьшением этого расстояния возрастает скорость возгонки.
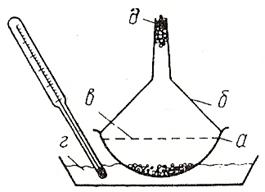 Рис. 8 Простейший прибор для возгонки: а-фарфоровая чашка с веществом; б-стеклянная воронка; в - кружок фильтровальной бумаги с отверстиями; г - песчаная баня; д - вата.
Рис. 8 Простейший прибор для возгонки: а-фарфоровая чашка с веществом; б-стеклянная воронка; в - кружок фильтровальной бумаги с отверстиями; г - песчаная баня; д - вата.
Для сублимации небольших количеств легковозгоняющихся веществ может быть использован простейший прибор, состоящий из фарфоровой чашки, часового стекла и обычной химической воронки. Фарфоровую чашку с возгоняемым веществом накрывают кружком фильтровальной бумаги с проколотыми в нем отверстиями.
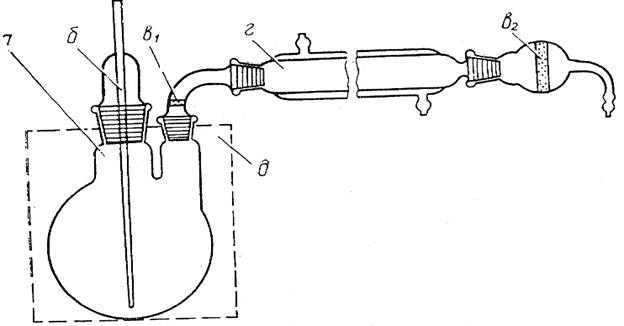
Рис. 9 Вакуум-сублиматор:
а – колба с возгоняемым веществом; б-капилляр для подачи воздуха или инертного газа; в1,в2- пористые стеклянные пластинки; г-холодильник, в котором собирается возгон; д – зона обогрева.
В вакуум-сублиматоре возгон собирается в горизонтально расположенном холодильнике с достаточно широкой внутренней трубкой. Во избежание преждевременной конденсации продукта колбу с возгоняемым веществом по горло погружают в нагретую до нужной температуры жидкостную баню. Небольшой ток воздуха или инертного газа, подаваемый в колбу через капилляр, способствует эффективному отводу паров от поверхности испарения, резко повышая производительность прибора.
Лабораторная работа 3
Тема. Очистка нафталина возгонкой.
Около 1г технического нафталина помещают в маленькую фарфоровую чашку и накрывают стеклянной воронкой. Отводную трубку воронки закрывают куском ваты. Между чашкой и воронкой помещают лист фильтровальной бумаги с небольшими отверстиями во многих местах для пропускания паров. Это делают для того, чтобы кристаллы вещества, образовавшиеся на холодной поверхности воронки, не падали опять на возгоняемое вещество. Воронку охлаждают, прикладывая к наружной поверхности смоченный в воде кусок ваты или ткани. Чашку слабо нагревают, не допуская плавления вещества. При этом нафталин возгоняется и оседает в виде игл на стенках воронки.
Таким способом можно очистить фталевый ангидрид, йод и ряд других веществ.
NB!!! Необходимо помнить, что даже небольшой перегрев может привести к термическому разложению очищаемого вещества.
III Качественный анализ органических веществ
Лабораторная работа 4.
Тема. Качественные реакции галогенпроизводных углеводородов, спиртов, фенолов, кислот, альдегидов.
4.1. Галогенпроизводные. Проба Бейльштейна на наличие галогенов в органических соединениях.
Метод основан на том, что галогены (за исключением фтора) при нагревании образуют с медью летучие соединения, которые окрашивают пламя горелки в зеленый цвет.
Опыт. Петлю из медной проволоки нагревают в пламени горелки до полного исчезновения зеленой окраски. После остывания проволоки берут в петлю небольшое количество исследуемого вещества (хлороформа) и снова нагревают в пламени. Голубовато-зеленая окраска пламени указывает на присутствие хлора, брома или йода.
4.2. Спирты.
1. Окисление хромовой смесью. Для того чтобы различить первичные и вторичные спирты, можно воспользоваться окислением хромовой смесью. Первичные спирты превращаются при этом в альдегиды, вторичные - в кетоны. Если полученный при этом дистиллят восстанавливает раствор Фелинга, то карбонильное соединение представляет собой альдегид и спирт был первичный, если же дистиллят не восстанавливает раствор Фелинга, то карбонильное соединение является кетоном и спирт был вторичным:
O
//
3RCH2ОH + K2Cr2О7 + 4H2SО4®3RC + К2SО4 + Cr2 (SО4)3+ 7Н2O
\
H
3RR’CHOH + K2Cr2О7 + 4H2SО4-+ 3R—CO—R’+ К2SО4 + Cr2 (SО4)3+ 7Н2О
Опыт. В течение 5 мин кипятят с обратным холодильником 1 мл спирта (пропилового и изопропилового) с 10 мл раствора Бекмана. Смесь Бекмана (хромовую смесь) готовят следующим образом: в 100 мл растворяют 20 г дихромата калия, добавляют 10 мл концентрированной серной кислоты.
Реакционную смесь перегоняют, собирая несколько миллилитров дистиллята в приемник с раствором 2,4-динитрофенилгидразина. Выпадение осадка указывает на то, что окисление прошло и образовалось карбонильное соединение. Другую часть дистиллята собирают в приёмник с раствором Фелинга. Выделение красного или желтого осадка закиси меди (Сu2О) при нагревании свидетельствует о том, что образовавшееся карбонильное соединение является альдегидом.
2. Образование глицерата меди. Эта реакция является качественной на многоатомные спирты.
Опыт. В пробирку наливают 1 мл 2н. раствора сульфата меди и 1 мл 2н. гидроксида натрия. К выпавшему осадку гидроксида меди (II) добавляют несколько капель глицерина. Почему происходит растворение осадка образовавшегося гидроксида меди (II)?

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



