4.3.Фенолы.
1. Реакция с FеСIз. Большинство фенолов дают интенсивную цветную реакцию с хлорным железом. Обычно возникает фиолетовая или синяя окраска, но для некоторых замещенных фенолов она может быть красной или зеленой:
Цветная реакция фенолов менее отчетлива в спирте, чем в воде, особенно чувствительна в хлороформе.
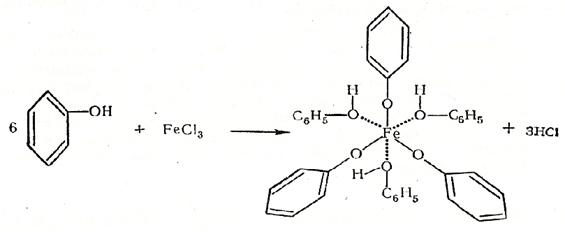
Опыт. а) В пробирку помещают 2-3 кристаллика фенола и растворяют в 2-3 мл воды, затем добавляют 1-2 капли 3%- ного раствора FеСlз. Появляется характерная фиолетовая окраска. Опыт повторяют с салициловой кислотой.
б) В трех пробирках готовят по 2-3 мл разбавленных растворов пирокатехина, резорцина, гидрохинона и добавляют по 1- 2 капли 3%-ного раствора FеСlз. Появляется зеленое, фиолетовое, желтое окрашивание соответственно.
Реакцию с гидрохиноном можно провести еще и так: приготовить в пробирке довольно концентрированный раствор гидрохинона в воде, нагреть его и к горячему раствору прибавить 2-3 капли 3% -ного раствора FеСlз. Смесь окрашивается при этом в красный цвет. Через некоторое время из охлажденного раствора выпадает хингидрон в виде длинных игл.
в) В две пробирки кладут по нескольку кристалликов в одну a-, в другую b-нафтола, приливают по 1 мл спирта и 1 мл воды. К полученным растворам добавляют по 2-3 капли 3%-ного раствора FеСlз. a-нафтол дает фиолетовое окрашивание, b-нафтол - зеленое.
2.Реакция с бромной водой. Фенолы со свободными о - и п-положениями обесцвечивают бромную воду и образуют при этом продукты замещения, которые обычно выпадают в осадок.
Опыт. Готовят по 1 мл водных растворов фенола, a - и b-нафтола. К каждому раствору прибавляют постепенно по 1 мл бромной воды. Наблюдают происходящие изменения.
3. Реакция с HNО2. Большинство фенолов не замещенных п-положении дают с азотистой кислотой нитрозофенолы, которые в присутствии концентрированной H2SО4 легко конденсируются с избытком фенола, образуя продукты конденсации, растворимые в гидроксиде натрия, с ярко-зеленой или синей окраской:
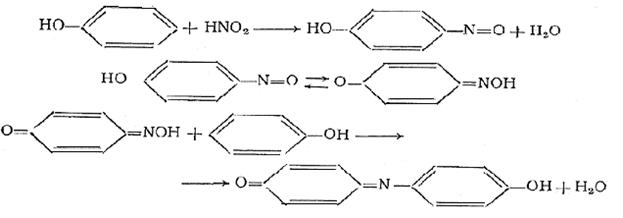
Опыт. К 0,5 мл концентрированной H2SO4 добавляют 2-3 капли 10%-нoгo раствора фенола и затем 1 каплю 10%-ного раствора NaNО2. При встряхивании смесь окрашивается в фиолетово-синий цвет. Интенсивно окрашенную жидкость осторожно выливают в 5 мл воды. Образуется розово-красный раствор. При добавлении к 1 мл этого раствора избытка 1 н. раствора NaOH розоватая окраска переходит в зеленую и синеватую. При подкислении жидкость вновь приобретает розовую окраску.
4. Реакция со щелочью (отличие фенолов от спиртов). Фенолы растворимы в разбавленном растворе гидроксида натрия вследствие образования растворимых в воде фенолятов. Спирты со щелочью не реагируют, и поэтому не растворимые в воде спирты не растворяются и в щелочи.
Опыт. В пробирку помещают несколько кристалликов фенола и приливают постепенно при встряхивании 5%-ный раствор NaOH до полного исчезновения кристаллов. Одновременно в другую пробирку наливают 0,2-0,3 мл бутилового или амилового спирта и добавляют щелочь. Сравнивают полученные результаты.
4.4. Карбонильные соединения (альдегиды, кетоны)
Качественные реакции карбонильных соединений многочисленны и разнообразны, что объясняется склонностью карбонильных соединений вступать в различные реакции замещения и присоединения. Альдегиды и кетоны ведут себя в этих реакциях почти одинаково. В некоторых случаях существует, однако, различие в скорости протекания реакций, чем и пользуются для того, чтобы различить карбонильные соединения разных групп (например, отличить альдегиды от кетонов, альдегиды жирного ряда от ароматических и
т. д.). В качественном анализе используется также реакция окисления.
Получение производных и количественный анализ карбонильных соединений основаны, главным образом, на реакциях замещения и присоединения.
1. Реакция с 2,4-динитрофенилгидразином. Карбонильные соединения можно обнаружить по реакциям с фенилгидразином и замещенными фенилгидразинами. Лучшие результаты дают и наиболее часто применяются 2,4-динитрофенилгидразин, n-нитрофенилгидразин и n-карбоксифенилгидразин:
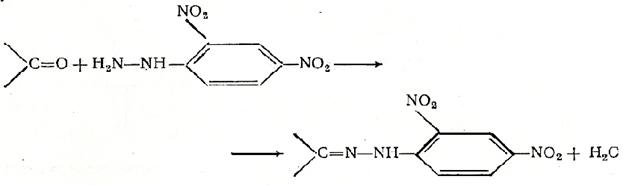
Образующиеся в этой реакции замещенные фенилгидразоны плохо растворимы в воде и поэтому обнаружение карбонильных соединений можно проводить в разбавленных водных pаствopax.
Опыт. Наливают в три пробирки по l мл солянокислого раствора 2,4-динитрофенилгидразина и добавляют по 1-2 капли следующих карбонильных соединений: в первую - ацетона, во вторую - метилэтилкетона, в третью - формалина. Наблюдают выделение желтых осадков.
2. Реакция с солянокислым гидроксиламином. Соединения, содержащие карбонильную группу, при взаимодействии с солянокислым гидроксиламином выделяют свободную соляную кислоту:
![]()
![]()
![]()
![]() С=O + H2NOH*HCI ® C=NOH+Н2О +НСI
С=O + H2NOH*HCI ® C=NOH+Н2О +НСI
Изменение рН среды можно обнаружить по изменению окраски индикатора, например, метилового оранжевого.
Опыт. В пробирку налить 2 мл 2%-ного раствора солянокислого гидроксиламина, добавить 1 мл ацетона, затем несколько капель метилового оранжевого. Сравнить окраску раствора в пробирке с окраской метилового оранжевого в 2%-ном растворе солянокислого гидроксиламина. Опыт повторить с метилэтилкетоном и бензальдегидом.
3. Реакция с [Ag (NНз) 2]0Н – реакция «серебряного зеркала». Все альдегиды восстанавливают аммиачный раствор окиси серебра:
R-C=O + 2 [Ag (NНЗ)2] ОН ® R-C=O + 2Ag ↓+ Н2О + 3NНз
ç ç
Н ОNH4
Выделяющееся металлическое серебро оседает на стенках пробирки в виде зеркала. Эту реакцию могут также давать некоторые ароматические амины, многоатомные фенолы и дикетоны.
О п ы т. В тщательно вымытую пробирку с 5 мл реактива – аммиачного раствора оксида серебра добавить 5 капель формалина или ацетальдегида. Смесь осторожно нагреть на водяной бане при температуре 60-70°. Выделяющееся через некоторое время металлическое серебро оседает на стенках пробирки в виде металлического зеркала. Повторить опыт, взяв вместо альдегида кетон, например, ацетон. Объяснить, почему ацетон не восстанавливает серебро.
4. Реакция с реактивом Фелинга. Альдегиды жирного ряда восстанавливают Cu (II+) в Cu (I+). В качестве реактива, содержащего ионы Cu (II+), применяют реактив Фелинга. Реактив Фелинга готовят перед употреблением, смешивая равные объемы двух растворов: 1) раствор CuS04 (34,6 г CuS04· 5Н2О растворяют в воде, подкисленной серной кислотой, доводят объем до 500 мл водой) и 2) щелочной pacтвоp сегнетовой соли - калиево-натриевой соли винной кислоты (173 г тартрат натрия-калия растворяют в 200 мл воды, добавляют раствор 70 г гидроксида натрия или 85 г гидроксида калия в 100 мл воды, разбавляют до 500 мл водой). При сливании растворов образуется гидрат окиси меди, который с сегнетовой солью дает комплексное соединение типа гликолята меди:
COOK COOK
![]() ç H ç O
ç H ç O
![]() CH¾O O¾CH //
CH¾O O¾CH //
![]()
![]()
![]() ½ Cu ç + R¾C +2H2O ®
½ Cu ç + R¾C +2H2O ®
![]() CH¾O O¾CH \
CH¾O O¾CH \
½ H ç H
COONa COONa
COOK
ç
CHOH
® R¾C=O + Cu2O¯ + 2 ç
CHOH
ç
COONa
Ароматические альдегиды эту реакцию не дают.
Опыт. Приготавливают в пробирке реактив Фелинга, сливая по 1 мл растворов 1 и 2, и прибавляют 2 мл 1 % -ного раствора глюкозы. Верхнюю часть содержимого пробирки нагревают в пламени горелки до начала кипения и наблюдают появление желтого или красного осадка закиси меди. Параллельно проводят реакцию с формалином и бензальдегидом, прибавляя к 2 мл реактива Фелинга (по отдельности) по 2-3 капли формалина и 1-2 капли бензальдегида. Наблюдают происходящие изменения.
5. Восстановление гидроксида меди ацетальдегидом. К 0,5 – 1 мл 1%-ного раствора медного купороса прилить равный объем 10%-ного раствора гидроксида натрия. К образовавшемуся голубому осадку гидроксида меди прилить ацетальдегид и нагреть. Отметить изменение окраски в процессе нагрева.
4.5. Карбоновые кислоты.
В качествениом и количественном анализе карбоновых кислот используют их кислотные свойства. Для получення производных важны реакции замещения водорода или гидроксила в rpyппe ¾СООН.
1. Реакция на лакмус. Карбоновые кислоты дают отчетливую реакцию на лакмус. Влажная снняя лакмусовая бумажка окрашивается в красный цвет. Эта реакция достаточно чувствительна, так что даже для плохо растворимых в воде кислот получают хорошие результаты. Применение универсальной индикаторной бумажки позволяет более точно определить изменение рН среды. Следует иметь в виду, что кислую реакцию на лакмус могут показывать и другие органические соединения, не содержащие карбоксильной группы, - сульфокислоты, тиофенолы, нитрофенолы, пиримидины и др.
2. Реакция с бикарбонатом натрия. Выделение двуокиси углерода при добавлении исследуемого вещества к водному раствору бикарбоната натрия может являться доказательством наличия карбоксильной rpyппы. В этом случае, кроме карбоновых кислот, только сульфокислоты, ди - и тринитрофенолы, барбитуровая кислота и некоторые другие оксипиримидины дают положительную реакцию.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



